为儿科创新开辟无障碍通道
发布时间:2024-01-10 15:09:18作者:吴俭宁 刘鑫荣来源:医药经济报
儿童适宜的药品供应不足是全球大部分国家面临的难题,儿童专用的药品品种、剂型和规格较少,导致儿童不合理用药普遍、用药依从性不佳。为加速国内儿童用药品种的上市进程,原国家食品药品监督管理总局2016年2月26日发布的《关于解决药品注册申请积压实行优先审评审批的意见》和2017年12月28日发布的《关于鼓励药品创新实行优先审评审批的意见》提出:具有明显临床优势的儿童用药品可申请优先审评审批。2020年7月1日起施行的《药品注册管理办法》第三节第六十八条中规定,符合儿童生理特征的儿童用药品新品种、剂型和规格,且具有明显临床价值的药品,可在上市许可申请时申请适用优先审评审批程序。
本文根据国家药品监督管理局药品审评中心(CDE)优先审评公示信息和药智网数据库检索结果,对2018年至2023年12月26日纳入优先审评儿童用药品种的药品注册申报、剂型和治疗领域、医保准入等情况进行简要分析。
药品注册申报统计
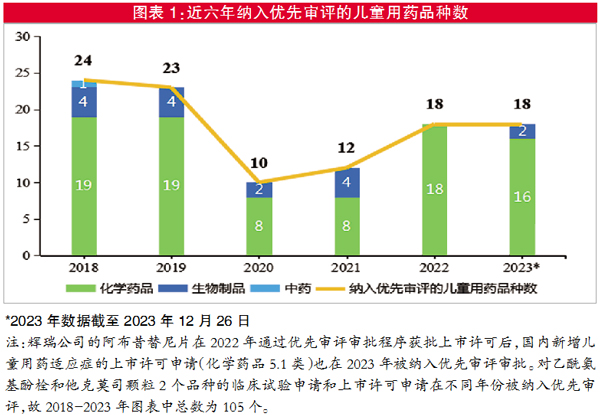
2018年1月1日至 2023年12月26日(以CDE承办日期计),共102个儿童用药品种被纳入优先审评审批程序,平均每年约18个(见图表1)。这些品种中,已有64个获批上市许可,包括50个化学药品、13个生物制品和1个中药;另有5个品种的上市许可申请未获CDE批准。已获批上市许可的品种从CDE承办日期起计算,至获批上市许可耗时中位数为459个自然日(15.3个月),最快如诺西那生钠注射液,耗时176个自然日(5.9个月)即获批上市许可。
102个被纳入优先审评的儿童用药品种中,境内生产的品种49个,境外生产的品种53个;新药品种57个,仿制药品种45个(化学药品3类、5.2类,原生物制品15类)。
对于国内未上市的儿童用药品种,如有多家企业先后在递交上市许可申请时申请优先审评审批程序,则均会被纳入优先审评。例如,远大医药的卡谷氨酸片作为儿童用药新品种被纳入优先审评后,在获批上市许可前,还有2家企业卡谷氨酸片剂的上市许可申请以相同理由被纳入优先审评。类似的品种还有4个:Sabin株脊髓灰质炎灭活疫苗(Vero细胞)、氨己烯酸散、盐酸普萘洛尔口服溶液、盐酸曲恩汀胶囊。
剂型和治疗领域分布
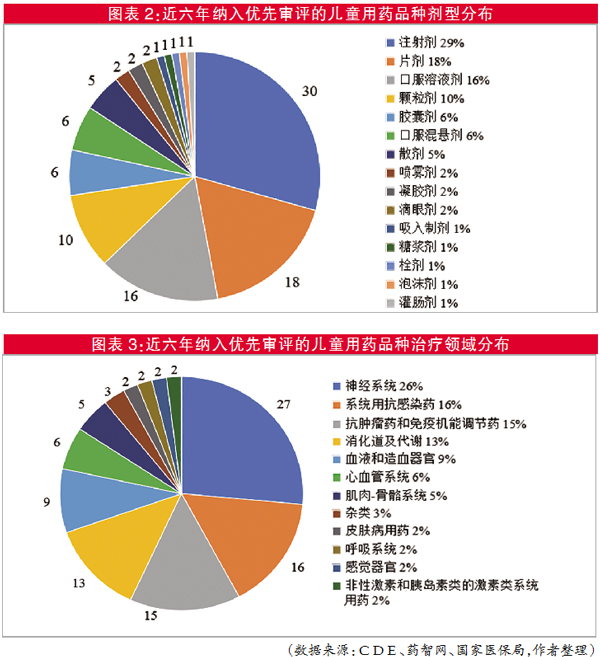
近六年纳入优先审评的儿童用药品种剂型分布较集中,以注射剂、片剂、口服溶液剂和颗粒剂为主(见图表2)。
为解决儿童用药的依从性差、拆分规格难的问题,儿童用药剂型改良的热点方向是口服溶液剂、糖浆剂等口服液体制剂。值得关注的是,近六年被纳入优先审评的儿童用药品种中出现了微型片剂(微片)、无针注射皮内给药系统、口颊粘膜溶液等适合儿童用药的新剂型。
例如,巯嘌呤微片是一种抗肿瘤药,片剂直径<3mm、规格是成人用药品的十分之一,方便根据患儿临床用药需求调整用量。咪达唑仑口颊粘膜溶液是颊粘膜给药的中枢神经系统抑制剂,将药液按剂量注入到患儿的面颊和牙龈之间,能够迅速控制急性惊厥发作。盐酸利多卡因无针注射皮内给药系统利用氦气高压喷射来实现无针注射透皮给药,用于儿童静脉穿刺或外周静脉插管前皮肤局部麻醉。这些儿童用药的新剂型给药方便、剂量准确且调整灵活,为儿童用药带来新的选择。
近六年纳入优先审评的儿童用药品种治疗领域以神经系统、系统用抗感染药、抗肿瘤药和免疫机能调节药、消化道及代谢4个治疗领域为主(见图表3)。神经系统药品适应症主要分布在抗癫痫(10个)和催眠镇静领域(7个)。
医保准入有关情况
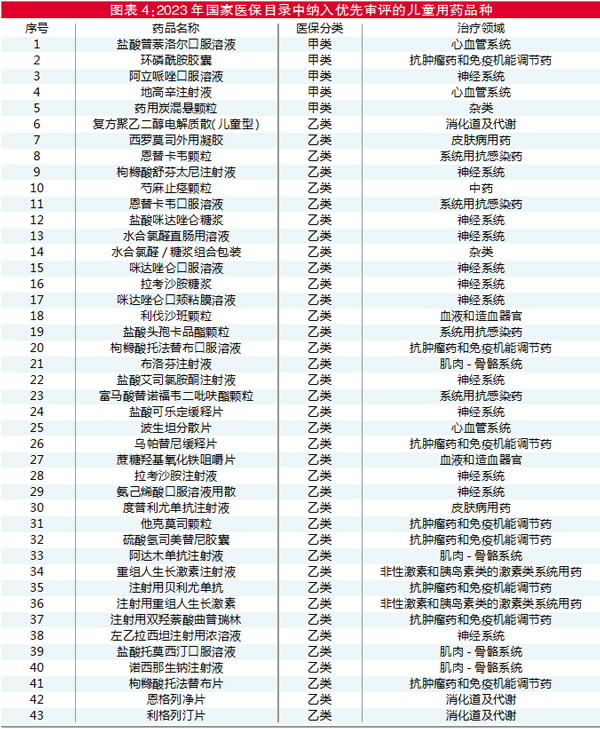
在纳入优先审评、且获批上市许可的儿童用药品种中,有43个品种已进入2023年国家医保药品目录(见图表4),占已获得上市许可同类品种的67%(43/64),其中5个为甲类,38个为乙类。
在2017年国家医保目录调整时,儿童用药进入医保目录首次得到关注。2020年、2022年和2023年的国家医保目录调整工作方案明确将《鼓励研发申报儿童药品清单》中的儿童用药品种纳入新增范围。预计未来以儿童用药新品种为理由纳入优先审评、或纳入《鼓励研发申报儿童药品清单》中的药品在上市后进入医保药品目录可能性更大。
>>>结语<<<
儿童并不是缩小版的成人。儿童因正处于成长发育过程,对药物的吸收、分布、代谢和排泄过程与成人有一定的差异,不同年龄段儿童群体间也存在差异。儿童群体因缺乏剂量合理性、有效性、安全性数据和适宜剂型、规格的药品,长期以来呈现“剂量靠猜,分药靠掰”的局面。研发儿童用药需要合理设计儿童临床试验来获得相关人群的数据,根据不同年龄段儿童的特点对剂型和规格进行改良,具有研发难度。将具有临床优势的儿童用药新品种、剂型和规格纳入优先审评,能够提高儿童用药品的可及性,进一步保障儿童群体用药有效、安全。
近六年,纳入优先审评的儿童用药品种绝大多数是化学药品,且境内生产和境外生产的品种,以及新药和仿制药约各占一半。剂型除传统的注射剂、片剂和口服液体制剂外,出现了微片、无针注射皮内给药系统、口颊粘膜溶液等儿童专用的新剂型。预计未来医保准入品种会继续向纳入优先审评的儿童用药新品种、以及进入《鼓励研发申报儿童药品清单》儿童用药品种倾斜。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






