中药创新固“真”气去“虚”火
发布时间:2023-10-24 15:40:58作者:本报记者 齐欣来源:医药经济报
10月18日,国家药监局药审中心发布的《基于人用经验的中药复方制剂新药药学研究技术指导原则(试行)》(下称《指导原则》)提到,人用经验是中医药理论、人用经验和临床试验相结合的中药注册审评证据体系(简称“三结合”中药注册审评证据体系)的重要组成部分,是在临床实践过程中积累形成的,可用于支持中药复方制剂新药的研发决策或注册申请。有专家表示,“充分重视‘人用经验’对中药安全性、有效性的支撑,同时明确注册申请人可根据中药人用经验对中药安全性、有效性的支持程度和不同情形,在研制时可选择不同的临床研究路径,将极大地激发中药新药研制的活力。”
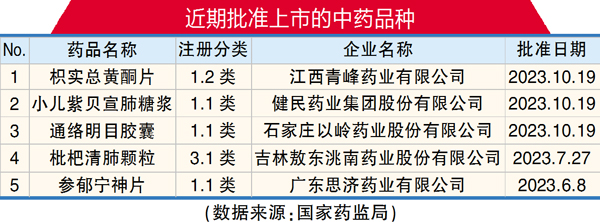
中药新药再结硕果
根据10月19日国家药监局官网信息,中药1.1类创新药小儿紫贝宣肺糖浆、通络明目胶囊,和1.2类中药创新药枳实总黄酮片的上市注册申请相继获批。
以中医临床价值为本
近年来,我国中药新药上市不断加速,中药新药临床试验和上市申请数量、批准数量同步增加。数据显示:2018年至今年7月初,我国已批准31个中药新药上市。加上7月27日披露的按古代经典名方目录管理的中药复方制剂(即中药3.1类新药)枇杷清肺颗粒获批上市,以及最新批准的3个药品,总计已达35个。
其中,中药复方新药是中药新药的重要组成部分。今年7月1日起,《中药注册管理专门规定》正式施行。支持研制基于古代经典名方、名老中医经验方、医疗机构中药制剂等具有丰富中医临床实践经验的中药新药。
院内制剂转化热
目前,医疗机构制剂转化新药热情高涨,对于医疗机构中药制剂转化为新药,广州中医药大学第一附属医院副院长杨忠奇在一场行业会议上表示,“医院制剂新药转化需要对处方的中医药理论依据、临床需求、药学基础、人用经验数据和质量进行评估。”他提到,部分制剂临床疗效和安全性缺乏可评价的数据,部分传统制剂多、工艺落后、剂型落后、环境污染大,部分制剂粗糙、生产资源利用率低且无法大规模生产,有的制剂包装、标签、说明书也不规范。中药新药应以“中医临床价值观”为指导,发现其治疗作用、辅助治疗作用、改善疾病症状、提高生活质量、治未病、给患者提供治疗选择、使用方便、药物经济学优势、与西药合并使用减毒增效等应用,并评估目标适应症的流行病学情况和治疗方法,与已有上市药品和其他治疗手段进行比较。
观察<<<
谨防“新药不新”
将已有的中药人用经验整合入中药的审评证据体系,长期以来一直是业界的呼声。有专家表示,“中医药学极其注重临床实践,中医药具有悠久的人用经验和数据,人用经验反映了中药的实践性特点。中药研制一般具有‘源于临床,用于临床’的特点,中药新药在上市前多数已有一定的人用经验。”
2022年CDE颁布的《基于人用经验的中药复方制剂新药临床研发指导原则(试行)》明确,“中药复方制剂新药研发应以患者为中心、以临床价值为导向、体现中医药的作用特点、发挥中医药的临床优势,以病证结合、专病专药或证候类中药等多种方式开展,明确患者的临床获益。”此次新发布的《指导原则》也提到,“人用经验所用药物来源包括中医临床经验方和医疗机构中药制剂等。支持注册申请的人用经验应当是高质量的中医临床实践的科学总结。”
在各项政策加持下,以上市公司为代表的中医药企业亦在加大研发创新投入。根据2023年半年报,以岭药业在研中药创新药品种达40余个,涉及临床12个系统疾病。康缘药业近三年已累计获批4个中药新药产品,今年上半年的研发费用达到3.63亿元,同比增长31.02%。健民药业截至今年上半年的新药研发项目也有27项。
在杨忠奇看来,目前已上市中药品种众多,许多产品功能主治雷同,应注重分析其临床优势或治疗特点,避免中药新药开发出现低含金量的创新“虚火”。同时,人用经验与临床经验总结有显著差别,人用经验研究作为药品注册资料是在有关药品法规监管范围之内,研究者要牢固树立合规意识。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






