荨麻疹管线新机制探究活跃
发布时间:2023-07-26 11:35:34作者:石军 陈慧 综合编译来源:医药经济报
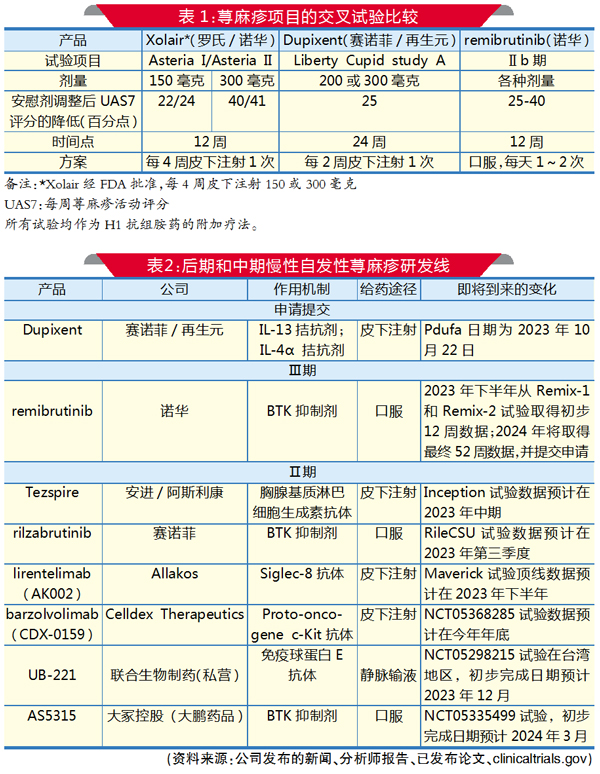
在慢性自发性荨麻疹(CSU)市场上,诺华和罗氏生产的Xolair处于垄断地位已经有一段时间了。但是,随着赛诺菲和再生元开发的Dupixent被批准用于这种皮肤病,预计今年格局将会有所变化。
而在未来6~12个月的时间里,有好几个后期研发项目将报告临床试验数据,其中包括来自诺华和赛诺菲的BTK抑制剂。安进、阿斯利康以及几家规模较小的公司(比如Allakos和Celldex)也在全力争夺市场份额。
Xolair树立标杆
荨麻疹是一种炎症性皮肤病,其特征是发痒性荨麻疹和肿胀。对CSU的一线治疗是H1抗组胺药,但许多患者即使在治疗之后仍然存在症状。
诺华和罗氏开发的Xolair在2014年被批准作为抗组胺药的一种附加疗法,但患者对此做出的治疗反应可能不一致。这只抗IgE抗体也携带黑框警告标志,提示可能导致过敏反应。
Xolair还被批准用于治疗中度至重度哮喘和鼻息肉,去年实现总销售额37亿美元。但是,针对该药有好几只生物类似药正在开发中,根据Evaluate Pharma汇总的市场分析人士的一致意见,到2028年,该药的总销售额预计将达14亿美元。
Berenberg公司估计,CSU在美国年销售额可达20亿美元,全球年销售额70亿~80亿美元,不过,该公司并没有给出达成这些目标的具体日期。
另一种治疗选择是赛诺菲和再生元开发的Dupixent,预计将在今年10月的PDUFA日期前获得FDA批准用于CSU。从疗效来看,这只可以抑制IL-4和IL-13信号传导的IgG4抗体与使用低剂量的Xolair效果同等。此外,由于目前没有携带黑框警告标志,Dupixent可能在安全性方面具有优势。
为了扩大患者群体,赛诺菲和再生元对使用Xolair难以治疗的CSU患者,使用Dupixent进行了测试,但试验遭遇失败。
BTK安全性较量
Xolair由诺华与罗氏旗下基因泰克合作开发和推广,于2003年首次获批,用于治疗症状难以控制的哮喘患者,2014年再次获批用于对H1抗组胺药物难治的CSU。在美国和欧洲,Xolair已失去专利保护。鉴于Xolair生物类似药的威胁迫在眉睫,诺华正在Ⅲ期试验中对一只布鲁顿酪氨酸激酶(BTK)抑制剂remibrutininb展开研究,其口服给药的便利性使该药与Dupixent不同。Remix-1和Remix-2这两项Ⅲ期研究预计将在今年下半年报告12周的试验数据,明年将获得52周的最终试验数据并提交申请资料。
Ⅱb期研究中展示出的疗效使得该试验项目与Xolair和Dupixent不相上下。不过,需要注意交叉试验比较。Ⅱb期研究中的安全性似乎也是可控的,2.6%的患者由于出现不良事件而停止使用remibrutininb,而安慰剂组则没有出现这种情况。最常见的不良事件包括头痛、恶心、腹泻和呼吸道感染。
产品的安全性似乎已经让用于治疗CSU的另外一种不同的BTK抑制剂成为泡影。罗氏的fenebrutinib此前显示出治疗CSU功效,但在Ⅱ期试验阶段也造成了3级肝毒性。
另外一种BTK抑制剂,赛诺菲的rilzabrutinib仍在接受试验中,预计Ⅱ期试验数据将在今年第三季度末公布。这项名为RileCSU的研究包括没有使用过Xolair的患者,或者对Xolair的治疗反应不完全的患者。对后一类患者群体开展的试验需要取得成功,才能使rilzabrutinib与竞争对手有所不同。不过,该药先前针对天疱疮(一种导致水泡和溃疡的自身免疫性皮肤病)试验遭遇的失败降低了人们的期待。
拓展机制研究
除了BTK抑制剂以外,制药公司还在测试其他几种作用机制。安进和阿斯利康的Tezspire是一种胸腺基质淋巴细胞生成素(TSLP)阻滞剂,该药已被批准用作严重哮喘的附加疗法。据悉,TSLP驱动下游T2细胞因子的释放,包括IL-4、IL-5和IL-13,导致炎症和哮喘症状。而IL-4和IL-13是Dupixent靶向作用的因子。
针对Tezspire的Ⅱ期Inception试验已经完成,预计很快会公布试验数据。该研究包括一个Xolair对照组,也有单独的Tezspire研究组。主要研究终点是在16周时与7日内荨麻疹活动度评分(UAS7)的基准线相比所发生的变化。
此外,Allakos公司正在对其唾液酸结合免疫球蛋白样凝集素8(Siglec-8)抗体lirentelimab进行测试。Siglec-8在嗜酸性粒细胞上高度表达,但尚不确定嗜酸性粒细胞耗竭是否具有临床意义,这从之前针对罕见炎症性胃肠道疾病的两次临床试验遭遇失败中可以明显看出。
针对lirentelimab的Ⅱ期CSU研究Maverick预计将在今年下半年报告试验数据,该项研究包括了之前使用过Xolair的患者。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






