生物类似药集采宜稳妥适度
发布时间:2023-02-27 11:16:40作者:风轻来源:医药经济报
2018年至今,除了化药、中成药外,关于生物类似药何时纳入带量采购的范围,业内一直存在各个角度的讨论与建议。日前,福建、安徽、河北等省份集采均出现生物药的影踪,生物类似药纳入带量采购的脚步似乎越来越近。
“似”如破竹
2018年是中国生物类似药的元年。当年6月,纳武利尤单抗正式通过国家药监局批准。同年12月,中国首个国产PD-1特瑞普利单抗获批上市。2019年2月25日,复宏汉霖的利妥昔单抗注射液上市,之后百奥泰生物的阿达木单抗注射液、海正的阿达木单抗注射液和齐鲁制药的贝伐珠单抗注射液在2019年11月7日、12月6日、12月9日先后获批上市。
仅仅几年间,中国的生物类似药获批上市堪称突飞猛进。以PD-1为例,目前国内获批上市的品种已经呈现快速井喷状。如贝伐珠单抗,2017年起经历了安徽、湖北、北京、天津、河北等五地抗癌药专项带量采购,其价格走势呈现明显下降趋势。以价换量的结果是,这个品种的销售金额有明显攀升。根据药渡仿制数据库数据,该品种的国内样本医院销售金额大约在75亿元左右。
审慎推进
近几年生物药是研发热点,也是国谈的热点产品,其关注度一直很高。从市场体量看,虽然部分生物类似药看似已经具备了集采的一些条件(如竞争相对充分、市场体量大),但要充分考虑的是,包括PD-L1、RANKL、CD20等各类靶点的药品,在质量、安全性和有效性方面,无法做到与原研药百分百相同。
其验证之路也包含多种不确定性。据有关数据分析,尽管生物类似药物的各级蛋白结构几乎一致,但工艺制作流程存在较多差异,包括选用的 DNA 载体、表达蛋白的细胞系、发酵条件、纯化工艺等因素,都会使结构几乎相同的蛋白质药物存在大量大同小异的衍生物。同时,选用辅料的不同也可能导致药物的疗效出现差异。
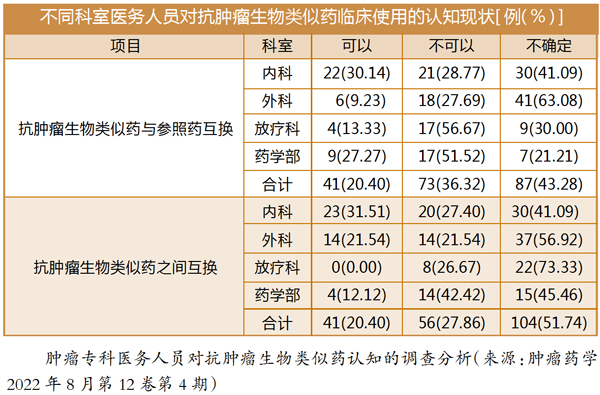
另一方面,医院临床各科室对生物类似药的替代持怎样的态度也极为关键。南方某肿瘤专科医院一项针对院内各科室进行的调查显示,不同科室和职业的医务人员对抗肿瘤生物类似药概念和特点的认知均不相同(见下图)。
因此,笔者建议,生物类似药的带量采购仍可遵循“稳定市场、保障供应、适度降幅”的原则,尽量将临床作用机制和治疗效果相似的药品合并为一个采购组,实现相互替代与竞争。对于降幅“及格”的品种,给予基础量的保护;对于实现超额降幅的品种,给予待分配量的待遇。
总之,生物类似药集采要慎之又慎,既要充分考虑中国医药行业创新发展的大局,也要思考具体落地时对临床应用的影响。更重要的是,如何在保证市场供应平衡的前提下适度降价,让各方满意。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






