近五年上市新药构成洞悉
发布时间:2023-02-20 11:02:58作者:刘鑫荣 吴俭宁来源:医药经济报
2月15日,国家药品监督管理局药品审评中心(CDE)连发多项药物评价/研究技术指导原则,旨在规范药物临床试验与研究,促进新药研发。近年来,我国创新药研发整体呈上升趋势,据现行《药品注册管理办法》创新药定义,以CDE年度药品审评报告建议批准/审评通过上市许可的创新药品种和NMPA官网公布正式批准上市许可时间为准,统计五年间(2018-2022年)NMPA共批准上市许可63个化学药品创新药和26个生物制品创新药。现对这两项五年数据作进一步分析。
化学创新药
近八成全球首发
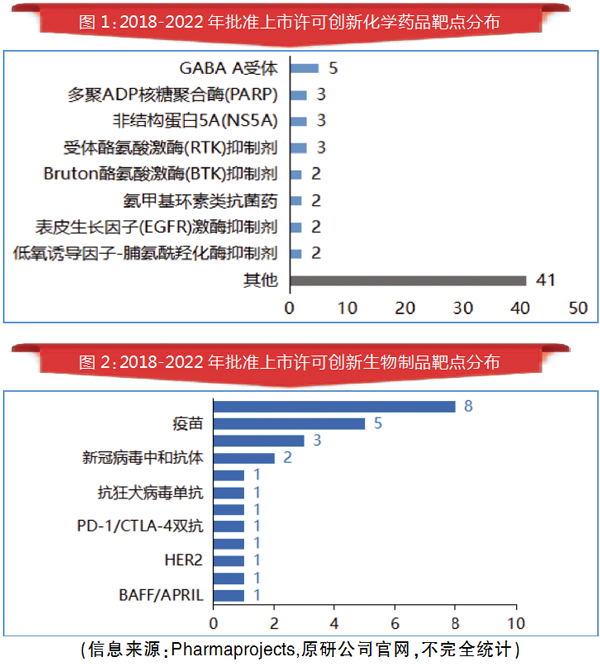
2018-2022年NMPA批准上市许可创新化学药品靶点分布见图1,其中,获批最多的γ-氨基丁酸A型受体(GABAA受体)有5个品种(4个活性成分),分别为:注射用磷丙泊酚二钠、环泊酚注射液(2个不同的适应症分别在不同的时间提交NDA,提交时该活性成分无任何制剂在全球获批上市许可,因此按药品注册类别统计为2个化学药品创新药)、注射用苯磺酸瑞马唑仑、注射用甲苯磺酸瑞马唑仑。
在2018-2022年国内批准上市许可的化学药品创新药中,国外全球首批的品种有13个:非奈利酮片、维立西呱片、替戈拉生片、阿布昔替尼片、注射用甲苯磺酸奥马环素、甲苯磺酸奥马环素片、利司扑兰口服溶液用散、普拉替尼胶囊、注射用苯磺酸瑞马唑仑、泽布替尼胶囊、西尼莫德片、甲苯磺酸尼拉帕利胶囊、达可替尼片。
2019年11月14日,百济神州(苏州)生物科技有限公司的泽布替尼胶囊在美国获得FDA全球首次批准上市许可,这是我国制药企业抗癌创新药“出海”全球规范医药市场首次获得批准上市许可“零的突破”。2020年6月2日我国批准泽布替尼胶囊上市许可,现已在全球近20个国家或地区上市。据米内网数据,2021年泽布替尼胶囊(商品名:百悦泽)国内样本医院及药店放大销售金额约8.5亿元(其中公立医院4.4亿元,实体药店4.1亿元)。
2018-2022年批准的63个化学药品创新药中,有50个品种在我国获得全球首次批准上市许可。
突破性治疗药物+优先审评审批:包括羟乙磺酸达尔西利片、甲磺酸氟马替尼片、可利霉素片、达诺瑞韦钠片4个品种。
附条件批准+优先审评审批:15个品种。阿兹夫定片是获得附条件批准和优先审评审批的品种之一,本品与核苷逆转录酶抑制剂及非核苷逆转录酶抑制剂联用,适用于治疗高病毒载量的成年HIV-1感染患者。本品种是新型核苷类逆转录酶和辅助蛋白Vif抑制剂的化学药品1类首创新药(First-in-Class),也是首个上述双靶点抗HIV-1药物,能够选择性进入HIV-1靶细胞外周血单核细胞中的CD4细胞或CD14细胞,发挥抑制病毒复制功能。其获批上市为HIV-1感染者提供了新的治疗选择。
附条件批准:1个品种,即甘露特钠胶囊。
优先审评审批:34个品种。盐酸安罗替尼胶囊(Anlotinib Hydrochloride Capsules)被纳入优先审评审批程序获得批准上市许可。该品种是小分子多靶点的受体酪氨酸激酶抑制剂,是我国自主研发的创新药,用于治疗晚期或转移性非小细胞肺癌。盐酸安罗替尼是在已上市同类药物索拉非尼基础上改构而成,作用靶点包括血管内皮细胞生长因子受体(VEGFR1-3)、成纤维细胞生长因子受体(FGFR1-4)、干细胞因子受体(c-KIT)、血小板源生长因子受体(PDGFR-β)等激酶,通过抑制肿瘤新生血管生成(VEGFR,FGFR,PDGFR)和生长增殖(c-KIT)信号通路发挥抗肿瘤作用。在关键的Ⅲ期临床试验(ALTER0303)中证实,对于现有治疗无效或失败的晚期非小细胞肺癌,安罗替尼相对安慰剂组可明显提高总生存期,为非小细胞肺癌患者提供了新的治疗手段。
米内网数据显示,盐酸安罗替尼胶囊在获批当年2018年国内公立医院及实体药店合计实现销售额7.2亿元,经过3年的市场推广,2021年销售额达44.9亿元。
新生物制品
PD-1约占三分之一
2018-2022年批准上市许可生物制品创新药26个品种。从靶点来看,PD-1有8个品种,均为全球首次批准抗肿瘤用药。26个品种靶点分布见图2。
突破性治疗药物+附条件批准+优先审评审批:1个品种,注射用维迪西妥单抗。
附条件批准+优先审评审批:4个品种。卡度尼利单抗注射液、恩沃利单抗注射液、瑞基奥仑赛注射液、注射用泰它西普。
附条件批准+特别审批:6个品种。重组新型冠状病毒疫苗(5型腺病毒载体)、安巴韦单抗注射液、罗米司韦单抗注射液及3个新型冠状病毒灭活疫苗(Vero细胞)。
附条件批准:共2个品种。赛帕利单抗注射液、派安普利单抗注射液。
优先审评审批:10个品种。佩索利单抗注射液、普特利单抗注射液、斯鲁利单抗注射液、奥木替韦单抗注射液、重组结核杆菌融合蛋白(EC)、替雷利珠单抗注射液、注射用卡瑞利珠单抗、康柏西普眼用注射液、信迪利单抗注射液、特瑞普利单抗注射液。
小结<<<
创新药研发具有“三高一长”(高投入、高风险、高回报、长周期) 的特征,创新药研发成功的标志并不是经过十多年的研发获得批准上市许可,而是要看该创新药是否可用于治疗选择很少或没有治疗选择的患者,是否在安全性、有效性、易用性方面有所改进,更重要的是看能否投入商业化具有可及性和销售市场的成功,这才是真正的成功的创新药,是激发持续投入研发创新药的源动力。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






