2022医疗器械注册深度盘点
发布时间:2023-02-13 13:43:26作者:摘编于国家药监局官网来源:医药经济报
近日,国家药监局发布《2022年度医疗器械注册工作报告》(以下简称《报告》)。
《报告》指出,2022年,国家药监局以习近平新时代中国特色社会主义思想为指导,深入学习贯彻党的二十大精神,全面落实党中央国务院重大决策部署,按照“四个最严”要求,坚持以人民健康为中心,坚持保安全守底线,促发展追高线,认真执行《医疗器械监督管理条例》,继续做好疫情防控产品审评审批工作,全面深化医疗器械审评审批制度改革,强化医疗器械注册管理,助推产业创新高质量发展,医疗器械注册管理各项工作有力向前推进。
《报告》详细介绍了2022年国家药监局的医疗器械注册工作情况、注册受理情况、注册审批情况。本版摘录重要信息,以飨读者。
注册工作情况
疫情防控服务保障全力以赴:共批准68个新冠病毒检测试剂。截至去年底,共批准新冠病毒检测试剂136个。并持续做好新冠病毒突变株监测和核酸、抗原检测试剂检出能力评估;新批准47个新冠病毒抗原检测试剂,延长已获批新冠抗原检测试剂注册证有效期,充分满足疫情防控需要;启动新冠病毒核酸采样设备应急审批;组织修订《医用外科口罩》《一次性使用医用口罩》行业标准;全程指导注册申请人做好体外膜肺氧合(ECMO)产品注册研发,推动产品尽快上市等。
促进产业创新高质量发展成果丰硕:批准首个国产质子治疗系统等创新医疗器械55个,优先审批医疗器械77个,创新医疗器械获批数量与2021年相比增加57.1%;与工业和信息化部联合启动生物医用材料创新任务揭榜挂帅工作;印发港澳医疗器械注册人在粤港澳大湾区内地9市生产医疗器械实施方案,推动区域产业发展;牵头组织推进海南博鳌乐城国际医疗旅游先行区临床真实世界数据应用试点工作,批准热蒸汽治疗设备及一次性使用前列腺热蒸汽治疗器械4个试点品种上市等。
医疗器械注册审评审批工作持续规范:修订发布《关于第一类医疗器械备案有关事项的公告》;开展境内第二类医疗器械注册清理规范,梳理第二类医疗器械近80000件,组织抽查31个省168个案卷;会同国家卫生健康委修订发布《医疗器械临床试验质量管理规范》(GCP);开展2022年度医疗器械临床试验监督检查(包括临床试验产品的真实性核查);发布《医疗器械注册质量管理体系核查指南》等。
医疗器械注册管理技术支撑体系不断完善:批准医疗器械行业标准制修订计划项目116项,审核发布行业标准114项,将92项强制性行业标准和在研项目转化为推荐性,废止20项强制性行业标准;会同工业和信息化部,组建医疗装备产业与应用标准化工作组;成立中医器械标准化技术归口单位;统筹推进新版GB 9706系列标准实施;及时研究明确热玛吉、水光针产品管理属性和类别;持续推进唯一标识工作;发布技术审查指导原则95项等。
医疗器械注册管理能力全面提升:继续做好政府购买服务项目,加强动态监测和工作绩效季度管理及评估;加大全国医疗器械技术审评人员培训力度,制定实训基地建设工作方案,统筹北京、上海、江苏、浙江、山东、广东等6个实训基地工作,线上开展专业培训12次,培训8000多人次;全面提升医疗器械注册信息化水平,2022年11月1日起全面发放医疗器械电子注册证,国家药监局全业务流程电子化基本完成;组织推进第二批监管科学研究6个重点项目,推动13个医疗器械子项目加快研究进度、加速成果转化;积极参与国际组织工作等。
注册受理情况
2022年,国家药监局依职责共受理医疗器械首次注册、延续注册和变更注册申请共计10571项,与2021年相比减少13.7%。
整体情况
受理境内第三类医疗器械注册申请5425项,受理进口医疗器械注册申请5146项。
按注册品种区分,医疗器械注册申请8105项,体外诊断试剂注册申请2466项。
按注册形式区分,首次注册申请2660项,占注册申请的25.2%;延续注册申请3964项,占注册申请的37.5%;变更注册申请3947项,占注册申请的37.3%。
分项情况
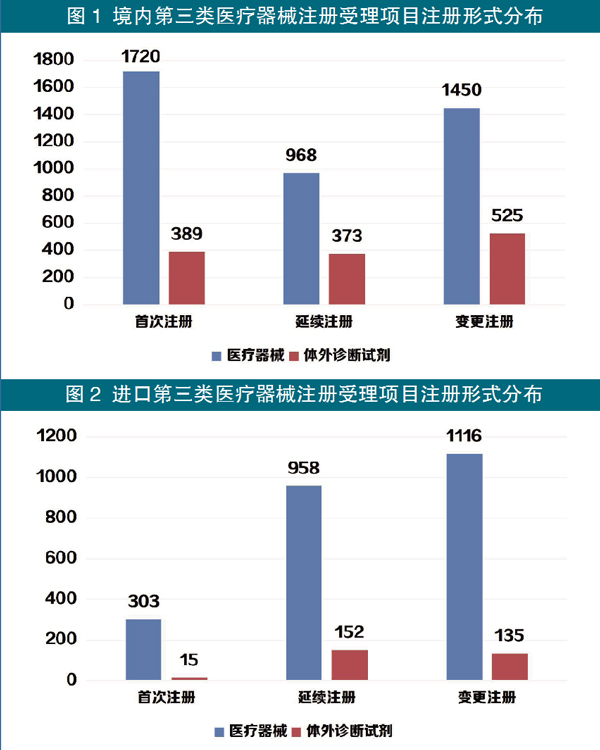
1.境内第三类医疗器械注册受理情况:共受理5425项,与2021年相比增加1.6%。其中,医疗器械注册申请4138项,体外诊断试剂注册申请1287项。
从注册形式看,首次注册2109项,占注册申请数量的38.9%;延续注册1341项,占注册申请数量的24.7%;变更注册1975项,占注册申请数量的36.4%。
2.进口第二类医疗器械注册受理情况:共受理2467项,与2021年相比减少33.1%。其中医疗器械注册申请1590项,体外诊断试剂注册申请877项。
从注册形式看,首次注册233项,占注册申请数量的9.4%;延续注册1513项,占注册申请数量的61.3%;变更注册721项,占注册申请数量的29.2%。
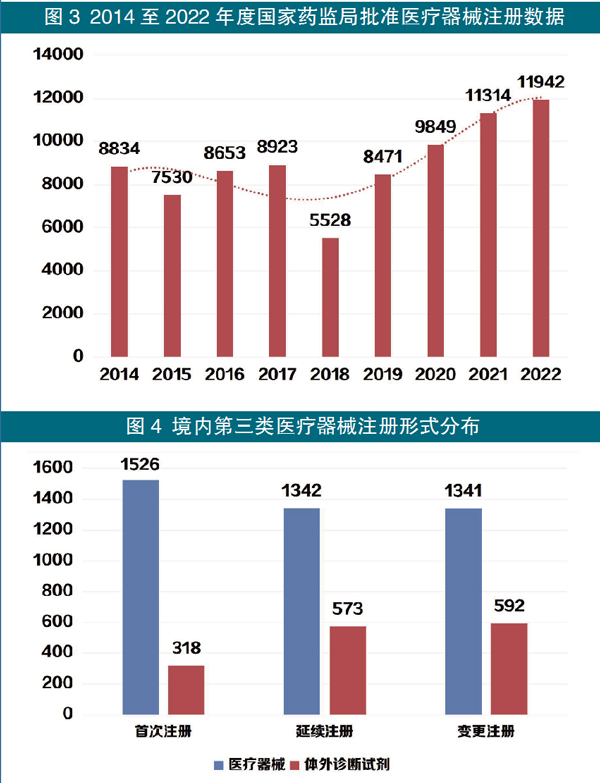
3.进口第三类医疗器械注册受理情况:共受理2679项,与2021年相比减少17%。其中医疗器械注册申请2377项,体外诊断试剂注册申请302项。
从注册形式看,首次注册318项,占注册申请数量的11.9%;延续注册1110项,占注册申请数量的41.4%;变更注册1251项,占注册申请数量的46.7%。
注册审批情况
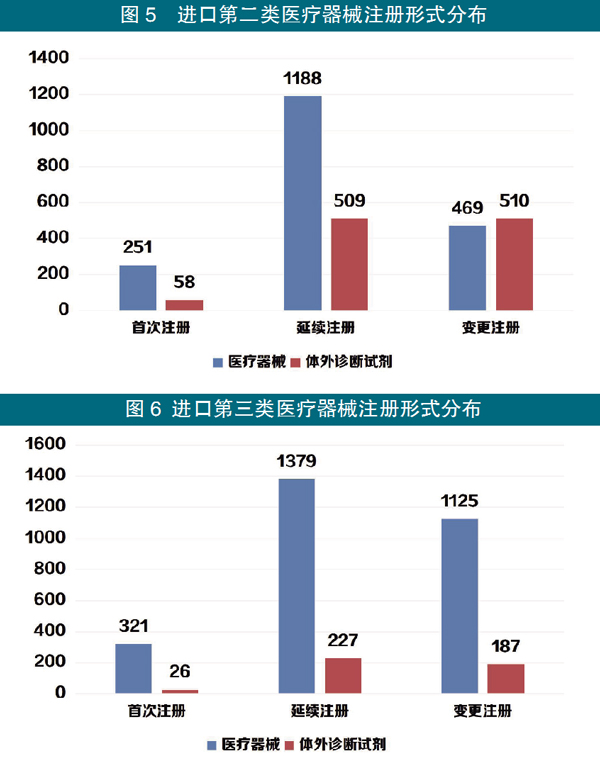
2022年,国家药监局共批准医疗器械首次注册、延续注册和变更注册11942项,与2021年相比注册批准总数量增长5.5%。
其中,首次注册2500项,与2021年相比增加46.2%。延续注册5218项,与2021年相比减少24.8%。变更注册4224项,与2021年相比增加58.5%。
2022年,企业自行撤回首次注册申请、自行注销注册证书214项。
整体情况
2022年,国家药监局批准境内第三类医疗器械注册5692项,与2021年相比增加23.8%,进口医疗器械6250项,与2021年相比减少7%。
按照注册品种区分,医疗器械8942项,占注册数量的74.9%;体外诊断试剂3000项,占注册数量的25.1%。
按照注册形式区分,首次注册2500项,占注册数量的20.9%;延续注册5218项,占注册数量的43.7%;变更注册4224项,占注册数量的35.4%。
分项情况
1.境内第三类医疗器械注册审批情况:共注册5692项。其中,医疗器械4209项,体外诊断试剂1483项。
从注册形式看,首次注册1844项,占注册数量的32.4%,延续注册1915项,占注册数量的33.6%;许可事项变更注册1933项,占注册数量的34%。
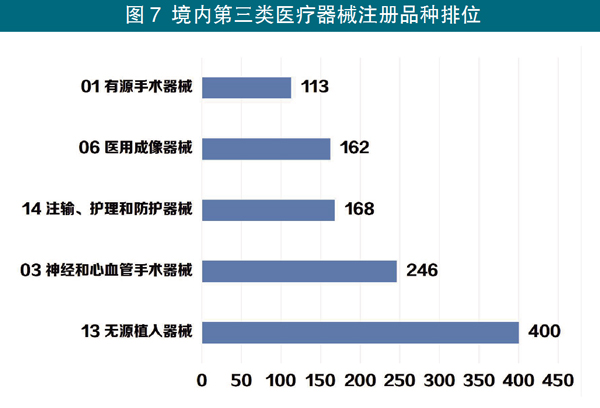
2.进口第二类医疗器械注册审批情况:共注册2985项。其中,医疗器械注册1908项,体外诊断试剂注册1077项。
从注册形式看,首次注册309项,占注册数量的10.4%;延续注册1761项,占注册数量的56.9%;许可事项变更注册1003项,占注册数量的32.8%。
3.进口第三类医疗器械注册审批情况:共注册3265项。其中,医疗器械注册2825项,体外诊断试剂注册440项。
从注册形式看,首次注册347项,占注册数量的10.6%;延续注册1606项,占注册数量的49.2%;许可事项变更注册1312项,占注册数量的40.2%。
具体批准品种种类分析
注册的境内第三类医疗器械,除体外诊断试剂外,共涉及《医疗器械分类目录》中18个子目录的产品。
注册数量前五位的境内第三类医疗器械是:无源植入器械,神经和心血管手术器械,注输、护理和防护器械,医用成像器械,有源手术器械。与2021年相比,神经和心血管手术器械注册产品数量超过注输、护理和防护器械,且相同类别注册数量均有大幅增加,其中有源手术器械增加76.6%,医用成像器械增加78%,神经和心血管手术器械增加92.2%,无源植入器械增加68.4%。
注册的进口医疗器械,除体外诊断试剂外,共涉及《医疗器械分类目录》中22个子目录的产品。
注册数量前五位的进口医疗器械,主要是:医用成像器械,无源植入器械,注输、护理和防护器械,口腔科器械,神经和心血管手术器械。与2021年相比,注输、护理和防护器械类产品取代眼科器械,相同类别产品注册数量略有增加。
进口医疗器械国别情况
2022年,共有28个国家(地区)产品在我国获批上市。
其中,美国、德国、日本、韩国、法国医疗器械在中国医疗器械进口产品首次注册数量排前5位,注册产品数量约占2022年进口产品首次注册总数量的76.4%,与2021年相比略有增加。
从进口医疗器械代理人分布看,共有18个省涉及有本省企业作为进口医疗器械代理人,其中上海市代理人代理的进口首次医疗器械数量最多,占全部进口医疗器械数量的62.4%。
境内第三类医疗器械省份分析
从2022年境内第三类医疗器械注册情况看,相关注册人主要集中在沿海经济较发达省份。
其中,江苏、广东、北京、上海、浙江是境内第三类医疗器械首次注册数量排前五名的省(市),占2022年境内第三类医疗器械首次注册数量的69.7%,与2021年相比增加1.8%。
创新医疗器械产品
2022年,国家药监局共收到创新医疗器械特别审批申请343项,比2021年增加37.8%,其中68项获准进入创新医疗器械特别审查程序。全年共批准55个创新医疗器械产品上市,比2021年增加57.1%。
2014年至2022年,国家药监局共批准189个创新医疗器械。其中,境内创新医疗器械涉及15个省的134家企业,进口创新医疗器械涉及2个国家的8家企业。
北京、上海、广东、江苏、浙江创新医疗器械获批产品数量和相应企业数量最多,约占全部已批准的189个创新医疗器械的82.5%。


此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






