专精特新“小巨人”厉兵秣马
发布时间:2023-01-05 15:49:48作者:特约撰稿 宁玉强来源:医药经济报
当前,我国正从制药大国向制药强国跨越。在世界经历百年未有之大变局之际,我国生物医药产业更要直面基础学科、研发投入、原始创新、行业标准、高端产品核心技术等方面的难题和挑战。“专精特新”企业具有细分领域专注度高、发展潜力大、创新能力强等特征,对于提升我国生物医药产业供应链韧性具有重大意义。截至2022年11月底,被评定为专精特新“小巨人”企业(以下简称“小巨人”)的总数为8997家,其中生物医药企业469家,占比为5.21%。
现状分析:医药“小巨人”特质
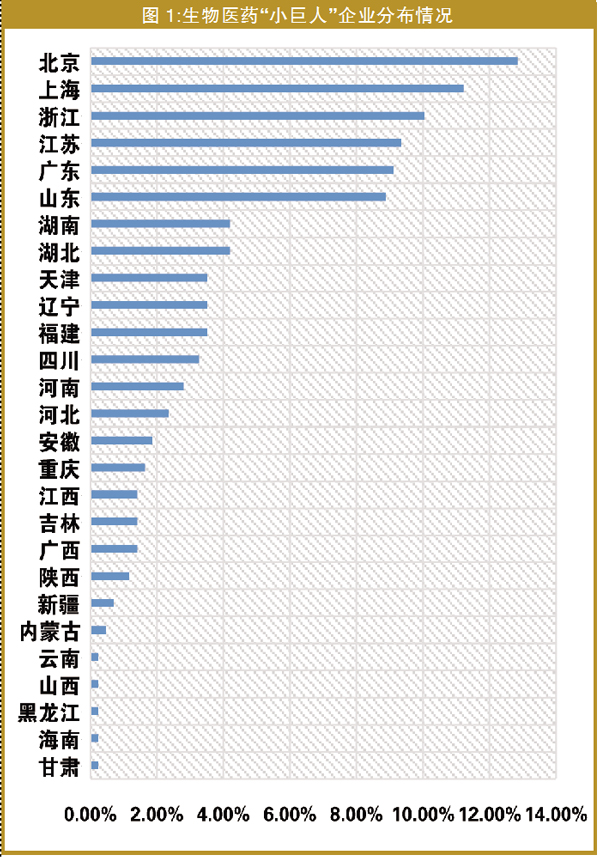
四大梯队初步形成
从区域分布来看,北京和上海的企业稳居第一梯队,拥有生物医药“小巨人”企业数量占比为24.07%;浙江、江苏、广东、山东等4个省份为第二梯队,拥有生物医药“小巨人”企业数量占比为37.38%;湖南、湖北、天津市、辽宁、福建、四川等6省(市)为第三梯队,拥有生物医药“小巨人”企业数量占比为22.20%;河南、河北、陕西等15个省(市、区)为第四梯队,拥有生物医药“小巨人”企业数量占比为16.36%。
六大领域全面覆盖
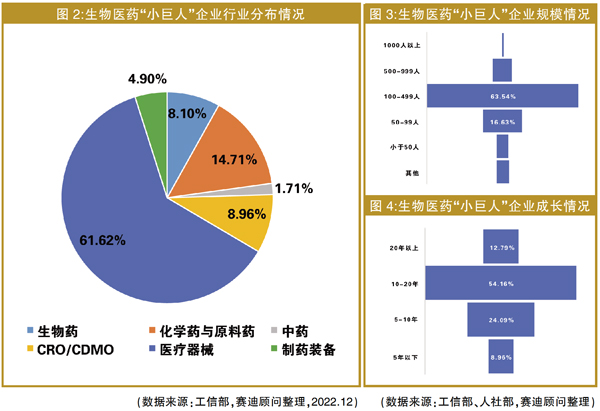
从产业分布来看,生物医药“小巨人”企业主要集中在医疗器械、化学与原料药、中药、生物药、制药装备、CRO/CDMO等六大领域。其中,医疗器械企业最多,占比为61.62%;化学与原料药企业第二,占比为14.71%;CRO/CDMO企业占比为8.96%;生物药企业占比8.10%;制药装备企业占比4.90%;中药企业最少,占比仅为1.71%。
腰部企业特征明显
从“小巨人”企业成长角度,一方面,从企业规模看,63.54%的企业从业人员在100~499人,21.75%的企业从业人员小于100人,仅有1.07%的企业从业人员在1000人以上。
另一方面,从成长周期看,54.16%的企业成立时间在10~20年;24.09%的企业成立时间在5~10年;12.79%的企业成立时间有20年以上;成立时间5年以下的企业占比仅为8.96%。
聚力难点:厘清束缚“风阻”
当前,生物医药“小巨人”企业的发展仍存在一些制约因素,涉及前沿领域的伦理、标准、临床转化,关键资源要素的自给能力,以及财政支持与鼓励制度等。
前沿领域配套政策待跟进
在前沿领域的相关创新探索过程中,仍存在伦理、标准、临床转化等无法及时明确的问题。
以现有药品评价体系为例,大多是基于化学药品制剂研发生产特点制定,而干细胞治疗、免疫细胞治疗等大分子生物技术治疗机理、生产方式等与小分子化学药有区别,传统评价体系无法与干细胞等前沿生物技术相适应,安全性评价和可靠性评价等有待完善。
标准方面,我国干细胞、AI医疗等领域标准制订处于探索阶段。而如果生物安全、伦理规范、质量等方面行业标准缺失,那么企业在研发生产过程中就无据可依,从而加剧产品上市风险。
鼓励与投入精准度尚不足
高投入、高风险是生物医药产业的特点之一。生物医药“小巨人”以民营企业为主,主要产品及布局具有首创型、开拓型特征,融资渠道多为社会资本,整体抗风险能力较弱。
在科研经费方面,我国需要更加有效、可持续性的财政支持与鼓励制度,对原创性、首创性的前沿研发项目的支持需要更多投入。此外,鼓励可持续性的多方合作研发机制仍待完善。
地方“小巨人”企业引培过程中,“重补贴轻补助、重后期轻前期”的支持方式一定程度上压抑了“小巨人”企业对前沿创新与突破性创新的热情与动力。
此外,我国医保和商业保险对创新型药械产品的支付体系尚待完善,加之创新型药械产品价格较高,导致民众对创新药械使用的渴望度与支付能力不匹配,医疗机构对创新药械产品的接受程度不高。这增加了创新型药械产品的商业化难度。
关键资源与分布均衡难题
从供应链看,高端生产设备、高端产品的核心技术和关键原材料等关键资源要素的自给能力不足,不仅增加生物医药产业链稳定发展的风险,也制约我国生物医药产业的健康发展。因此,构建稳定的生物医药供应链体系迫在眉睫。
从创新链看,一方面,49%的国家重点实验室集中在一线城市,北京、上海、广州最多,创新资源分布不均衡现象依然存在。另一方面,整体布局上,针对前沿领域、创新型产品的检测检验机构及相关设备配套不足,检验量相对有限,检测速度较慢。
未来引擎:插上腾飞“翅膀”
前瞻引导长效发展
对于前沿领域伦理、标准、临床转化等暂未及时明确的问题,笔者认为,可考虑创新提效,探索构建中国特色的创新型药械长效引导体系。
一是分阶段分类别设置审查规范。根据基础研究、临床应用和产业化等不同阶段,以及创新型药械产品的不同类别,综合考量原料、工艺等多方面因素,设置不同严格程度、不同审查标准的审查规范,加强基础研究支持,明确审查细则。
二是优化修订相关行业标准,促进前沿医疗领域行业快速发展。充分发挥生物医药“小巨人”企业在细分领域的技术优势和创新实践,联合一流科研机构围绕技术规范、研究标准、医学伦理等,完善创新型药械产品的临床试验、质控质检、疗效评价等行业标准,缩短创新型药械产品所属领域全流程的规范化和标准化制定周期。
三是在保证有效监管的基础上,减少行政审批事项,建立高效的创新产品上市机制。完善透明公正的市场准入制度,建立赏罚分明的市场运行机制,保障有实力的创新型企业获得长效发展支持。
重点保障要素资源
对于配套资源供给失衡的情况,笔者认为,可考虑精准施策,重点保障产业可持续高质量发展的要素资源。
一是发挥政府引导作用。针对生物医药产业的基础保障、重点/短板环节,制定系统的企业扶持政策,提升企业攻克技术难关的信心。依托专项课题、专项基金,鼓励生物医药企业间展开合作。
二是探索构建多层次的医疗支付体系,促进创新型产品商业化进程。适度扩大医保覆盖,针对可靠度较高、应用较为广泛的产品服务,分层次扩大医保报销比例,提升医疗患者使用创新型药械产品服务的动力,推动前沿技术、创新产品市场化、商业化进程。鼓励商业保险开发覆盖创新型药械产品全生命周期的责任险,参照首台(套)重大技术装备保险补偿机制,激发医疗机构使用创新型药械产品服务的积极性。
三是以提升科技成果转化率为目的,成立生物医药产业引导基金,聚焦能够解决专用设备、材料、工艺等共性问题的创新型企业,帮助提升抵御研发风险能力,推动科技成果工程化、产业化,增强产业供应链韧性。
产业主体多维合作
可考虑构建产业生态,引导产业主体多维合作实现协同创新。
一是充分发挥生物医药“小巨人”在细分赛道的先发优势。鼓励龙头企业搭建“政产学研医”协同创新平台,积极攻关下一代技术和产品,实现从“单一创新”向“融合创新”、“封闭式研发”向“开放式研发”的转变,帮助企业在细分赛道从“开拓者”转变为“领航者”。
二是组织开展创新型药械产品示范应用工程,鼓励国内医疗机构优先采购示范产品,对示范产品的市场表现分阶段评估,并对达标企业给予相应支持,树立行业榜样,提升“小巨人”企业品牌认可度。
三是鼓励干细胞、制药装备、高端医疗设备等领域企业与国际先进企业在技术开发、工艺提升、商业模式探索等方面开展交流合作,鼓励企业对国外市场进行投资布局。
(作者为赛迪顾问医药健康产业研究中心总经理)
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






