瓣膜快车道前赴后继
发布时间:2022-09-28 14:28:09作者:郑文秀来源:医药经济报
日前,宁波健世科技第三次向港交所递交招股书,拟在香港主板挂牌上市,中金公司及花旗为其联席保荐人。这是其于2021年6月21日、2021年12月21日先后两次递表失效之后的又一次申请。
健世科技创立于2011年,是国内结构性心脏疾病领域创新医疗器械企业,此前获得多起重磅融资,2021年完成了数亿美元新一轮融资,由高瓴创投、春华资本领投,天际资本、Cormorant、光远资本等知名投资机构跟投。
究竟瓣膜行业有着怎样的吸引力与大前景,能令企业对IPO念念不忘呢?本文将做相关梳理。
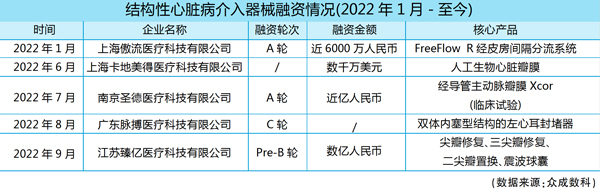
结构性心脏病介入器械
市场规模将超500亿元
结构性心脏病是近十余年心血管疾病领域一个新型的亚专业,弗若斯特沙利文数据显示,中国结构性心脏病介入器械市场规模持续扩大,预计2030年将达到595亿元人民币,针对心脏瓣膜病的治疗方式主要有药物治疗、外科手术及介入治疗。
目前,介入治疗已成为结构性心脏病最重要的发展方向。伴随着介入手术的发展,结构性心脏病介入器械逐渐成为一个高增长、大体量、高价值的成长行业,成为资本重点关注领域。2022年1月至今,已有5家企业获得融资,其中,臻亿医疗获得数亿人民币Pre-B轮融资,核心产品为二尖瓣修复、三尖瓣修复、二尖瓣置换、震波球囊。
结构性心脏病囊括各种原因导致的心血管结构异常,除多种先天性心脏病以外,瓣膜性心脏病是重要的一类结构性心脏病,发病率与老龄化密切相关。随着全球老龄化趋势加深,诊疗需求扩大,瓣膜产品的市场需求有望持续释放,被业内人士认为是未来引领心血管耗材发展的重点领域。据TCT(美国经导管心血管治疗会议)预测,2025年主动脉瓣膜产品的经济价值将超越冠脉支架。
根据心脏瓣膜结构,可以初步把治疗市场划分为主动脉瓣、二尖瓣和三尖瓣领域。
主动脉领域竞争激烈
未来格局尚不明朗
弗若斯特沙利文预计, 到2025年中国主动脉瓣患者将由2018年的800万人增加至2025年的930万人, 经导管主动脉瓣置换术市场的年复合增长率将达65%, 市场规模接近10亿美元。
对瓣膜性心脏病,目前的治疗方式主要有球囊扩张术(主要用于治疗患有先天性主动脉瓣狭窄的儿童及青少年患者)和主动脉瓣置换术,其中主动脉置换术又分为外科主动脉置换术以及经导管主动脉置换术。
经导管主动脉瓣置换术(TAVR)是指将组装完备的人工主动脉瓣经导管植入到病变的主动脉瓣处,在功能上完成主动脉瓣的置换。相比需要开胸的外科治疗,TAVR作为新的术式表现出诸多优势,如适合重症患者、不需要心脏停跳等。
据医械数据云统计,截至2022年7月底,我国仅有5件经导管主动脉置换系统获批,分别来自美敦力、爱德华、沛嘉医疗、心通医疗、启明医疗、杰成医疗(2022年2月被健适医疗收购)。
全球TAVR市场高度集中,国际巨头美敦力、爱德华、波士顿科学占据超90%的份额,目前国内TAVR市场规模较小,渗透率仍然较低,主要由于产品价格高昂、手术操作难度高等。
公开数据显示,我国具有独立开展TAVR能力的中心仅10余家,2021年TAVR手术量为6500多例,相较于我国庞大的患病人群,手术渗透率较国外有一定差距。
此外,TAVR手术费用高昂也是阻止其放量的关键因素,据悉,单件的国产经导管主动脉置换系统终端价为20万~26万元,其中启明医疗VenusA-Valve的单价约为24.8万元,心通医疗VitaFlow单价为19.6万元,杰成医疗J-Valve单价26万元。
值得关注的是,价格高昂问题有望通过纳入医保逐步得到解决,2022年上海医保局发布《关于部分医用耗材试行按绩效支付的通知》,提出对心脏瓣膜(折叠)耗材按绩效支付,选取TAVR手术后即刻成功率或围手术期严重并发症发生率为评价指标,对达到指标要求的TAVR 耗材按医保基金平均支付水平(80%)纳入医保支付范围。
随着TAVR纳入医保进程逐步推进,国民可支配收入提高,将会带动国内的TAVR市场放量。
二尖瓣、三尖瓣领域
获批数少空间广阔
目前已上市的置换瓣膜产品,主要是经导管主动脉置换瓣。但实际上,在瓣膜性心脏病中,二尖瓣以及三尖瓣患者占比更高。《中国心血管健康与疾病报告2019》显示,主动脉狭窄、二尖瓣反流及三尖瓣反流患者分别占心脏瓣膜疾病患者的11.8%、29.2%和25.1%。
经导管二尖瓣治疗产品主要分为经导管二尖瓣修复术(TMVr)、经导管二尖瓣置换术(TMVR)。修复术具有较好的可行性及安全性,但受限于解剖结构不佳,如二尖瓣小叶明显增厚、钙化、二尖瓣后叶短等,置换术有望解决这一问题。
截至2021年年底,全球范围内仅有1件经导管二尖瓣置换系统上市,仅7件经导管二尖瓣修复系统获批,正在成为国内企业布局的重点。
据医械数据云统计,我国截至今年7月底有8件二尖瓣治疗产品进入创新审批通道,其中,德晋医疗、纽脉医疗各2件,捍宇医疗、申淇医疗、迈迪顶峰医疗、雅培各1件。
截至2021年底,三尖瓣领域仅有3件修复类产品在欧洲获批上市,分别来自爱德华以及雅培,其中爱德华独揽2件,最早获批产品为爱德华的Cardioband,于2018年4月在欧洲获批上市。目前我国尚无产品获批,但已进入临床试验阶段的产品有美敦力的Intrepid、爱德华的Evoque以及健世科技的LuX-Valve,健世科技的产品于2019年进入创新审批通道,2021年11月获得FDA突破性器械认定,预计可在2023年实现商业化。
在国内,瓣膜治疗不管从机构发展还是产品研发来看,仍处于初级阶段,随着我国老龄化趋势加重,市场空间值得期待,更重要的是,跨国械企还没多少“戏份”,国产瓣膜前景广阔。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






