血癌细胞疗法迭代出赢家
发布时间:2022-08-08 13:52:22作者:李勇来源:医药经济报
细胞疗法是目前研究最多的血癌治疗产品类型之一,据数据和分析公司GlobalData分析,到2028年,全球肿瘤细胞治疗市场预计将超过370亿美元。不过,如果持续大量的细胞疗法管线获得监管部门的批准上市,血癌市场将无法容纳过度饱和的产品。
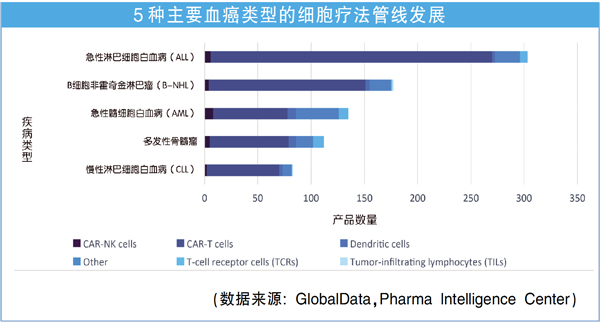
血癌研发管线拥挤
GlobalData发布的数据显示,目前正在开发中的仅针对5种主要血癌的极具潜力细胞疗法产品就超过800种。5种血癌分别为急性淋巴细胞白血病(ALL)、B细胞非霍奇金淋巴瘤(B-NHL)、急性髓细胞白血病(AML)、多发性骨髓瘤和慢性淋巴细胞白血病(CLL)。
市场过度饱和在ALL适应症尤为明显,该适应症有300多种细胞疗法项目在研,还有2种药物已经获得FDA批准。
诺华的嵌合抗原受体T细胞(CAR-T)疗法Kymriah(tisagenlecleucel)早于2017年8月就在美国获得了ALL适应症的批准。随后,吉利德科学同类产品Tecartus(brexucabtagene Autoleucel)在当年10月也获得了FDA对ALL适应症批准。
GlobalData的肿瘤学和血液学管理分析师Sakis Paliouras博士评论说:“细胞疗法在肿瘤学市场上取得了一些巨大的成功,吉利德的Yescarta和诺华的Kymriah为其他开发商CAR-T细胞疗法铺平了道路。这一成功也带来了丰富的同类产品开发。肿瘤学与心脏病学或免疫学等其他治疗领域不同,在这些领域,大量具有相似属性的产品商业化是常态。如果所有正在开发的血癌药物都获得FDA的批准,竞争将过于激烈。”
尽管B-NHL的市场规模至少是ALL的5倍,但B-NHL的细胞疗法管线规模较小。这意味着,ALL这种罕见性疾病的管线异常拥挤。不幸的是,由于战略决策,ALL管线中的大多数CAR-T细胞产品将永远不会进入市场。Me-too(后续药物)和后期上市细胞疗法也将面临市场表现不佳的高风险。
细胞疗法面临挑战
尽管同种异体技术具有显著优势,但大约80%的管线是自体细胞疗法,因为同种异体细胞在临床上仍未得到大规模验证。
与此同时,平衡需求与制造能力已被证明是商业CAR-T细胞疗法参与者面临的一大挑战。去年夏天,对于新推出的多发性骨髓瘤CAR-T细胞疗法Abecma(idecabtagene vicleucel)的需求超过生产能力,百时美施贵宝将其归咎于需要预留制造位置以进行每位患者的个性化治疗,以及整个行业的病毒载体短缺。
另一个即将出现的细胞疗法陷阱是定价和获得问题。随着越来越多公司的细胞和基因疗法面临FDA的“批准障碍”,该领域可能遭遇成本上升的挑战。与此同时,在极其罕见的情况下,付款人可能倾向于寻找支付下一代细胞疗法。对于更普遍的疾病,覆盖面谈判可能带来全新挑战,并为政府审查和价格控制打开大门。
细胞治疗领域在过去五年取得了长足进步,但更新技术才能使其全面开花。GlobalData采访的主要意见领袖认为,通过解决当前细胞疗法的几个挑战,该技术的下一次迭代将成为最成功的新技术。
改变规则再次飞跃
作为第一代CAR-T细胞疗法领航者,诺华等公司已经在癌症领域取得了相应的成功。接下来,该领域的领头羊有何举措,成为业界关注的焦点。
虽然百时美施贵宝、吉利德的KitePharma和诺华等公司获得批准的CAR-T细胞疗法在疗效方面取得了成功,但该类产品的制造仍是一个漫长而复杂的过程,进而阻碍了其更广泛的可及性。
不过,诺华新一代平台T-Charge有望彻底改变CAR-T细胞疗法,新产品可能为患者提供更好和更持久的反应,并具有最终治愈的潜力。
CAR-T细胞疗法是从患者的血液中取出T细胞,在实验室中对其进行体外基因工程改造,以添加嵌合抗原受体或CAR的基因,然后再将其回送给患者。借助T-Charge平台,CAR-T细胞扩增主要发生在患者体内,无需体外延长培养时间。与传统的CAR-T相比,T-Charge平台只需不到2天就能完成CAR-T细胞的生产。
此外,T-Charge保留了T细胞干性(自我更新和成熟的能力),从而使产品具有更大的增殖潜力以更少损耗T细胞。T-Charge平台的这些独特性可能改善患者预后,减少严重不良事件的风险。
诺华正在试验两种由该平台生产的CAR-T细胞疗法。近日发布的Ⅰ期临床试验阶段数据显示,其中一项被称为YTB323的项目在26名复发/难治性弥漫性大B细胞淋巴瘤(DLBCL)患者中,3个月后产生了63%的完全缓解率,将进入Ⅱ期研究。
诺华表示,8名患者在输注药物后8~16个月继续表现出反应率,并且尚未达到中位反应持续时间。
同时,对另一项目PHE885的Ⅰ期研究的后续分析显示,在可评估疗效的23名复发/难治性多发性骨髓瘤患者中,总体反应率为96%。临床反应迅速发生并随着时间的推移而加深。据诺华称,在数据截止时,有15名患者表现出持续反应。
除了YTB323和PHE885之外,诺华还拥有多种临床前项目,这些项目有可能利用该平台获得更多适应症。T-Charge平台提供了将其CAR-T产品组合扩展到CD19(已获批准的CAR-T疗法中使用最广泛的靶点)之外的机会。
诺华也将探索血液系统恶性肿瘤的新疗法,以及CAR-T和其他免疫疗法和传统抗癌疗法的组合。
诺华宣称将“在CAR-T细胞疗法的发展和重构癌症生存方面实现下一个飞跃”,估计在使竞争对手感到巨大压力的同时,也会吸引潜在的生物技术合作伙伴加入。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






