FDA药品审批是否收紧?
发布时间:2021-11-22 14:57:29作者:综合编译/王迪来源:医药经济报
进入10月下旬,美国FDA的监管行动开始提速,其在一周内发出了3封完整回复函(CRL),并推迟了两个药物的审批。这些动作引起了美国制药行业的关注,FDA是否正在偏离许多人所认为的宽松阶段?
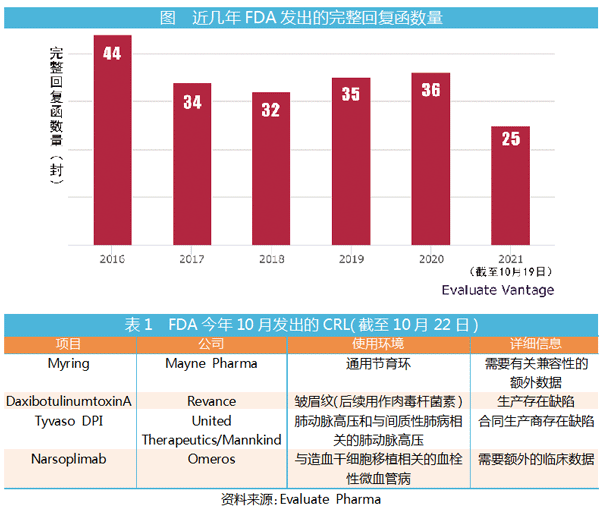
不过,根据Evaluate Vantage的统计数据,算上最新发出的CRL,今年以来FDA发出的CRL总数达到25封,这意味着,2021年的CRL数量应该不会多于往年。这或许会让那些正致力于将新药推向市场的制药企业松一口气,不过,因为新冠疫情而导致有关工作的延迟仍然是一个现实问题。
例如,优时比(UCB)公司称,FDA未能在10月15日《处方药申报者付费法案》(PDUFA)规定日期之前完成对其中度至重度斑块状银屑病治疗药物bimekizumab的上市申请的审批,新冠疫情是一大原因。FDA表示,由于出差限制,其无法开展现场检查工作。事实上,这种情况并不是第一次发生。
FDA已经发布了疫情大流行期间开展审查工作的相关指南,其指出,在没有发现任何缺陷,并且新药申请也满足批准要求的前提下,如果因疫情影响阻碍了现场检查工作,那就会推迟审批。如果不满足这些条件,则会发出CRL。以此来看,bimekizumab最终获批希望很大。
当然,疫情并非是造成药品审批延迟的唯一原因。考虑到投资者并不总能完全清楚相关情况,因此,制药公司有责任披露审批被延迟的原因。例如,Avadel Pharmaceuticals公司称,旗下发作性睡病项目FT281,FDA没有给出任何延迟的理由。不过,就目前来说,其并未收到CRL,这可能是一个积极因素。
Evaluate Vantage的上述数据是基于其每月跟踪FDA的批准情况,以及Evaluate Pharma的大事纪要(可以回顾性地梳理那些已经被披露的CRL)而构建起来的。不过,由于药企并不总会及时公布相关情况,因此上述CRL数值也有可能被低估了。
此外,要判断FDA对药品审批是否收紧,如果只看CRL的数据可能存在一定的局限性,还需要参考其它数据,比如,每年新药申请的数量,以及发出CRL后与相应药物最终获批所经历的时长等。不过,单看CRL的情况,至少可以判断其并未出现显著增加的趋势。
与此同时,FDA释放的信号也差异颇大,这让生物制药行业和投资者难做预判。例如,渤健的Aduhelm尽管疗效指标非常微弱,但仍然获得FDA批准;而FDA拒绝Fibrogen公司开发的roxadustat是基于安全考虑,但该药在中日欧已经获批。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






