支付承压VS投资回报? 聚焦孤儿药政策六道思考题
发布时间:2021-11-05 17:12:52作者:胡善联 复旦大学公共卫生学院教授来源:医药经济报
孤儿药的政策制定是个全球性的难题:既要确保支付方对孤儿药费用的可承受性,还要确保生产孤儿药的企业有足够的投资回报,如何提高罕见病患者的药物可及性?
一方面,结合我国国情,不断探索我国罕见病保障的经验,如建立和健全全国罕见病登记报告制度、实行罕见病目录病种管理、探索罕见病立法制度、探索政府主导下的各种多元筹资方式;鼓励地方积极探索专项基金方式,通过总结地方经验,出台全国性罕见病医疗保障政策。另一方面,吸取国际孤儿药政策的经验同样十分重要。
本文针对孤儿药的6个重点问题,探讨孤儿药政策的现状、问题与解决方向。
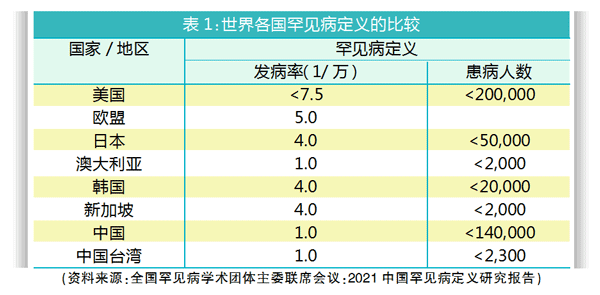
[焦点1] 各国罕见病、孤儿药定义有何不同?
任何针对罕见病(rare diseases)的药物,或针对没有满意的诊断、预防或治疗方法的疾病的治疗药物,均可称为孤儿药(orphan drugs)。罕见病是指只有有限手段治疗的疾病,只影响很小一部分患者,平均患病率在4~5/10,000以下。事实上,世界各国对罕见病的定义各不相同,详见表1。
目前,罕见病总数有7000多种,影响全球3亿人口,半数为儿童,30%死于5岁以内,也可被称为“有显著意义的少数”(significant minorities)。大部分罕见病患者不能获得及时治疗,全球只有1/10的罕见病患者可以有特殊的治疗药物和方法。
[焦点2] 政策框架?主要内容?
孤儿药政策的框架是寻找最优化的药品、研发、许可、定价和报销补偿的过程。
1983年美国颁布孤儿药法案以来,通过财政和法规的支持和鼓励,1983-2009年间已有400多个孤儿药、420个以上的适应症被批准。10个销售量最大的药品中7个是孤儿药。此外,欧盟、新加坡、日本、澳大利亚、韩国和中国台湾地区也在发展孤儿药政策。
孤儿药政策中,提高罕见病患者的药物可及性是重要内容。其次,需要改进药品政策,包括价格规制、激励市场可及性、鼓励孤儿药的研究与开发。另外,要确保支付方对孤儿药费用的可承受性,还要确保生产孤儿药的企业有足够的投资回报。
孤儿药政策的内涵分析包括销售许可、安全性和疗效的要求、价格如何规制、激励和鼓励市场可及性、激励和鼓励研发等方面。
[焦点3] 药物经济学研究特征?问题?如何解决?
孤儿药的临床试验往往是单臂试验、开放式的研究设计。样本量少,而且长期的结果评价资料不足,在真实世界中临床治疗效果和安全性不够确定,这些都是问题。
未来,需要建立罕见病的登记系统,收集可靠的纵向资料,运用大数据挖掘方法,对孤儿药进行上市后的效果和安全性评价。同时,发挥社会媒体的药物警戒作用。
由于孤儿药在申报时往往采用临床结果的替代指标,患者人数少,提供评审的证据质量差,所以需要上市后进一步观察。
Sirrs(2021年)报道,加拿大对治疗法布雷病药品上市后的国家独立的登记报告制度(CFDI),要比由药企资助的登记报告制度(IFR)质量更好:制度运行费用低、患者乐于参与登记、数据收集质量高、费用资料登记较全。这证实国家独立的罕见病登记制度是一种具有成本-效果的有效工具,适合于孤儿药的上市后监测(postauthorization surveillance,PAS)。
[焦点4] 孤儿药市场失灵有哪些表现?
孤儿药的市场失灵表现在其垄断独占性(monopolization),缺少仿制药或生物类似物的竞争,需要花费高成本的陡峭式研究(steep research)。另外,由于人们对罕见病知识信息的不对称性(asymmetrical knowledge),罕见病患者往往缺乏及时治疗,导致对生命的威胁,患者的需求缺乏弹性(inelasticity)。而且,孤儿药的国际参考价格在高收入和低收入国家中类似。
[焦点5] 市场独占权可以取消?有何条件?
孤儿药品具有市场独家经营权。各国对孤儿药品的市场独家经营权也不尽相同。比如,欧盟、日本、中国台湾孤儿药的市场独家经营权均为10年;加拿大为8年(儿童孤儿药为8.5年);美国为7年;澳大利亚为5年。
值得一提的是取消孤儿药资格的规定。取消少数孤儿药的市场独立经营权资格,可增加市场竞争力,极大地节约医疗费用,并激励孤儿药研发。
美国设定了否认孤儿药独占权的阈值:当孤儿药适应症治疗的目标人群超过20万时,根据患病率的阈值可取消授予市场独立经营权的资格。另外,一旦药品获得非孤儿药品证实,市场独立经营权的资格也会取消。
Socal等人报道,美国FDA孤儿药数据库从1983年到2017年共批准孤儿药453个,其中21%的孤儿药用于2种或以上罕见病,31%为生物制剂,近半数(49%)为治疗肿瘤的药物。30余年来,有33%的孤儿药因治疗人数超过20万人而最终被取消孤儿药资格,38%的孤儿药因审批为非孤儿药而被取消孤儿药资格。
[焦点6] 价格谈判,“他山之石”有何借鉴之处?
为确保孤儿药的可利用性和价格的可承受性,孤儿药的价格谈判在高收入国家中是常用的一种策略,以期在价格与数量之间取得平衡。
比如,德国依赖于强制性价格谈判机制,对孤儿药进行成本效益分析,但这种政府与企业的谈判往往被批评为“黑箱操作”,忽视患者的参与和程序透明化。比利时孤儿药上市申请,在临床结果和医保预算补偿不确定时,医保支付方可与药品上市许可人进行药品管理合同谈判;孤儿药价格可根据疗效、安全性和适应症进行价格调整,类似于非罕见病药物。荷兰则实行有条件性补偿,每4年需要对孤儿药再评估一次。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






