再生医学全方位突破
发布时间:2021-08-30 15:47:18作者:益安来源:医药经济报
近年来,以基因和细胞疗法为主的再生医学正在以极快的速度向前迈进。美国再生医学联盟(ARM)近期发布的2021年上半年报告显示,2021年以来,再生医学领域已经取得多项突破。
突破1 再破纪录!2021上半年融资金额141亿美元
2021年上半年,再生医学和先进疗法筹集资金141亿美元,比2020年上半年增长了35%,融资金额飙升至新的高度,已经是2020年全年筹集资金的71%。2021年全年融资金额有望超越2020年。尽管面临新冠病毒大流行的挑战,该行业去年仍以近200亿美元的融资金额打破了融资记录。
基于细胞的免疫肿瘤学(IO)融资首次超过基因疗法,在2021年上半年筹集了66亿美元。基因疗法开发者筹集了64亿美元,细胞疗法开发者筹集了11亿美元。
随着再生医学的发展,针对内外部制造能力的需求不断增长。较小的细胞和基因治疗合同开发和制造组织(CDMO)是有吸引力的收购目标,推动今年上半年宣布的合并和收购金额超过108亿美元。其中,包括丹纳赫以96亿美元收购质粒、mRNA和蛋白质制造商Aldevron,以及Charles River Laboratories分别以8.75亿美元和2.93亿美元收购CDMO公司Cognate BioServices和Vigene Biosciences。也有公司在建设内部产能并投资新的制造设施,例如BioNTech最近从Kite Pharma收购了细胞治疗设施。
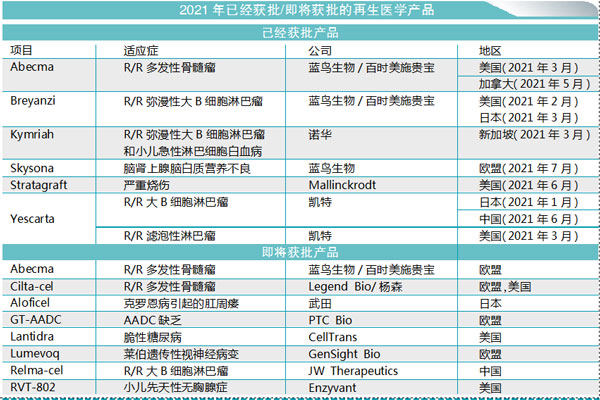
突破2 创新高!18种产品等待批准
2021年有望迎来“全球新”再生医学和先进疗法获批的“分水岭”。预计6个地区的监管机构将针对18种再生医学产品作出批准决定,其中10种是之前从未获批的产品,这意味着新产品批准可能超过2016年创下的记录(9种)。
其中4种已经获得批准:百时美施贵宝的Breyanzi、蓝鸟生物/百时美施贵宝的Abecma以及Mallinckrodt的Stratagraft均获得FDA批准,蓝鸟生物的Skysona在欧洲获得批准。其中3种产品——Breyanzi、Abecma和Skysona是基因疗法/基因修饰细胞疗法,这意味着2021年可能成为此类产品新批准的创纪录年份。
预计今年将对另外4种基因治疗/基因修饰细胞治疗产品作出决定,可能获得7项批准——将是2017年之前记录(3项)的两倍多。截至发稿时,2021年迄今已有两种产品是通过再生医学先进疗法资格(RMAT)获得首批上市的:1.Breyanzi,用于复发或难治性大B细胞淋巴瘤的CAR-T疗法;2.Stratagraft,用于严重烧伤的再生皮肤组织疗法。此外,用于治疗多发性骨髓瘤的Abecma是首个获批的BCMA靶向CAR-T疗法。复星凯特的Yescarta成为第一个在中国获批的CAR-T疗法。
突破3 2600多项临床试验进行中
目前,全球有1320项行业赞助的再生医学和先进疗法试验正在进行中。自2020年底以来增加了100项,亚太地区是主要增长中心。另外还有由包括学术中心和政府非行业团体赞助的1328项试验正在进行。与行业赞助的试验相比,非行业团体赞助的试验Ⅲ期比例较低(6%对12%),细胞治疗试验的比例较高(59%对39%),基因治疗试验的比例较低(6%对22%)。
Ⅲ期阶段试验有243项,包括158项由行业赞助的试验和85项由学术、政府和其他机构赞助的试验。这些晚期候选产品正对多种适应症,包括糖尿病神经病变、心力衰竭、罕见遗传疾病和肌萎缩侧索硬化症(ALS)等神经肌肉疾病进行测试。
尽管自2020年底以来行业赞助的临床试验数量略有减少,但预计未来几年将显著增长。目前有956种独特疗法正在开发中,其中136种处于Ⅲ期阶段。预测到2026年,这一数字将增长至3100多种,其中355种将进入Ⅲ期阶段。
CAR-T领域持续推进。除了Abecma,越来越多的BCMA靶向CAR-T疗法将公布数据。强生和Legend Biotech于6月公布了BCMA靶向CAR-T疗法cilta-cel的数据,显示多发性骨髓瘤的总体缓解率为98%,严格的完全缓解率为80%,而EMA和FDA预计今年晚些时候对cilta-cel作出批准决定。Precision BioSciences和CRISPR Therapeutics各自开发的BCMA靶向CAR-T疗法的试验数据也有望在今年晚些时候公布。
基因编辑也不断取得进展。近期,Intellia Therapeutics宣布了一项有希望的转甲状腺素蛋白(ATTR)淀粉样变性试验的临床数据:NTLA-2001将转甲状腺素蛋白(一种有害肝脏蛋白质)的血清水平降低了87%,优于通常达到80%的标准疗法。从CRISPR Therapeutics和Vertex Pharmaceuticals得到的关于镰状细胞病基因编辑疗法的数据:所有15名接受治疗的β地中海贫血患者均不依赖输血,所有7名镰状细胞病患者均未出现血管闭塞危象。在CRISPR领域之外,Homology Medicines报告数据显示,在使用其同源重组基因编辑技术治疗甲基丙二酸血症的试验中对第一位患者给药,该试验是首次在儿科患者中进行的体内基因编辑试验。
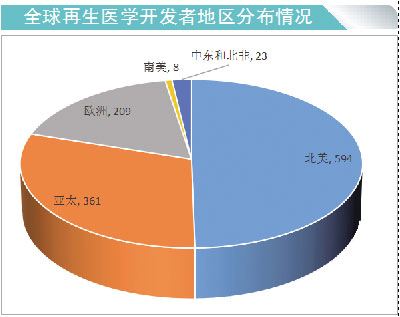
突破4 开发者数量增119%!亚太地区超欧追美
作为再生医学曾经的领航者之一,欧洲面临落后的风险,过去三年中无论开发者数量还是新临床试验数量都远远落后于美国和亚洲。
全球有近1200家公司积极参与再生医学和先进疗法开发,比去年同期增加了近200家。自2018年以来,欧洲的再生医学和先进疗法开发者数量减少了4%,而美国增加了23%,亚太地区增加了119%。
从2018年到2021年上半年,欧洲启动了224项由行业赞助的再生医学试验,而美国(597项)和亚太地区(473项)启动的数量是这一数字的两倍多。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






