复杂注射剂开发抢夺战 国内企业介入几许?
发布时间:2021-07-12 15:43:14作者:本报特约撰稿 李勇来源:医药经济报
复杂注射剂开发由于具有较高的技术难度,转化效率和临床成功率较低,成为国内外创新药和仿制药开发的主要技术壁垒之一。
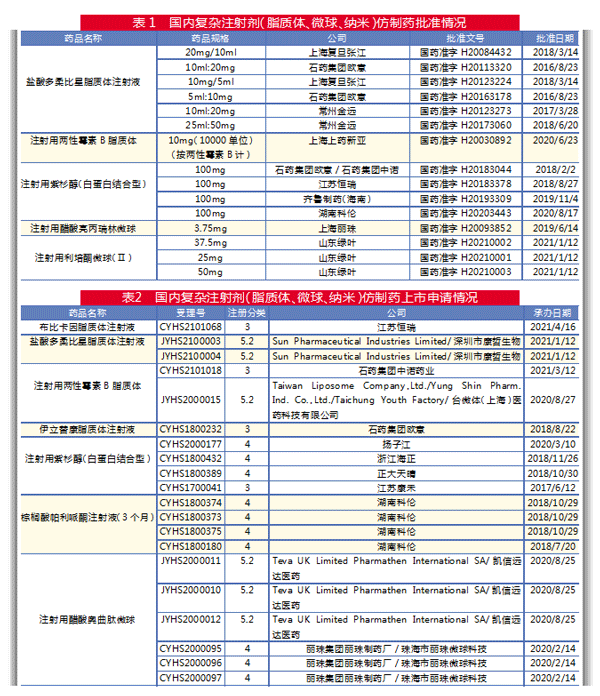
据笔者初步统计,FDA已批准至少35种脂质体、微球、纳米复杂注射制剂,目前已有多款产品进入中国,而且已有仿制药获批上市。在国内,复杂注射剂正成为具有更高药物开发技术水平制药公司的争夺场。
脂质体注射剂
脂质体是一种人工膜,主要由天然或合成的磷脂(如DLPC、DMPC、DPPC等)制备。药物装入囊泡中,随着脂质体的逐渐降解而缓慢释放。
国外多款产品已上市
1995年,FDA批准首款脂质体注射剂药物Doxil(盐酸多柔比星脂质体注射液),用于治疗卵巢癌、艾滋病相关的卡波西肉瘤和多发性骨髓瘤。与游离多柔比星相比,Doxil中的盐酸多柔比星脂质体由于长循环半衰期(45小时)和被动靶向性,显示出更强的疗效和更低的心脏毒性。此外,Doxil还能通过肿瘤部位增强的通透性和保留(EPR)作用靶向肿瘤。
Doxil(欧盟上市商品名为Caelyx)在2001年达到年销售额峰值6亿美元,取得了巨大的商业成功,从而吸引了更多制药公司进入脂质体领域。
Ambisome(注射用两性霉素B脂质体)1997年获批用于治疗深部真菌感染,Depodur(硫酸吗啡脂质体注射液,2004)和Exparel(布比卡因脂质体注射液,2011)作为麻醉剂进入市场。Daunoxome(枸橼酸柔红霉素脂质体注射液,1996,已撤市)、Depocyt(注射用阿糖胞苷脂质体,1999)、Margibo kite(硫酸长春新碱脂质体注射液,2012)、Onivydeo(伊立替康脂质体注射液,2015)和Vyxeos(注射用柔红霉素阿糖胞苷脂质体,2017)获批用于癌症治疗。
国内紧紧跟上
而在国内,盐酸多柔比星脂质体注射液原研品种曾经进口中国(商品名为楷莱/Caelyx),2015年注册证号到期后未进行再注册。原研品种伊立替康脂质体注射液、注射用两性霉素B脂质体进口上市申请分别于2020年6月和2020年10月获CDE受理。
目前,石药集团欧意药业、常州金远药业、上海复旦张江生物3家药企获得盐酸多柔比星脂质体注射液仿制药的6个批准文号。今年5月,石药集团欧意药业的产品(10ml:20mg规格)已获NMPA批准通过仿制药质量和疗效一致性评价,为国内该品种首个通过一致性评价。值得一提的是,印度太阳制药/深圳市康哲生物该品种仿制药进口上市申请今年1月获CDE受理,而太阳制药开发的盐酸多柔比星脂质体注射液仿制药2013年获得FDA批准。
上海上药新亚药业1家药企获得了注射用两性霉素B脂质体仿制药的批准文号,石药集团中诺药业该品种仿制药上市申请今年3月获CDE受理。
恒瑞医药的布比卡因脂质体注射液仿制药上市申请今年4月获CDE受理。石药集团欧意药业的伊立替康脂质体注射液上市申请2018年获CDE受理。
其他几款产品——硫酸吗啡脂质体注射液、硫酸长春新碱脂质体注射液、注射用柔红霉素阿糖胞苷脂质体,目前原研暂未在国内上市或申请注册,亦无国内企业获得仿制药批文或提交仿制药注册申请。
微球注射剂
微球是小的球形微粒,直径通常为1微米至300微米。开发缓释注射微球的关键是如何选择合适的生物可降解聚合物。目前市场上销售的产品主要使用合成聚合物,例如PLGA和PLA都是可生物降解且具有生物相容性的合成聚合物。
十余种缓释微球获FDA批准
美国批准上市的第一款缓释微球Lupron depot(注射用醋酸亮丙瑞林微球)由武田公司开发(与艾伯维合作)。Lupron depot含有促性腺激素释放激素(GnRH)激动剂,用于晚期前列腺癌的姑息治疗。
目前,已有十多种缓释微球注射剂获FDA批准上市。例如,Sandostatir Lar(注射用醋酸奥曲肽微球)解决了肽类药物的短生物半衰期,将给药期延长至4周并改善了患者的依从性。Risperdal Consta(注射用利培酮微球)解决了精神疾病患者的药物治疗困难和药物滥用问题。
多个原研品种已进口中国
在国内,注射用醋酸亮丙瑞林微球原研品种已经进口中国。上海丽珠制药获得了注射用醋酸亮丙瑞林微球仿制药的批准文号。
注射用醋酸奥曲肽微球原研品种已经进口中国。梯瓦/凯信远达、丽珠集团的注射用醋酸奥曲肽微球仿制药上市申请于去年2月和8月分别获CDE受理。
注射用利培酮微球原研品种已经进口中国。今年1月,绿叶制药开发的注射用利培酮微球(Ⅱ)(瑞欣妥)已获NMPA批准上市,是该公司第一个由长效缓释平台开发的获批上市创新制剂。
此外,注射用艾塞那肽微球、注射用双羟萘酸曲普瑞林、注射用六氟化硫微泡原研品种都已经进口中国。
纳米注射剂
纳米粒子是一种至少具有小于100nm的微观粒子。上世纪90年代以来,纳米粒子药物传递系统引发关注。
美国已有十余产品上市
紫杉醇的白蛋白结合纳米粒子制剂Abraxane(注射用紫杉醇(白蛋白结合型))在治疗复发性乳腺癌方面取得了巨大的商业成功。Abraxane比纯紫杉醇具有明显优势。此外,Abraxane不包含磷脂,可以避免脂质体的溶血反应。
如今,美国已有十余种纳米颗粒注射产品获批上市。在这些产品中,几种具有新技术的药物引起了广泛关注。具有纳米晶体技术的Invega Trinza(棕榈帕利哌酮酯注射液(3M))会在很长一段时间内缓慢释放,带有Atrigel技术的原位凝胶成型系统的Sublocade(盐酸多西环素牙龈下控释给药系统)被认为是划时代的产品。
国内企业纷纷加入
在国内,注射用紫杉醇(白蛋白结合型)、棕榈酸帕利哌酮注射液、棕榈帕利哌酮酯注射液(3M)原研品种已经进口中国。阿立哌唑长效肌肉注射剂原研进口上市申请于今年3月获CDE受理。
目前,石药集团、恒瑞、齐鲁和湖南科伦4家药企获得了注射用紫杉醇(白蛋白结合型)仿制药的批准文号,且被纳入中国药品目录集。此外,扬子江药业等3家企业提交了本品的仿制药上市申请。
★★★ 结语 ★★★
在FDA批准的35种复杂注射剂(脂质体、微球、纳米)中,目前国内仅有5种有仿制药获批上市。随着国内相关企业技术积累和更多制药公司进入该领域,复杂注射剂的开发种类将日益增加。不容忽视的是,越来越多的国外仿制药公司开发的复杂注射剂产品也在加速进军中国市场。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






