Aduhelm获批 同类项目复活几率多大
发布时间:2021-06-16 11:59:59作者:李勇来源:医药经济报
6月7日,FDA加速批准渤健的β淀粉样蛋白单克隆抗体Aduhelm(aducanumab)用于治疗阿尔茨海默病,那么,该领域的其他几个项目有复活希望吗?
哪些项目复活欲最强?
美国FDA引用了Aduhelm减少大脑中β淀粉样蛋白斑块的证据,证明其加速批准渤健Aduhelm的合理性。此举尽管引发业界哗然,但其他几家曾有失败的β淀粉样蛋白单克隆抗体的公司也跃跃欲试,或许也想让其同类项目“复活”。
辉瑞/强生公司是否应该复活其合作开发的bapineuzumab呢?该项目于2012年在几项Ⅲ期临床试验研究失败后已经被放弃。数据显示,bapineuzumab确实显示出对大脑β淀粉样蛋白有影响。在一项大型试验中,与安慰剂相比,bapineuzumab达到了名义上的统计显著性。
另一项试验也显示出bapineuzumab与安慰剂相比的数值差异(p=0.159)。根据《新英格兰医学杂志》发表的结果,其余两项Ⅲ期临床试验显示,尽管bapineuzumab没有改善患者症状,但与安慰剂相比,该药血浆β淀粉样蛋白显著增加,这表明有些β淀粉样蛋白从大脑中被清除。
礼来的solanezumab在12~80周可促使血浆β淀粉样蛋白升高。Expedition和Expedition-2试验显示,与安慰剂相比,在减少脑脊液中的β淀粉样蛋白方面具有统计学显著性。然而,Expedition-3对原有的β淀粉样蛋白斑块没有影响。
与其让solanezumab复活,礼来还不如专注于donanemab的开发,后者已经对β淀粉样蛋白显示出显著效果。然而,目前仅为一项规模相对较小的研究,该公司已经启动了Ⅲ期临床试验计划。
“回头看”不如“向前看”
重新复活曾经失败的同类项目应该考虑到:任何追随Aduhelm脚步的项目都不会真正具有新颖性,这与新药开发的目标背道而驰,可能无法获得FDA的监管批准支持。
尽管如此,许多靶向于β淀粉样蛋白的项目确实达到了Aduhelm获批时的标准。只有罗氏的crenezumab似乎缺乏具有清除脑内β淀粉样蛋白活性的证据,但这可能是因为其Cread和Cread-2研究在2019年就被仓促取消而缺乏试验数据。
罗氏的gantenerumab也已被证明可以降低β淀粉样蛋白,不过是在高剂量的开放标签试验中达到的,而不是在其最初的Ⅲ期临床试验中。需要警惕的是,测量β淀粉样蛋白这种生物标志物的不同方法很难与Aduhelm标签上声称的效果直接比较。
如今,在阿尔茨海默病领域,目前业界将目光转向solanezumab针对记忆丧失患者的A4研究,以及卫材/渤健的lecanemab一项治疗早期阿尔茨海默病的Clarity AD试验研究。两者都可能在明年结束。
“复活”或许没有动力
复活曾经失败的β淀粉样蛋白同类项目看起来似乎可行并被提起,可能与阿尔茨海默病领域新药研发高失败率和巨额资金投入有关。据《华尔街日报》,阿尔茨海默病向来被称为新药研发的“黑洞”。此前有报告显示,阿尔茨海默病新药研发失败率高达99.6%。目前FDA仅批准过6种阿尔茨海默病治疗药物,渤健的Aduhelm获批也是一波三折,多次面临失败风险。
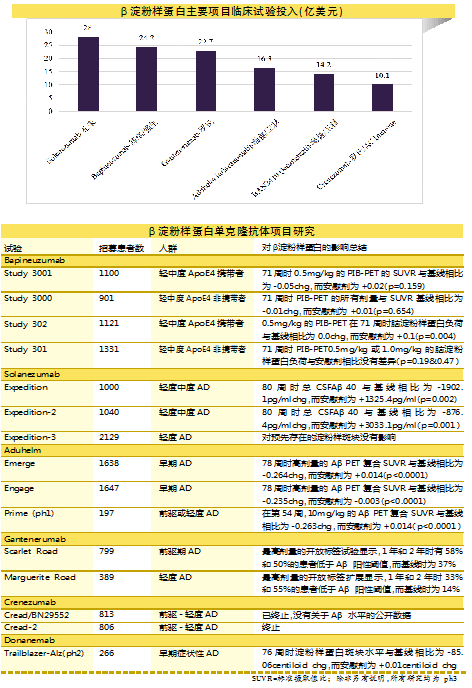
伴随高失败率,阿尔茨海默病新药开发是最费钱的投入领域。据医药市场调研机构Evaluate估计,aducanumab临床试验耗资16.3亿美元,而其总研发投入可能要高得多。而其他几项进入临床中晚期的β淀粉样蛋白项目投入也都在十亿美元以上。礼来的solanezumab临床试验投入估计达到28亿美元。
此外,对于这些曾经失败的中晚期项目,专利保护也是开发者考虑的主要因素,例如bapineuzumab在美国关键的专利将于今年陆续到期。尽管重新推出这类药物的公司都将受益于数年的数据独占权,但看看Aduhelm每年56000美元的定价,缺乏正式的知识产权保护可能会大大缩短其在市场上高价销售的时间。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






