高端制剂迎收获期 还有哪些赛道?如何接力?
发布时间:2021-03-10 09:11:10作者:本报特约撰稿 镜陆来源:医药经济报
高端制剂已然开启收获期。以口溶膜为例,2020年11月24日,江苏豪森的奥氮平口溶膜(5mg/10mg)获批上市,为国内首个上市;紧接着,2021年1月19日,齐鲁制药的奥氮平口溶膜(5mg/10mg)获批上市。力品药业亦加入口溶膜领域竞争,2020年申报产品有阿立哌唑口溶膜、他达拉非口溶膜和盐酸多奈哌齐口溶膜。
集采常态化大背景下,高端制剂成为许多药企眼中的避风港。除了微球注射剂、脂质注射剂、胶束注射剂、口溶膜、吸入剂(详见本报2020年10月26日刊发的《五大高端制剂赛道PK》一文),业界关注的高端制剂还有缓/控释口服剂、泡腾片/口崩片、混悬滴眼液、透皮贴剂。在这些高端制剂领域,企业布局和竞争情况如何?哪些领域还能有所作为?
本文涉及的高端制剂包括改良药和仿制药。其中改良药主要针对的是2.2类,即含有已知活性成分的新剂型(包括新给药系统)、新处方工艺、新给药途径,且具有明显临床优势的药品。仅仅新增适应症的产品不被纳入分析。
缓释/控释口服剂
[热度] ★★★★★
[热点] 各种慢性病用药
[前排企业] 江苏恒瑞(改良药);宜昌人福(仿制药)
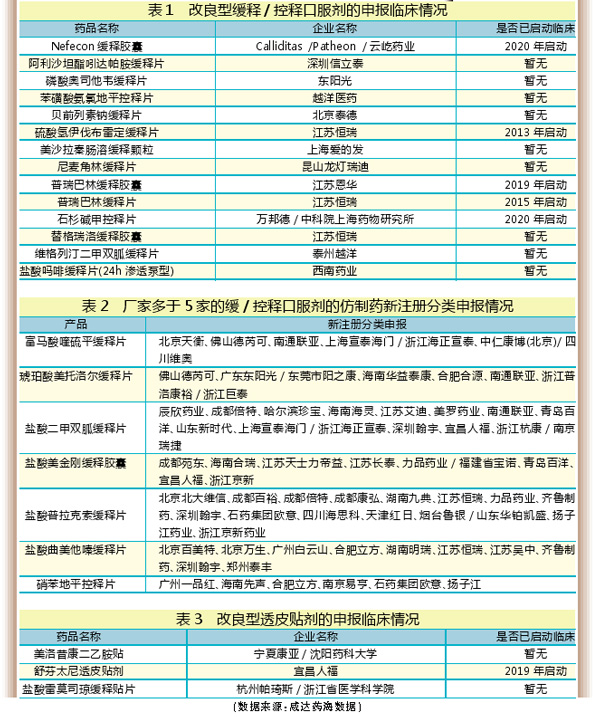
江苏恒瑞是改良型缓释口服剂申报临床产品最多的厂家,申报的产品包括硫酸氢伊伐布雷定缓释片、普瑞巴林缓释片和替格瑞洛缓释胶囊,也是缓释口服剂中已启动临床项目最多的厂家,硫酸氢伊伐布雷定缓释片和普瑞巴林缓释片都已启动临床。
而广州柏赛罗的格列齐特缓释胶囊的上市申请不予批准。2020年东阳光已经终止了磷酸奥司他韦缓释片的临床申报,但2021年又重新启动了此项目的临床申报。
普瑞巴林缓释胶囊和普瑞巴林缓释片都已启动临床,根据国内集中采购的合并剂型规则,缓释控释剂型合并剂型招标,缓释片、缓释包衣片、控释片、缓释胶囊、控释胶囊都会纳入同一组,预计上市后会和原研普瑞巴林控释片进入集中采购同一分组。
以新注册分类申报的缓释和控释产品仿制药对应的生产厂家多于5家的产品如表2所列。热点产品主要聚焦于慢性药市场。
宜昌人福药业是申报缓释仿制药最多的企业,申报产品包括琥珀酸去甲文拉法辛缓释片、氯化钾缓释片、盐酸安非他酮缓释片、盐酸安非他酮缓释片(Ⅱ)、盐酸二甲双胍缓释片、盐酸美金刚缓释胶囊、盐酸羟吗啡酮缓释片、盐酸氢吗啡酮缓释片和盐酸他喷他多缓释片。
上海宣泰紧跟其后,合作开发的产品包括盐酸安非他酮缓释片(Ⅰ)、盐酸安非他酮缓释片(Ⅱ)、盐酸帕罗西汀肠溶缓释片、盐酸普罗帕酮缓释胶囊、富马酸喹硫平缓释片、盐酸二甲双胍缓释片、普瑞巴林缓释片和西格列汀二甲双胍缓释片。
泡腾片/口崩片
[热度] ★★★
[热点] 奥氮平口崩片、阿立哌唑口崩片(仿制药)
2021年,青海制药厂申报了盐酸美沙酮泡腾片改良新药。口崩片改良新药方面,成都康弘药业申报了依匹哌唑口崩片,北京星昊申报了磷酸奥司他韦口崩片。
仿制药方面,2021年海南涛生/南京海纳申报了对乙酰氨基酚维生素C泡腾片,沈阳奥吉娜申报了对乙酰氨基酚泡腾片。2020年健乔信元/Synmosa进口引进乙酰半胱氨酸泡腾片。
口崩片仿制药最热的是奥氮平口崩片,共7家申报,分别是佛山德芮可、广东东阳光、哈尔滨三联、河北龙海、江苏豪森、齐鲁制药和浙江华海。
阿立哌唑口崩片也有4家申报,分别是广东东阳光/东莞市阳之康、齐鲁制药、扬子江南京海陵和浙江华海。
混悬滴眼液
[热度] ★
[特点] 改良药和仿制药项目均稀缺
新注册分类中,暂无混悬滴眼液改良新药申报。2016年兴齐药业曾申报了他克莫司混悬滴眼液,2017年获批临床,2020年8月才启动安全性和药代动力学特征的Ⅰ期临床试验。
新注册分类以混悬滴眼液申报的仿制药也没有,这主要是因为原研药没有以混悬滴眼液为名申报,例如布林佐胺滴眼液,而布林佐胺滴眼液暂无新注册仿制药申报,齐鲁药业是按旧注册分类申报的。
透皮贴剂
[热度] ★★
[热点] 镇痛药、消炎止痛药
[前排企业] 宜昌人福(改良药);湖南九典(仿制药)
按新注册分类申报的改良型透皮制剂启动的项目并不多,目前处在临床研究阶段的仅宜昌人福的舒芬太尼透皮贴剂。
透皮贴剂以新注册分类申报的仿制药只有3个产品:氟比洛芬凝胶贴膏、洛索洛芬钠凝胶贴膏和吲哚美辛凝胶贴膏,都是非甾体抗炎药。上述3个产品,湖南九典制药都有申报。
小结<<<
根据医保目录的凡例介绍,化学药品的医保剂型是合并剂型的。以旧注册分类获批的不同剂型,在集采时也是合并剂型处理。
根据2021年2月《国务院办公厅关于推动药品集中带量采购工作常态化制度化开展的意见》(国办发〔2021〕2号)所提到的,“按照合理差比价关系,将临床功效类似的同通用名药品同一给药途径的不同剂型、规格、包装及其采购量合并,促进竞争”。这意味着改良剂型产品有可能被集中带量采购列进同一分组。
2.2类新药通常指的是国内外未上市的改良药,获批上市需要“临床优势”,上市前需要投入较高的临床费用。但是,改良药获批后要和仿制药一起分组,若改良药和该活性成分的集采仿制药竞争没有价格优势,可能会在集中采购中丢标。这类同一给药途径的改良新药,经评估投入和回报后,非常有可能“不予立项”。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






