“十三五”医械标准制修订收官 超额完成12%
发布时间:2021-02-22 12:39:51作者:本报记者 胡睿 发自北京来源:医药经济报
提高医疗器械质量、制修订完成500项医疗器械标准……是2017年国务院印发《“十三五”国家药品安全规划》中明确的工作任务目标。近日,国家药监局网站发布的“中国医疗器械标准管理年报(2020年度)”(以下简称《年报》)显示,既定目标已经立项561个,超额完成12%,“十三五”医疗器械标准质量提升专项计划圆满收官。
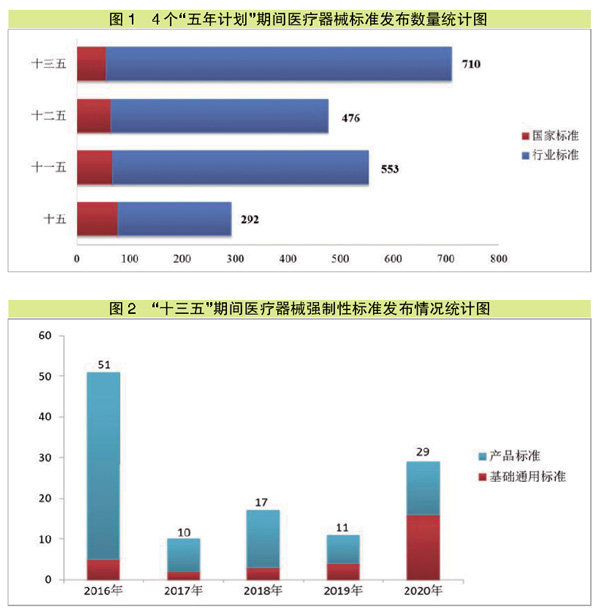
《年报》显示,“十五”“十一五”和“十二五”期间分别发布医疗器械标准292项、553项和476项。“十三五”期间,已发布医疗器械标准总数为710项,较“十二五”期间增长了49%,其中国家标准发布数量减少了15%,行业标准发布数量增长了59%。2020年共发布医疗器械标准149项,标准发布数量较上一年度增长了93%。
自2001年“十五”实施以来,医疗器械标准发布数量大幅提升(见图1)。从标准领域覆盖情况来看,截至2020年12月31日,按标准规范对象统计,现行有效的医疗器械标准按照《中国标准文献分类法》,主要归类在医疗器械综合(C30)至医用卫生用品(C48)之间,占比前5位的分别是:医用化验设备(C44)14%,一般与显微外科器械(C31)11%,矫形外科、骨科器械(C35)11%,口腔科器械、设备与材料(C33)10%,医用射线设备(C43)9%。医疗器械标准基本覆盖医用电气设备、手术器械、外科植入物等医疗器械各技术领域。
标准约束力更加优化
采访中,记者了解到,近年来国家药监局持续优化医疗器械强制性行业标准体系。去年7月,国家药监局印发《关于进一步加强医疗器械强制性行业标准管理有关事项的通知》(以下简称《通知》),明确了进一步维护医疗器械强制性行业标准的法律地位,以及进一步优化标准体系等具体要求。
截至2020年12月31日,现行有效的医疗器械强制性标准共397项,占比23%。其中强制性国家标准92项,行业标准305项。397项医疗器械强制性标准中基础通用标准106项(占27%)、方法标准2项(1%)、产品标准 289项(72%)。基础通用标准主要涉及产品通用安全和技术要求等方面;1项方法标准在2020年通过实施评价后拟整合修订为医疗器械推荐性行业标准。2016-2020年发布医疗器械强制性标准统计情况见图2。
另外,2020年4月,新版GB 9706.1-2020《医用电气设备 第1部分:基本安全和基本性能的通用要求》正式发布,是医用电气设备需要遵循的基础通用安全标准,新标准有三年过渡期,将于2023年5月实施。
相关负责人介绍,“该标准及其并列、专用标准均采用IEC 60601系列国际标准,其中适于转化的IEC 60601系列标准共74项。国家药品监督管理局组织制定了一揽子标准转化、编号、宣贯方案,有序推进系列标准转化。截至2020年12月31日,已发布15项标准,39项已完成制修订正在标准审核及出版社审校阶段,15项正在制修订中,需新转化制定的5项专用安全标准正在申请国家标准立项。”
超90%标准对接国际
医疗器械标准是医疗器械研制、生产、经营、使用以及监督管理所共同遵循的技术规范,是医疗器械监管和产业发展的重要技术支撑。上述负责人表示,“近年来国家药监局持续实施医疗器械标准提升计划,每年组织制修订100项左右医疗器械标准,对重大基础性标准、通用性标准、高风险产品标准、战略新兴产业相关领域标准优先立项。目前,我国医疗器械标准与国际标准一致性程度达到90%以上,标准体系的覆盖面、系统性不断加强,医疗器械标准的整体水平不断提升”。
在参与国际标准制修订上,2020年共提出《医用输液器 第15部分:避光输液器》《组织工程医疗产品-脱细胞基质支架材料的残留DNA定量检测方法》等9项医疗器械国际标准立项申请,其中1项已成功立项,2项已通过成员国同意,进入项目立项(NP)投票阶段。
《年报》还显示,由我国主导或牵头的8项医疗器械国际标准制定,其中由我国提出并成功立项的首个新冠疫情防控相关医疗器械国际标准项目已结束国际标准草案(DIS)投票;《心血管植入物-心脏封堵器》《医用输液器 第15部分:避光输液器》等2项国际标准项目已通过了委员会草案(CD)阶段投票,进入DIS投票阶段;《组织工程医疗产品 软骨核磁评价 第1部分:采用dGEMRIC和T2 Mapping技术的临床评价方法》由技术报告(TR)调整为技术规范(TS),项目立项(NP)投票阶段获得成员国一致同意,进入工作组草案(WD)讨论阶段。
另外,为应对新冠疫情,国家药监局紧急组织制定YY/T 1799-2020《可重复使用医用防护服技术要求》,及时公开标准文本。组织申报新冠病毒核酸检测试剂和高流量呼吸治疗设备专用安全等疫情防控相关6项国家标准立项,正按计划制定。组织紧急制定《医用防护口罩技术要求》《医用一次性防护服技术要求》《心肺转流系统 热交换水箱》《心肺转流系统 滚压式血泵》《气囊式体外反搏装置》《一次性使用静脉输液针》6项疫情防控重点医疗物资国家标准英文版。
在申报国家标准立项的基础上,国家药监局组织同步申报新冠病毒核酸检测试剂和高流量呼吸治疗设备专用安全等疫情防控相关国际标准立项。其中《医用电气设备 第2-90部分 高流量呼吸治疗设备基本安全和基本性能》项目,国际电工委员会(IEC)和国际标准化组织(ISO)分别以94.4%和94.7%支持率高票获得通过,并由中国专家担任该项目负责人。据悉,这是由我国提出并成功立项的首个新冠疫情防控相关医疗器械国际标准项目。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






