更快、更高成功率 临床试验设计三大变道
发布时间:2020-12-04 14:37:23作者:本报特约 科睿唯安来源:医药经济报
提高研发效率、增加新药上市成功率无疑是各制药公司研发的努力方向。随着申办方对研究中心绩效、监管审评审批流程和时间线、疾病的流行病学特征以及不同国家受试者招募等情况的深入了解,临床试验的设计策略也被不断调整。
其中,国家选择、适应性临床试验设计和基于生物标志物的精准治疗和受试者招募等方面的变化,在临床试验设计时更受重视。
国家选择位次变化
中国升至第二,仅次于美国
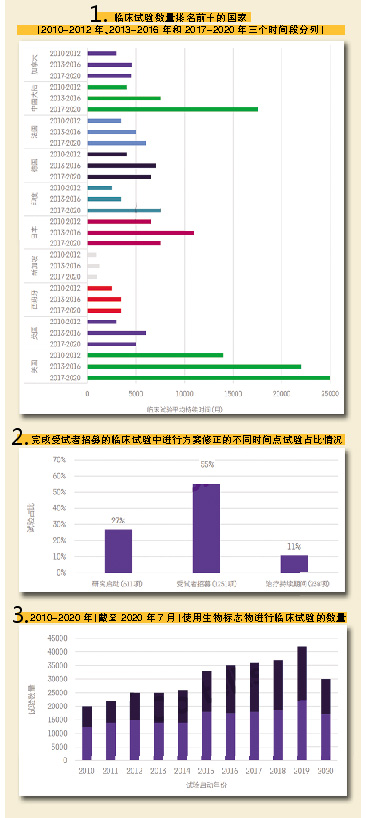
申办方对开展临床试验的国家的选择发生了变化,这从在各国进行的临床试验数量的变化趋势可以反映出来。近十年,临床试验数量排名前十的国家发生比较明显的变化。
特别是中国,在过去数年开展的临床试验数量出现大幅增长。2017-2020年,中国开展的临床试验数量飙升,居全球第二位,仅次于美国。这可归因于今年截至目前针对COVID-19已开展的大量研究,以及过去数年中国监管机构为简化和缩短审批流程以及与国际标准接轨而在审批流程和批准方面进行的改革。
印度开展的临床试验数量增多,则是因为该国2019年对药政监管法规进行了修订,开始启用个体化的审评时限。此举增加了监管审评通道的透明度,而且达到了国际合作伙伴对审评质量的预期。
值得关注的是,日本开展的临床试验数量出现大幅下滑,从2012-2016年全球第二的位置下跌至目前的第三位。日本于2018年出台的旨在提高临床试验可靠性的监管法规修正案,可能对正在进行的临床试验数量产生负面影响,可能的原因是法规变更会导致财政支出和行政管理负担大幅增加。
“非常规试验”增加
适应性试验设计受重视强调入组前设计
根据Cortellis临床试验情报,过去10年,临床试验的启动数量逐年增加,并显现出两个明显趋势:一是Ⅱ期临床试验数量在临床试验所有阶段中的占比最高;二是包含“非常规试验阶段”(即临床试验中的某些试验阶段不符合FDA的定义)的临床试验数量明显增加。
Ⅱ期临床试验中出现的变化趋势,可以由进入Ⅲ期及后续试验阶段的临床试验比例较低(31%~38%)得以解释。
而含有“非常规试验阶段”的临床试验数量增加,则表明临床试验设计正逐渐被调整。将不同试验阶段进行融合或使用加速审评通道以加速上市的设计,被越来越多临床试验采用。快速通道状态、适应性试验设计和孤儿药研发(特别是次要适应症)的增加,可能与这种转变直接相关。
在Ⅰ~Ⅲ期试验中,至少有50%在启动后需要进行至少一次修正,通常在临床试验的入组阶段进行,但这会导致临床试验的进度延迟和成本增加。
而在研究设计阶段对患者分组方法加以改进,能够提高受试者招募数量,减少和避免不必要的修正,并缩短试验持续时间。
“篮式试验”和“伞式试验”
基于生物标志物缩短试验时间、提高成功率
使用基因组学定义和选择入排标准,是基于生物标志物进行的临床试验(包括篮式试验和伞式试验)的共同特征。
在FDA“使用同一个研究设施、试验设计和研究方案,在多项子研究中同时对多种药物和/或患者人群进行评价,从而提高药物研发的效率和速度”指导原则下,这类设计使得共享对照组或集中进行数据采集成为可能,从而提高临床试验设计方面的灵活性和临床试验的效率;避免低效地为每一种药物或每一个亚组患者人群制定新的研究方案。
解决受试者招募难题
遵循精准医疗的原则,这些设计对那些最有可能从疗法中获益的患者进行识别。
“篮式试验”是在多个患者人群中对单一疗法疗效进行评价的试验,通过疾病类型、疾病分期、既往治疗数量、遗传因素或其他生物标志物或人口统计学特征对这些患者人群进行定义。
“伞式试验”是在单个患者人群中同时对多种疗法(单药治疗或联合治疗)的疗效进行评价的试验,根据疾病分期、既往治疗数量、遗传因素或其他生物标志物或人口统计学特征将一个患者人群分为多个亚组。
过去五年,这两种临床试验设计获得了更为广泛的应用。虽然这两种试验设计最初被用于针对肿瘤适应症的临床试验,以更好地针对具有预测价值的生物标志物和靶向治疗进行联合应用,但最近已被用于肿瘤之外的其他治疗领域。
提高试验成功率
使用生物标志物对患者进行分层,可确保对患者和研究治疗进行最佳匹配,在降低试验损耗率的同时提高试验成功率。对于针对肿瘤适应症进行的试验尤其如此,因为这类试验已受到试验持续时间的限制。有数据显示,肿瘤适应症的试验持续时间,几乎是非肿瘤适应症试验的两倍。
在提升肿瘤在研药物上市成功率方面,采用生物标志物可使成功率提升一倍:采用生物标志物和不采用生物标志物的成功率分别为10.3%和5.5%。而进一步对基于生物标志物的患者分层后,成功率升高至10.7%。
不过,过去3年,生物标志物在临床试验的使用率仅50%。而这恰恰表明其中蕴藏着机会,使用生物标志物对患者进行分层,临床试验的成功率还有提升空间。
对肿瘤适应症的临床试验进一步分析可发现,使用生物标志物分层的占比有所降低,尽管这一比例(57%)仍高于2019年的总体数据(48%),但与预期相反。
虽然纳入携带基因变异的患者可以提高患者分层的效果,但事实上仅有一小部分的肿瘤试验(自2019年开始约有10%)采用这种方式对患者进行分层。自2010年以来,这类肿瘤试验的比例仅增加了约3%。而肌肉骨骼疾病的这类试验比例(约2%)在2010-2019年间保持不变。
研究中心的更好选择
在临床试验中,对受试者识别、招募和入组起关键作用的是研究中心。制药公司有加快受试者的招募进度来缩短试验持续时间的需求,因此,增加研究中心的数量可能会成为制药公司试验提速的另一种策略。
可以选择能够对目标生物标志物进行检测的研究中心,这样需要招募的患者人数会减少。由于能够选择最有可能从治疗中获益的患者,因此临床试验可以在减少入组患者人数的情况下达到疗效终点。此外,选择对招募目标患者人群有经验的研究中心,可在一定程度上确保招募到目标患者人群,提升试验的效率。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






