PD-1/L1新药受理达470个 生物药立项如何破局?
发布时间:2020-11-16 11:00:46作者:本报记者 张松来源:医药经济报
PD-1/L1新药受理达470个
生物药立项如何破局?
10月29日,国家药品监督管理局药品审评中心(CDE)公示,君实生物递交了PD-1抑制剂特瑞普利单抗注射液一项新的临床试验申请,加速推进新适应症的扩展。作为肿瘤免疫治疗的明星靶点,PD-1/L1抑制剂的开发不仅成为了国内药企争先进军的热门领域,目前也已陷入同质化的竞争“红海”。
有业内人士在日前的第五届成都生物医药创新发展大会上透露,来凯医药在10月21日向CDE申报临床试验的LAE005注射液(JXSL2000187)已是国内累计的第64款PD-1/L1抑制剂。与此同时,根据CDE数据,截至10月28日,以PD-1/L1为靶点的新药受理号达到了470个。
抗体新药研发严重同质化
在业界看来,由于具备药理活性高、毒副作用小、靶向性强等显著优点,以单抗、重组蛋白等为代表的生物制药近些年在疾病治疗中得到愈来愈多的应用。无论是针对影响人类健康的重大疾病问题,还是针对制药企业寻求自身生存或发展的问题,生物制药都扮演着重要的角色,发挥着传统药物不可替代的作用,从2019年全球销售额排名前 10 的药品中,生物药占据6个席位即可见一斑。
而随着阿达木单抗、英夫利西单抗、利妥昔单抗、贝伐珠单抗、曲妥珠单抗等重磅单抗类生物药近些年来陆续在欧美专利过期或面临到期,生物类似药领域吸引了包括跨国药企以及本土原研生物药制造商的进场角逐,这一细分市场有望实现爆发式增长。据中国产业信息网预测,2022年中国生物制药市场将达755亿美元,预计约占中国制药市场整体规模的22.8%,约占全球生物制药市场的18.7%。
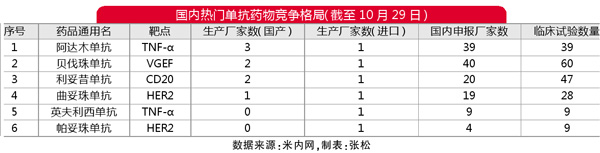
潜在的市场增长预期难以避免药企扎堆赛道,除PD-1/L1抑制剂以外,多年蝉联全球药品销冠的阿达木单抗也引来国内多达39家药企申报布局。针对抗体新药研发严重同质化竞争的本质,百奥赛图董事长沈月雷表示,药企在新药立项时,对靶点分子的选择与其是否亲手经历过该靶点研究和熟悉程度深浅其实并无直接关联,很多时候选择的动机就来自于科学文章。“但尽管是非常好的科学杂志,可能只有10%的文章能够实现重复,很多药企基本无从下手,只是道听途说看到其他药企较好的临床数据,认为自家企业也可以跟随,临床或许能够做得更快。”
君实生物首席运营官冯辉在接受本报记者采访谈及特瑞普利单抗的研发历程时也表示:“研制抗PD-1单抗是2012年成立君实生物时的想法,最开始是避免未知风险,因此找到已经验证好的靶点来做出创新抗体,这是当时的标准。现在应当与时俱进,看看是否可以凭借企业的人才和这套体系开发出国际领先的全球首创药物(First-in-class)靶点,而不只是同类最佳(Better-in-class)。”
沈月雷认为,在后PD-1/L1时代,药企面临的不是能够开发的药物靶点较少的难题,而是是否愿意冒着较高失败风险探索新兴靶点。“从数据库来看,我们找到的可开发抗体药物的靶点约为1500多个,目前在国外处于临床阶段的药物靶点约为400个,而中国进入临床的药物靶点却只有30~40个。临床潜力较大的成药靶点还是很多的,但很多新靶点需要进行药效验证,目前仍然缺少较好的动物模型进行验证。”
药企调整研发模式成必然
业界普遍认为,近些年药政改革促使我国新药研发环境发生较大变化,恒瑞医药副总经理、研发中心CEO陶维康表示,仿制药一致性评价推动仿制药质量国际化,NMPA加入ICH实现监管制度国际化,鼓励开展国际多中心临床试验(MRCT)体现创新药研发国际化,进口药加速进入中国说明国内医药市场走向国际化,对国内制药企业提出了新的要求和挑战。“在这样的条件下,要求药企研发新药要从中国新走向全球新,从中国市场走向全球市场。药物要能真正给病人带来益处,与现在已有药物相比要有更好的疗效,体现出所谓创新的临床价值。”
在他看来,面对本土药企创新药研发难题,解决办法无疑要从提升新药研发的创新力度,提高新药研发的效率和速度,以及加快国际化步伐等维度入手。“在国内做首创新药目前还面临着较大困难,因为药企研发基础并不扎实,仍然存在诸多门槛,但还是要坚定该目标朝着该方向前进。当然,药物的创新度越高也意味着研发失败风险性越大,而且不同种类的药物比如生物药大分子和化药小分子本身的成功率就有着较大差别,这就要求药企进行深度研究。”
此外,前述专家提醒,如何在保证药物质量前提下,通过优化流程、采用新技术、建立关键技术平台、加强转化研究等手段,提高效率和速度,形成高效的研发体系,也是新药研发过程中的重要环节。“与此同时企业还要加强对外合作,既能引进开发,也可以走出去实现对外授权,最终的目的是形成企业自身的优势和特长。如果新药与其他企业相同,时间又晚于竞争对手,没有更多的临床价值,也就没有市场价值。”
而在创新药靶点的选择上,陶维康强调了药企研发模式调整的必然性,可以秉持“更新、更快、更优”的原则:“更新”是指企业要勇于探索和尝试国际前沿具备First-in-class特质的靶点,但相应地要承担研发失败的高风险;“更快”则是药企可以追踪全球热门靶点或技术,诸如PD-1/L1、KRAS等靶点以及细胞、基因治疗等技术,项目研发进度能够快速跟上;“更优”是指药企可以手持一定比例的成熟靶点,从中产生具有差异化的Best-in-class的创新药物。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






