细胞与基因疗法:可及性挑战与机遇
发布时间:2020-10-21 14:44:11来源:医药经济报
亲历2020 HTAi线上会
细胞与基因疗法:可及性挑战与机遇
上周,国际卫生技术评估组织(HTAi)以“让病人能够得到细胞和基因疗法”为主题举办了线上虚拟专题讨论会。会上,笔者介绍了中国CAR-T细胞治疗研发的现状与成就,专家也对当前细胞和基因产品疗法面临的最大挑战作了分析。
中国情况
截止2020年6月,根据Clinicaltrial网站的登记,中国已有131个细胞治疗产品,共开展了148个临床试验。吉利德和Kite公司生产的Yescarta(益基利仓赛注射液)已于2020年2月成为在中国首个申请上市的CAR-T 产品,预计在未来2~3年内细胞和基因治疗产品有望申请纳入国家医疗保险报销目录,开展价格谈判。
目前申报细胞和基因治疗的病种主要为血液肿瘤和实体瘤两个方面,前者以CD19和BCMA靶点为主,通过率分别达到61%和80%。但大部分临床试验尚处于临床Ⅰ期或Ⅱ期阶段,用于小儿急性淋巴细胞白血病、急性粒性白血病、复发性和难治性急性髓细胞白血病以及非霍奇金淋巴瘤等疾病的治疗。细胞和基因治疗面临的主要挑战是安全性问题,包括细胞因子释放综合症和神经毒性反应等。在技术管理方面,业界最关心的问题是医疗机构选择CAR-T制备机构的标准是什么,以及开展CAR-T治疗的医疗机构应该具备哪些条件。2017-2019年中国相继出台制定了《细胞治疗产品研究与评价技术指导原则》《医疗机构CAR-T临床应用的标准》,无论是政府部门还是行业组织,均十分关心未来中国细胞和基因治疗的发展和规范。
笔者认为,在中国,多渠道筹措CAR-T研究经费是必要的。由于中国医疗保险服务于基本医疗的性质和发展高新技术需要的高额补偿之间存在矛盾,细胞和基因治疗的医保补偿在将来依然是一个问题。为了避免财务预算和临床结果的不确定性,需要进一步考虑创新支付方式。
在讨论通过什么样的筹资机制来促进高价细胞或基因治疗在中国的发展时,业内专家提出可否采用超孤儿药的多渠道筹资模式,建立特殊的基金或预算;或采用国际上常用的,如果没有达到预先设定的治疗目标时可以返回治疗费用的风险分担机制。并提到可否通过价格谈判或利用国内细胞和基因治疗产品的市场竞争机制来降低CAR-T产品的价格;建立医院联盟,通过第三方论证机构对医院或制备机构进行资格论证,确保治疗的安全性。
国外现状
全球有多个公司涉足细胞和基因产品的研发、生产。以诺华为例,其已向全球提供了三种细胞和基因治疗产品。细胞治疗产品Kymriah(tisagenlecleucel)主要治疗急性B细胞淋巴白血病(ALL)和弥散性大B细胞淋巴瘤(DlBCL),前者发病率为1.3/10万,后者为2.5~4/10万,目前该产品已在26个国家获得了报销。基因治疗产品Luxturna,为RPE65介导的治疗遗传性视网膜萎缩(inherited retinal dystrophy,简称IRD),该病的发病率为1/20万,该产品目前已在9个国家的市场获得报销。还有一个基因治疗产品Zolgensma,是针对侧索肌肉萎缩症(spinal muscular atrophy,简称SMA),该病的发病率为每1100万人中有一个发病,属于罕见病,该产品现已在美国、法国、德国和日本四个国家得到报销。
从药企角度来看,影响细胞和基因疗法应用的主要因素有三个:一是价值的挑战,主要是对长期结果的不确定性;二是价格和经费的挑战,细胞和基因疗法属于一次性治疗,虽然以价值为基础定价,但标价太高;三是患者确定的挑战,即最终患者人数的高度不确定性。
为此,我们需要建立整体解决方案。首先要树立一个价值为基础的定价观念,注意细胞和基因治疗带来的成本效果以及各方面的价值。如能改变患者生命的影响,具有长期的疗效,能避免和减少卫生系统的各项费用,包括政府、个人、社会救助和当前患者医疗费用的支出。其次是需要创新解决可及性的方案,帮助卫生系统提供细胞和基因治疗的方法。如通过价格谈判,开展以临床治疗结果为基础的协议,或推行按年支付的年金制(annuities),将高额费用按年度分摊。三是注重加强卫生系统的力量,建立战略合作的关系。如需要卫生政策的支持、诊断方法的配合运用、提高诊断率、加快临床医生的能力培养等。
英国的态度
英国将基因治疗药物(gene therapy medicines,即含有导致治疗、预防或诊断效果的基因)、干细胞治疗药物(somatic-cell therapy medicines,即含有被操纵以改变其生物特性的细胞或组织,或不打算用于身体同样基本功能的细胞或组织)、组织工程药物(tissue-engineered medicines,即含有一些细胞或组织经过改造,可以用来修复、再生替代人体组织)统称为高级治疗药物(Advanced therapy medicinal productr,简称为ATMP)。这些高级治疗药物指包含基于基因、细胞或组织工程基因的药物。
这些细胞和基因治疗药物的特点是制备过程耗资巨大,研究过程往往缺乏资金且需要多专业的人才参与。因此,其面临的挑战不仅在于高昂的前期费用(upfront cost),且长期的效果不确定,还在于在制备过程缺乏资金和专门技术人才,制造过程昂贵。此外,临床证据有限,因为不可能开展临床随机对照试验,结果的外推性有限,临床结果只能用替代指标而不是最后的临床结果,报告的结果也因此是相对比较短期的,临床证据有待不断完善。正因如此,需要上市后进一步收集数据。
英国开展管理型的可及性协议(managed access agreement),其实质就是我们常讲的风险分担协议(risk sharing agreement),通过商业协议安排获得英国卫生服务系统(NHS)的支持。药企要承诺在一定时间范围内进一步收集附加的临床结果资料,获得卫生技术评估,并获得不同相关利益集团的同意,包括企业、NHS、NICE和患者组织。最后商业安排有以下三种形式:(1)患者可及计划单纯的药价打折(simple discount patient access scheme,简称PAS)),过程可以保密,适用于广泛的适应症;(2)复杂的PAS计划 (complex PAS),比较复杂,可以针对特殊的适应症,但交易结果不易保密;(3)商业可及的协议(commercial access agreement,简称CAA),类似于PAS,但由中央一级实行交易,可以做到保密。可管理不确定性、可负担性,可建立专门的肿瘤基金(CDF)或高新技术基金(HST)。
总之,要尽可能多地收集临床资料,使结果透明化,同时要认识到细胞和基因疗法存在的局限性,有计划开展进一步随访和前瞻性的资料收集,早期介入和共享财务风险以减少结果的不确定性,做好敏感度分析,同时要事先考虑到有哪些可能因素会影响到最后行政部门的决策。
当前挑战
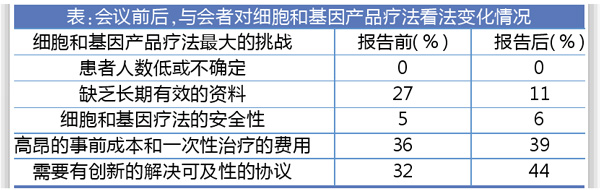
研讨会上,主持人诺华肿瘤新兴市场负责人Fran Milnes女士就当前细胞和基因产品疗法面临的最大挑战向参会者发起投票,以了解在专家报告演讲前后参会者对于细胞和基因产品的认识是否发生改变,其结果见上表。
尽管由于调查人数不详,无从比较前后差异的显著性。但从结果分析来看,细胞和基因疗法主要面临的最大挑战还是高昂的一次性治疗费用和需要提出更多的创新支付方式来解决治疗的可及性。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






