研发线收缩 巨头热衷挖潜已上市药品
发布时间:2020-09-23 14:56:40作者:综合编译/廖联明来源:医药经济报
分析发现,大型制药企业在研的候选新药变得越来越少,但对每个新药进行的新适应症研究却越来越多
EP Vantage一项最新分析发现,过去几年大型制药企业新的关键阶段项目的数量明显下降。与此同时,其在已上市的新药上投入了更多资金,开发新适应症以挖掘更大的市场潜力。
相关数据显示,自2014年以来,上市新药的新适应症试验的平均数量明显增加。这在很大程度上是受肿瘤免疫产品的推动,但在其他新药上也可以看到同样的趋势。
“OK”药领衔适应症拓展
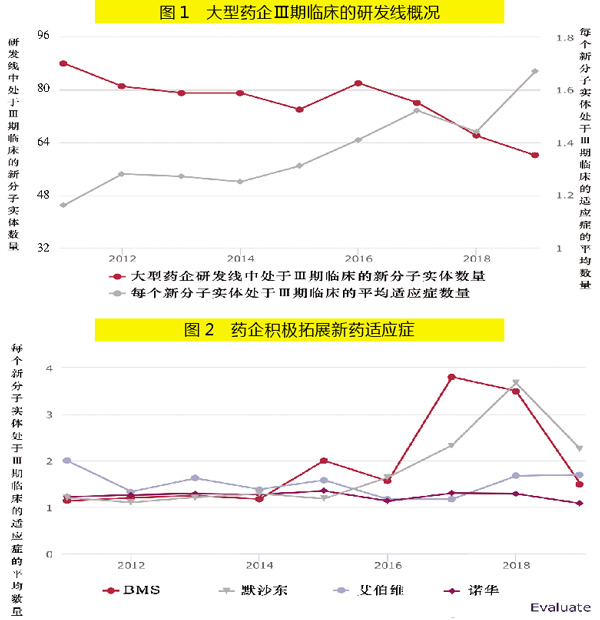
如图1显示,在肿瘤免疫产品市场起飞的同时,大型制药企业的在研新药数量开始收缩,但这一趋势并不体现在启动的试验数量出现减少上。根据EP Vantage统计,全球11家大型制药公司在2019年启动了2243项新分子实体(NME)的Ⅲ期试验,这一数字仅比2011年下降了4%。
但与此同时,这些制药公司进入Ⅲ期临床研究的候选新药数量下降了32%。这是通过EvaluatePharma公司的历史上市新药数据计算得出的,EvaluatePharma每年4月进行一次统计。
为了分析每个NME的平均适应症数量,Vantage每年会收集所有Ⅲ期临床试验——无论是已上市药物还是仍处于研发阶段的新药。该分析只纳入了主要申办方是大型制药公司的临床研究,他们还统计了每年启动的试验中每种产品涉及的不同适应症的数量。这使其可以计算大型制药企业的Ⅲ期临床研究中每种新药的适应症的平均数量。
结果显示,2019年,NME开展临床研究的适应症平均数量为1.7项,高于2011年的1.2项。
具体来看,默沙东(MSD)的Keytruda与百时美施贵宝(BMS)的Opdivo在很大程度上推动了这一趋势。这两个PD-1抑制剂都进行了大量的临床研究,此外,阿斯利康(Astrazeneca)的Imfinza和罗氏(Roche)的Tecentriq也正在进行广泛的临床试验。
默沙东对Keytruda的临床研究投入打破了纪录。2015年,针对9种不同的肿瘤类型,Keytruda启动了14项Ⅲ期临床试验。
应避免过度依赖单一产品
在大量拓展适应症上,PD-1/L1抑制剂并非首开先河。事实上,类风湿性关节炎、克罗恩病和银屑病等疾病的免疫疗法的兴起也促使相关药物在许多疾病中进行了临床试验。艾伯维(Abbvie)的阿达木单抗(Humira)和诺华(Novartis)的苏金单抗(Cosentyx)在这方面尤其突出。
因此,从图2中可以看到,在肿瘤免疫市场占主导地位的公司与聚焦自身免疫疾病的公司单个新药研究的适应症数量存在上升势头。
Ⅲ期临床研究的数量正在收缩,更多的注意力集中在更少的新药项目上。这一战略是否奏效是另一个问题,当然总会有赢家和输家;在肿瘤免疫学产品领域,默沙东已经将其他竞争者甩在了身后。
但与此同时,大型制药公司也面临需要强化后期研发线的压力,其被要求转型进行多元化产品的开发,而不是消耗大部分的人力物力在一些重磅产品上。例如,艾伯维因过于依赖阿达木单抗而受到热议,默沙东对Keytruda的过度依赖也同样存在隐忧。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






