抗癌药NCCN扩容攻略
发布时间:2020-09-16 16:02:44来源:医药经济报
如何获得“超适应症”“治疗线前移”市场?
对于制药公司来说,肿瘤领域无疑是个极具吸引力的市场。预计到2024年,全球肿瘤药销售额将从2018年约1250亿美元(约占全球市场份额的15%)增长到约2350亿美元(约占全球市场份额的20%),复合年增长率(CAGR)约为11%。此外,2011-2016年期间推出的重磅药物中,约有35%~40%是肿瘤药物。
其中,获得“超适应症”和“治疗线前移”的市场扩容,是肿瘤药企业获得高额利润的重要战略。因此,制定一套与世界接轨的指南和药典战略至关重要,尤其是NCCN战略。
在美国,美国国家综合癌症网络(NCCN)的建议用药推动了药物在更前线的治疗和其他适应症中的使用(即非主要/非注册适应症),是公立和私营保险公司在决定新的和现有肿瘤药物报销覆盖范围时会考虑的黄金标准。
中国肿瘤治疗市场正与国际接轨。由于NCCN指南对中国医生临床实践的影响力度,NCCN战略对肿瘤药在中国市场的拓展也发挥着十分重要的作用。
复杂市场
独特挑战
尽管药物开发方面已经取得了长足进展,但几乎所有肿瘤类型仍存在巨大的未满足需求,这吸引了大量的研发投资,已有数百家公司研发了数千种药物。然而,复杂的市场动态给制药公司的战略规划带来了独特挑战。
a.如何推动或赶上快速的创新步伐(例如生物标志物为基础的泛肿瘤治疗的出现)?
b.如何应对不断发展的治疗模式(如靶向治疗和分期治疗)?
c.如何顺利通过充满不确定性、昂贵且漫长的批准程序?
d.在竞争日益激烈和以价值为中心的环境中,如何获得有利的医保支付覆盖范围?
e.如何使可及患者群体最大化?
f.在药物生命周期的各个阶段都面临激烈的竞争,如何应对?
g.如何计划和管理适应症扩展,以延长药物的生命周期?
h.如何保障非FDA批准的适应症的报销(即“超适应症”或“扩展适应症”)?
对这些问题的追问与解决,是许多肿瘤药物获得成功的关键内容。
“捷径”NCCN
在美国,目前已经有5种药典得到了美国联邦医疗保险和医疗补助服务中心(CMS)的认证,可用于确定药物从医学角度而言适用于哪些适应症,并为保险报销决策提供支撑信息。
在5个CMS认证的药典中,NCCN是唯一一个专注于肿瘤治疗的。NCCN指南涵盖97%的肿瘤类型,并根据最新的循证医学证据进行更新。其被广大医生和医保支付方视为肿瘤药物评估和使用的黄金标准。
鉴于NCCN评定意见对报销和患者用药有重大影响,制药公司必须在药物上市前后/生命周期管理阶段就重视并考虑向相关机构和组织提交数据和临床试验证据。
一个由多学科专家组成的小组对提交给NCCN的数据进行评估。1类或2A类能获得大多数商业医保支付者的报销;而第3类则不能获得大多数支付者的报销。此外,对于大多数医保支付方而言,如果肿瘤药物被NCCN评定为1类、2A类或2B类,其超适应症使用的情况也可以被报销。
提交数据给NCCN获得评定意见与获得FDA批准是相互独立的,可以在FDA批准之前或者之后进行。对于已获批的药物,公司也可以要求提交新的数据,证明药物在新的治疗线或肿瘤类型中的效用。
商业价值
NCCN的建议用药对扩大药品可及患者群体基数产生重要影响。特别是适应症扩展(获批新的肿瘤类型)和治疗线前移,能够使这些药物的销量得到显著增加。更重要的是,NCCN的建议通常能够在FDA获批之前获得。
由于中国的肿瘤临床实践紧跟国际步伐,NCCN的建议也可以成为药物在中国临床实践和上市申请的重要参考因素。
适应症扩展
帕博利珠单抗(Keytruda,K药)和维莫非尼(Zelboraf)是适应症扩展的两个经典案例。
默沙东的K药被FDA批准用于14种肿瘤的治疗。其通过NCCN评定可用于其他10种肿瘤,使得可及患者群体数量增长20%~30%。默沙东开展了超过25个临床试验并公开发表多篇科研文献证明其在FDA批准以外的适应症中的效用。
罗氏/基因泰克的维莫非尼于2011年获批用于晚期黑色素瘤,2017年获批用于脂质肉芽肿。这款药物经NCCN评定可用于其他4种肿瘤,这使得可及患者群体数量增长了200%~300%。首次获批后,维莫非尼又进行了至少5个临床试验,并且至少在4篇经同行审稿的顶级期刊文章中发表了相关结果。
在中国,NCCN对药品适应症扩展的影响依然存在。例如细胞治疗已被NCCN建议作为一些肿瘤的后线治疗,即使在中国还未有获批产品,许多临床医生也已据此推荐一些肿瘤病人尝试细胞治疗的临床试验。再以K药为例,2018年NCCN建议K药用于PD-L1阳性或具有MSI-H/dMMR的复发或转移性宫颈癌患者的二线治疗,即便在中国该适应症至今尚未获批,但临床实践中,已有许多医生将其用于治疗晚期/复发的宫颈癌患者。
治疗线前移
肿瘤生物学以及靶向治疗领域的突破性研究使肿瘤治疗发生了翻天覆地的变化。包括联合治疗在内的许多药物已经可以跨治疗线使用于不同疾病亚型的病人群体(例如不同的分期和严重程度)。竞争的加剧以及快速进入市场的需求导致一大部分药品在上市初期未能释放全部的商业潜力。
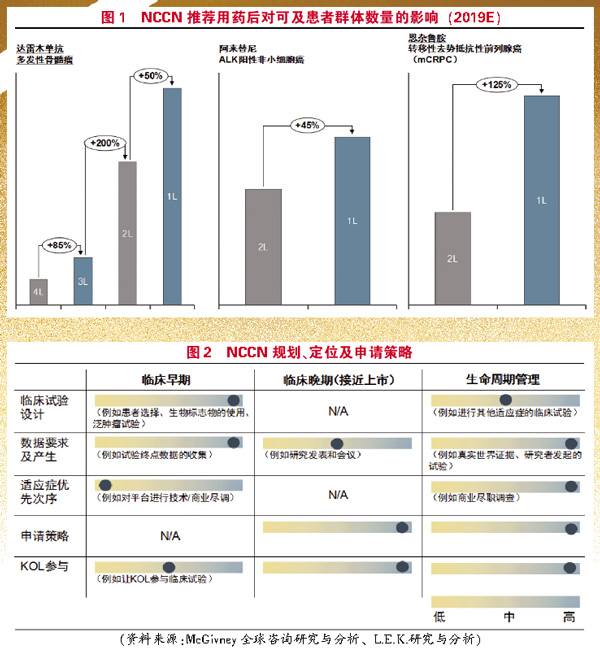
治疗线前移,可延长药品的生命周期、扩大商业潜力。达雷木单抗、阿来替尼和恩杂鲁胺是治疗线前移的典型案例。
FDA最先批准达雷木单抗(Darzalex)用于多发性骨髓瘤的四线治疗。但在一年内,NCCN将其评定为1类,并获得该药物用于二线治疗的建议,这使得该药物在三个月内销量增长了25%。随着临床试验结果的公布,这一药物在更前线治疗中的效果得到了证实。在获得NCCN用药建议的约6个月后,FDA也批准该药物用于二线治疗。总的来说,强生共获得了8条NCCN 的建议,其中2条还未得到FDA的批准,3条在FDA批准前获得,3条在FDA批准后获得。所有的NCCN建议都得到了临床试验结果的证实(至少来自于4个额外的Ⅲ期临床试验),为药物可使用的治疗线的前移提供了支持。治疗线前移的同时也将可及患者群体的基数相比于最初上市时扩大了7~8倍。
日健中外制药/罗氏的阿来替尼(Alecensa)最初被FDA批准用于ALK阳性的非小细胞肺癌的二线治疗。在此之后,基于Ⅲ期试验的结果,该药物争取到了NCCN用于一线治疗的建议。被NCCN评定为1类后,该药物在接下来的一个季度中销量增长了25%,可及患者群体基数也扩大了40%~50%。在NCCN发表建议后的6个月,FDA也批准了该药物的一线使用。中国国家药品监督管理局于2018年8月正式批准阿来替尼用于ALK阳性的局部晚期或转移性非小细胞肺癌,包括一线和二线的治疗。在2019版的中国临床肿瘤学会(CSCO)原发性肺癌诊疗指南中,阿来替尼也被作为ALK阳性患者一线治疗的优先推荐。
辉瑞/安斯泰来的恩杂鲁胺(Xtandi)也呈现出类似的趋势。该药物可用于治疗转移性去势抵抗性前列腺癌(mCRPC)。NCCN在FDA批准前就建议可将其用于一线治疗(在化疗之前),这促进了该药物销量的增长。值得注意的是,临床试验结果证实,当恩杂鲁胺(Xtandi)用于一线治疗mCRPC(在化疗之前)时,病人整体生存率得到了改善。2019年11月,恩杂鲁胺在中国获批,用于未接受化疗的转移性去势抵抗性前列腺癌(mCRPC)成年患者,成为mCRPC的一线治疗药物。
药典攻略
生物制药企业制定有效的指南和药典战略至关重要,包括发现和收集针对不同肿瘤种类、治疗线以及超适应症使用的数据。这可以扩大公立和私立医疗保险对疾病的覆盖、提升药物的可及性,帮助药物在竞争日益激烈的肿瘤市场获得更多的市场份额。
一个强有力的指南和药典战略需要涉及药品生命周期的所有阶段,且需要多个部门共同参与。其中,创新型生物医药公司应争取做到以下几点,才能在医保、市场准入和药物使用上获得最大优势:
首先,评估目标肿瘤领域中所需要的数据(例如进行模拟药物分析、对标分析),将这些数据结合到临床试验设计中,从而在NCCN的评审中获得有利条件。
其次,随着临床试验的进行,有策略地发布最新的试验证据(例如会议报告、公开发表等),并且在提交NCCN申请时,强调大型临床试验所证实的终点数据和结果。
另外,除了积累临床试验证据,还要结合关键意见领袖的观点,收集他们对药物潜力的看法,并且进行额外的数据收集和分析,这可以进一步巩固公司的NCCN申请。
最后,通过KOL的分析、真实世界数据的收集以及向NCCN递交申请时研究者发起的研究(研究者发起的研究通常在主要/注册适应症上市之后进行),来发掘药品治疗前移以及扩展到其他适应症的机会。
鉴于NCCN可以基于临床试验证据以及专家观点做出药物超适应症使用的建议,制药企业可以抓住这一重大机会扩大自己的产品在市场上的影响力。
总结
考虑到中国肿瘤临床实践与美国NCCN的趋同,争取获得NCCN的建议对于药品在中国市场的发展同样重要。一方面,鉴于NCCN对中国医生的影响,可以在药品上市前建立良好的用药意识和市场基础,NCCN用药建议也成为了中国医生超适应症使用药品的重要参考标准;另一方面,NCCN对于治疗线前移的建议不仅能够推进药物在FDA的获批进展,也对药物在中国市场占领治疗前线奠定了基础。
作者:Jonathan Kfoury、Robert Albarano、曾凡凡(L.E.K.);William McGivney(McGivney Global Advisors)
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






