干细胞产业日本崛起
发布时间:2020-06-10 14:50:45作者:廖联明来源:医药经济报
一面是乱象丛生,另一面是全球标杆,何解?
2012年,因“体细胞重编程技术”研究,时任京都大学教授的山中伸弥获得当年的诺贝尔生理或医学奖。2012年12月,上任不久的日本首相安倍晋三许诺在未来十年内投资1100亿日元(约10亿美元)用于发展再生医学,作为振兴日本经济的重要手段之一。为了促进企业发展和将日本定位为再生医学世界领导者,他很快宣布了两项对再生医学产品“松绑”的法规,即《再生医学安全法》和《药品和医疗器械法》,希望快速改变临床应用缓慢的状况。
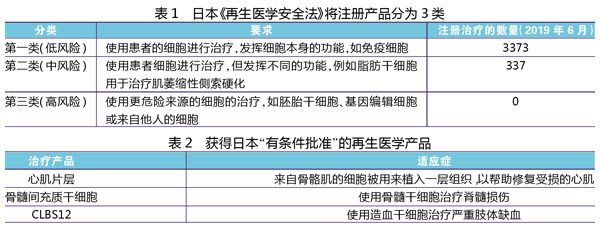
这些政策推动了日本再生医学行业的发展。在这些法规5年时间的推动下,日本数百家诊所获批了3700多种不同的治疗方法,其中包括许多基于干细胞的治疗方案,并鼓励了一批外国公司在日本开设诊所。日本真正成为了全球再生医学疗法应用中心。
但是,许多公司正利用这个监管法规,将许多缺乏临床证据支持的产品卖给了病人。使用这些产品的病人可能得不到有效的治疗或者耽误了其它有效的治疗手段。
两条快速通道
日本出台的两项法律,为干细胞治疗和其他类型的再生医学进入市场提供了一条快速通道。
《再生医学安全法》(ASRM)允许医院和诊所无需经过常规试验证明药物有效就可推广细胞疗法。医院需要证明他们有一个经日本卫生、劳动和福利部认证的细胞生产设施,然后由独立的伦理委员会审核即可。
另一项是《药品和医疗器械法》的有条件批准条款。根据该条款,一家公司获得“有条件批准”后,产品可以在全国范围内销售。公司可以出售相关产品长达7年,条件是在7年期间必须收集疗效数据,证明其疗效。到目前为止,有3种治疗方法获得了日本有条件批准。
过于宽松之弊
对于《再生医学安全法》,批评人士认为,相关注册信息可能会产生误导。患者会将登记注册视为得到了政府的“疗效验证”,这是一种真正的风险。
例如东京的“Avenue Cell Clinic”,更像是一家水疗中心。它在其网站上强调其治疗方法在ASRM注册中心可以查到。他们从肌萎缩侧索硬化病人的脂肪中制备干细胞,以延缓神经退行性疾病的进程。每剂干细胞的费用为150万日元。
简化临床试验所需的批准条件也激起了科学界的关注。
国际干细胞研究学会指出,在小规模试验的基础上批准干细胞产品上市,可能会削弱业界对该领域科学标准的信心。争论的核心是随机、安慰剂对照试验的价值,这是公认的临床研究的金标准。但2012年日本再生医学学会明确指出,证明疗效的试验设计不应总是要求采用这个金标准。
山中伸弥在放松管制问题上一直保持沉默。他的研究所不愿仓促将干细胞疗法引入临床。他表示,只要有可能,就应该考虑双盲对照研究,提倡科学家应该尽最大努力使临床试验尽可能客观和科学。
仍是全球标杆
尽管该体系存在漏洞,但日本一直试图让其再生医学政策在其他国家得到推广。根据日本药物管制司发布的一项五年计划,政府资助了旨在“传播日本再生医学产品监管模式,增强对日本监管机构的信任,并将日本监管模式引入其他国家”的推广计划。
确实,日本在放松管制方面的大胆尝试已经开始影响其他国家和地区。例如中国台湾根据日本模式起草了再生药品有条件审批法,韩国也在8月批准了类似日本的制度。印度在2015年首次有条件批准再生医学的审议中提到了日本的制度。美国、英国和加拿大等国家的监管机构则一直面临来自企业和患者团体越来越大的压力,要求其采取类似于日本的方法。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






