2019年境内三类获批增86% 医疗市场“强者恒强”
发布时间:2020-04-08 13:54:10作者:本报记者 胡睿来源:医药经济报
近年来,随着医药改革不断深化,我国医疗装备产业体系不断完善升级,不仅加快了一批高性价比产品投入临床应用,也加快了一批医疗器械关键核心技术实现突破。面对高品质医疗服务需求不断增加,各类技术加快融合,相关制度逐步完善,医疗装备产业面临难得的发展机遇。
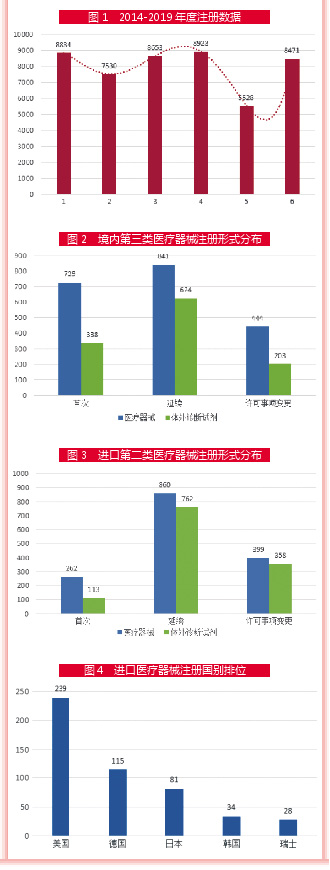
3月17日,国家药品监督管理局发布的《2019年度医疗器械注册工作报告》(以下简称《报告》)显示,2019年,国家药监局共批准医疗器械首次注册、延续注册和变更注册8471项,与2018年相比注册批准总数量增长53.2%。其中,首次注册1726项,延续注册4504项,许可事项变更2241项。
而从分类来看,2019年批准境内第三类医疗器械注册3179项,与2018年相比增加86.0%;批准进口医疗器械5292项,与2018年相比增加38.6%,进口第三类医疗器械注册2538项,与2018年相比增长38.9%。
国家药监局药品监管司相关负责人在接受《医药经济报》采访时表示:“近年来,境内第三类医疗器械注册增长较快,目前来看,与进口产品已经开始日渐趋同。”
这也意味着,在高端医疗器械领域,国内市场竞争逐步激烈、研发能力“强者恒强”的局面开始显现。
心脑血管领域提速快
《报告》显示,注册的境内第三类医疗器械,除体外诊断试剂外,共涉及《医疗器械分类目录》中19个子目录的产品。
注册数量前五位的境内第三类医疗器械是:无源植入器械(239个),注输、护理和防护器械(139个),神经和心血管手术器械(90个),医用成像器械和有源手术器械(31个)。
相关负责人介绍,从2019年境内第三类医疗器械注册情况看,相关注册产品生产企业主要集中在沿海经济较发达省份。其中,江苏、北京、广东、上海、浙江是境内第三类医疗器械首次注册数量排前五名的省份,占2019年境内第三类医疗器械首次注册数量的69.1%,与2018年相比略有增加。
而注册的进口医疗器械,除体外诊断试剂外,共涉及《医疗器械分类目录》中23个子目录的产品。
注册数量前五位的进口医疗器械,主要是:医用成像器械(81个)、口腔科器械(57个)、无源植入器械(50个)、临床检验器械(41个)、神经和心血管手术器械(33个)。
2019年,美国、德国、日本、韩国、瑞士医疗器械在中国医疗器械进口产品首次注册数量排前5位,注册产品数量约占2019年进口产品首次注册总数量的75.4%,与2018年相比基本持平。
不难看出,随着我国医疗器械自主创新能力的提升,神经和心血管手术器械基本已经不再依赖进口。但在医学成像上,技术能力有待提升。
采访中,记者还了解到,2019年,共有36个创新产品和12个优先审批产品进入“绿色通道”,其中涉及神经、心血管领域产品较多,包括全球较为领先的腹主动脉覆膜支架、生物可吸收冠状动脉雷帕霉素洗脱支架、经导管植入式无导线起搏系统、经导管主动脉瓣膜、一次性使用血管内成像导管、植入式左心室辅助系统、冠状动脉造影血流储备分数测量系统、一次性使用有创压力传感器。
继续提升自主创新力
《报告》显示,为持续深入医疗器械审评审批制度改革,近年来国家药监局可谓是打出了“组合拳”:发布《关于调整医疗器械临床试验审批程序的公告》,进一步优化临床试验审批程序,由“明示”许可调整为“默示”许可,这也使得医疗器械审评审批时限大大缩短。
2019年,继续扩大免于进行临床试验医疗器械目录,新增148项医疗器械产品和23项体外诊断试剂产品免于进行临床试验,对48项医疗器械产品和4项体外诊断试剂产品名称和描述进行了修订。截至2019年年底,免于进行临床试验医疗器械目录包含1003项,体外诊断试剂目录包含416项,合计达到1419项。
另外,进一步扩大医疗器械注册人制度,将医疗器械注册人制度试点推至北京、江苏、浙江等21个省(区、市)。
2019年全年共有22家企业的93个产品按照注册人制度试点获批,其中包括跨省委托生产和第三类医疗器械通过注册人制度委托生产等不同情况。
相关负责人表示:“医疗器械注册人试点扩大,不仅进一步释放医疗器械注册人制度红利,鼓励医疗器械创新,还为全面推进实施医疗器械注册人制度提供重要支撑。”
中国药品监督管理研究会医疗器械监管研究专业委员会主任委员王宝亭在接受本报记者采访时曾表示:“近年来,尽管我国具备了一定的医疗器械制造能力,但医疗器械产品依然存在结构性差距,如技术、材料、装备和工艺水平等方面的差距,缺乏自主创新技术引领下的新概念,难以制造出符合医学技术趋势的高附加值新产品,部分关键核心零部件技术尚未完全攻克,有的细分领域专业化程度有待提高,有的产业结构过于分散。”
他指出,期待新生代的企业家具有国际视野,一是要增强专利保护意识,二是要保证产品的稳定性、均一性,三是要更加注重实效的学术推广,四是要寻求知识结构相似、具有同质性的合作伙伴,同时发现更多的潜在的异质性合作伙伴形成异质性创新。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






