NASH大热,me-too/me-better跟进? 机制不明,恐“AD第二”
发布时间:2019-12-03 16:51:58作者:本报特约撰稿 边界来源:医药经济报
NASH大热,me-too/me-better跟进?
机制不明,恐“AD第二”
NASH(Nonalcoholic Steatohepatitis,非酒精性脂肪性肝炎)是近年来国内外研发热点。非酒精性脂肪性肝病(nonalcoholicfattyliverdisease,NAFLD)指除外酒精和其他明确的肝损害因素所致的、以弥漫性肝细胞大泡性脂肪变性为主要特征的临床病理综合征,包括单纯性脂肪肝及其演变的NASH、肝硬化。其中一部分患者甚至走向肝功能衰竭、肝细胞癌(hepato cellular carcinoma,HCC),最终死亡的结局。
德意志银行发布的报告显示,NASH药物市场前景巨大:到2024年,全球NASH药物市场规模将超过300亿美元;而EvaluatePharma预测,到2025年,全球NASH药物市场规模将达到400亿美元。FDA也在最近不到一年内连发指南,支持这个领域的研发。
面对这么好的市场前景,国内各大企业纷纷进入该领域,尝试走me-too/me-better路线,欲抢头筹。
但是,NASH的情况类似于阿尔茨海默病(AD),是个机制不明的领域。立项时需要考虑,NASH是否会像AD一样全军覆没?
研发方向
FDA连发两个指南,立项参考书有了!
FDA于2018年12月发布临床研究指南征求意见稿《非肝硬化非酒精性脂肪性肝炎合并肝纤维化:药物研发的临床指南(Noncirrhotic Nonalcoholic Steatohepatitis With Liver Fibrosis: Developing Drugs for Treatment)》(以下简称《非肝硬化NASH合并肝纤维化指南》),2019年6月又发布《非酒精性脂肪性肝炎伴代偿性肝硬化:药物研发的临床指南(Nonalcoholic Steatohepatitis with Compensated Cirrhosis: Developing Drugs for Treatment Guidance for Industry)》(以下简称《NASH伴代偿性肝硬化指南》)的征求意见稿。
一年内连续发布两个指南征求意见稿,可侧面反映出NASH药物研发的热度。
问题1:肝纤维化和肝硬化,哪类更受鼓励?
NASH是NAFLD中较严重的一种类型,NASH一般出现在NAFLD演化的中间阶段。NAFLD本身是一个慢性疾病过程,NAFLD的进展速度常取决于初次肝活检的组织类型,年龄超过50岁、肥胖(特别是内脏肥胖)、高血压、2型糖尿病、胰岛素抵抗、高甘油三酯水平以及家族史等,也是NASH和进展期肝纤维化的危险因素。
NAFLD在组织学上有着多样的表现形式,它可以仅仅是肝脏出现脂肪浸润,也可以是出现慢性肝脏炎症。严重时,患者的肝脏会出现纤维化和肝硬化。《非肝硬化NASH合并肝纤维化指南》主要针对的是前者的病变,《NASH伴代偿性肝硬化指南》更多对应的是后者在代偿期肝硬化的NASH。
问题2:非肝硬化NASH合并肝纤维化可否“优先审评”?
《非肝硬化NASH合并肝纤维化指南》提出,目前还没有获得批准的NASH治疗药物,考虑到NASH的高患病数量、相关的发病率、末期肝病日益加重的负担,以及器官移植可用肝脏源的有限,FDA认为找出减缓、停止或逆转NASH和NAFLD的疗法具有巨大的临床需求。鉴于尚未有标准来确定哪些NAFLD患者会进展为NASH,FDA建议研究申办者应该把重点放在开发非肝硬化NASH伴肝纤维化的治疗上,直到有方法来确定哪些患者亚群有疾病进展的风险。并且,FDA还鼓励临床申办者开发和验证诊断NASH和肝纤维化的生物标志物,因为肝活检是目前诊断这种疾病的唯一可靠方法。
在Ⅲ期临床研究中,申办者应该在登记后的6个月内完成组织学诊断为NASH合并肝纤维化的患者入组,同时应考虑到患者的护理标准和其他慢性疾病的背景治疗。此外,患者体重应该在入组前3个月内保持稳定。
临床设计方面,FDA认为NASH的Ⅲ期临床研究应该是双盲和安慰剂对照的,其目标是减缓、停止或逆转疾病进展,并改善临床结果。NASH进展缓慢,并且需要时间来评估临床终点,如肝硬化或生存期。因此,申办者应考虑将可以合理地预测临床获益,以支持加速批准的肝组织学改善作为终点,例如脂肪性肝炎的整体病理诊断、NASH临床研究网络(CRN)肝纤维化评分等,FDA将依据肝脏组织学的疗效给予加速批准。
问题3:代偿期肝硬化招募注意事项?
肝硬化可以分为两类——代偿期肝硬化和失代偿期肝硬化。《NASH伴代偿性肝硬化指南》主要针对的是代偿期肝硬化,即症状相对较轻,NASH相关性肝硬化患者氨基转移酶水平有可能表现正常;若血清清蛋白降低、血小板减少和胆红素升高,应考虑为肝硬化失代偿期,尚需进行其他检查以排除慢性肝病的其他病因。
当患者的代偿期肝硬化进展到失代偿期后,肝脏功能就会严重受损。因此,如何在NASH肝硬化的代偿期对其进行有效治疗,就成为缓解和终止肝脏纤维化、避免疾病进一步恶化的关键。
《NASH伴代偿性肝硬化指南》认为,首先要确定患者的肝硬化是由NASH而非其他疾病(包括酒精性肝病或病毒性肝炎等其他慢性肝脏疾病)引起的,并且失代偿期肝硬化患者也不得列入随机分组。
此外,FDA认为,肝硬化的诊断需要得到组织学的验证。如果不采纳组织学标准作为诊断依据,则诊断需要有其他科学依据。FDA也鼓励使用生化标志物等非侵入性手段来替代肝脏活检,并且FDA也列出了一些招募患者的生化指标要求,例如NASH患者体内的ALT与AST水平会出现升高。如果这些指标超出了正常上限的5倍,研究人员则应当避免对其进行招募。除了ALT与AST指标,患者的胆红素水平应当不超过正常上限,碱性磷酸酶水平应当低于正常上限的1.5倍。
问题4:肝硬化NASH临床终点不好定,优先审评无望
《NASH伴代偿性肝硬化指南》认为,肝硬化的组织学变化与临床受益之间的关系至今尚未确认,而且逆转肝硬化在目前看来依旧难以做到。因此,组织学改善可能并不能作为充分的替代终点。正由于目前的机制认识尚不足,FDA预计将使用传统审评流程来评估药物的疗效,而暂时不会考虑使用“加速批准”途径。这意味着NASH伴代偿性肝硬化在研药物需要在随机、双盲、设置安慰剂对照的临床试验中评估其疗效。
此外,NASH伴代偿性肝硬化在研药物的潜在肝脏毒性特别是药物诱导的肝脏损伤是安全性需要评估的一大难题。考虑到NAFLD与心血管疾病之间的关联,临床试验还应当监测心血管方面的安全性。
研发现状
机制不明、造模困难,临床研究失败率高
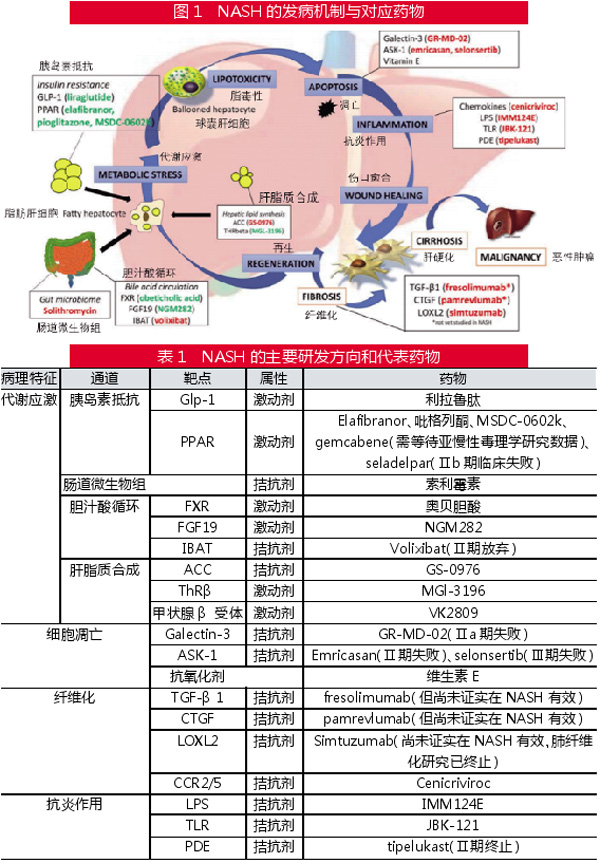
目前,NASH多针对主要病理特征如炎症、纤维化、细胞凋亡等开发药物,主要研发方向和代表药物见表1。但是,由于这些病理特征难以同时在临床前模型中模拟,从而导致NASH药物从临床前数据到临床病人疗效的转化率很低。
目前进入Ⅲ期临床的药物包括FXR激动剂Ocaliva(脂代谢类)、PPARα/δ激动剂Elafibranor(脂代谢类)、ASK1抑制剂Selonsertib(抗氧化抗炎类)以及CCR2/5抑制剂(抗肝纤维化)。
脂代谢
脂代谢的靶点包括PPAR激动剂、ACC抑制剂、ThRβ激动剂、FGF19激动剂、ThFXR激动剂等。
抑制脂肪生成,尤其是抑制胆汁酸途径的药物包括FXR配体,如奥贝胆酸(OCA),其可阻碍法尼酯X受体的活化,进而减少脂肪的从头合成。然而,奥贝胆酸在亚洲人群的不良反应较高,成为其能否在中国上市的一大疑点。
胰岛素抵抗发生时,可使用胰岛素增敏剂。最常用的胰岛素增敏剂是吡格列酮,吡格列酮为PPAR-γ激动剂。
PPAR激动剂可促进脂肪降解。但是,目前只剩下药理相对简单的PPARα/δ激动剂Elafibranor还在坚守,其余药品基本失败。实际上,Elafibranor的NASHⅡ期临床数据并不乐观,但仍挺进Ⅲ期。
抗氧化抗炎
针对炎症及氧化应激的药物包括抗氧化剂如维生素E。
ASK-1(细胞凋亡信号调节激酶)可激活JNK、P38等关键调节蛋白诱发炎症和纤维化。虽然临床前模型中能抑制p38、JNK通路活性、改善组织纤维化,但在Ⅱ期临床中表现欠佳,在肾纤维化、肺动脉高血压试验中基本失败。
相对应地,奥贝胆酸尽管副作用不小,但其改善一级纤维化患者的疗效比安慰剂翻倍,就足以让FDA批准其未来用于NASH引起的纤维化。
抗肝纤维化
NASH抑制枯否细胞炎性因子释放也是一条通路。目前该通道的趋化因子CCR2/5拮抗剂Cenicriviroc已进入Ⅲ期临床,由位于美国加州的Tobira Therapeutics开发,该公司是爱尔兰制药巨头艾尔健(Allergan)的全资子公司。
CCR2/5在枯否细胞、肝星状细胞、单核细胞和巨噬细胞上表达,并且当被激活时,促进这些细胞向肝脏的募集,诱导炎症和纤维发生。Cenicriviroc通过抑制CCR2和CCR5,从而减轻炎性反应从而起到抑制肝纤维化的作用。
★★★ 小结 ★★★
NASH的临床新药成功率极低,与其诊断机制和治疗机制尚不明确有非常大的关系。近年来我国药企纷纷进入该领域,尝试走me-too/me-better路线,NASH是其中一个热门的方向,但会不会因为机制不明确而像AD一样全军覆没,仍待时间证明。
鉴于目前的困境,上述靶点的新药可以考虑像PPARα/δ激动剂elafibranor开拓罕见病原发性胆汁性胆管炎(PBC)适应症,先上市再开始扩充适应症或者联合用药走超适应症(off-label)路线,未尝不是一条保底之路。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






