新疫苗法鼓励创新 审评审批“绿灯”开启
发布时间:2019-11-14 20:35:15作者:本报记者 胡睿来源:医药经济报
新疫苗法鼓励创新 审评审批“绿灯”开启
疫苗是特殊的药品,是国家战略性、公益性产品。为了规范疫苗研制、生产、流通预防接种全过程监管,《中华人民共和国疫苗管理法》(下简称《疫苗管理法》)已经于6月29日第十三届全国人大常委会第十一次会议审议通过,自12月1日起施行。该法是全世界首部专门针对疫苗这一品种颁布的综合性法律。
另外,为积极促进我国疫苗质量进一步提升,新颁发的《疫苗管理法》做出了一系列新规鼓励疫苗的创新和发展。第十四条指出,国家根据疾病流行情况、人群免疫状况等因素,制定相关研制规划,安排必要资金,支持多联多价等新型疫苗的研制。国家组织疫苗上市许可持有人、科研单位、医疗卫生机构联合攻关,研制疾病预防、控制急需的疫苗。
不仅如此,近日,记者在《疫苗管理法》颁布法规解读宣贯研讨会上还了解到,为了进一步鼓励疫苗产品研发创新,在疫苗产品的审评审批上也进行了相应调整。随着《疫苗管理法》的正式出台,国家药品审评部门已为创新型以及重大公共卫生事件的疫苗产品审评开启了“绿灯”。
多联多价“研发热”
据药品审评中心生物制品临床部高级审评员杨焕介绍,近年来为了加快创新型药品的审评审批工作,药审中心设立了多个疏通渠道,包括特殊审评、优先审评,以及有条件审评等。实际上,这些方式都已经在疫苗审评审批工作中应用已久,最早在甲流疫苗的审评中就采用了特殊审评,以及后来的埃博拉疫苗都启用过。
现阶段,药审中心还为创新型产品增设了沟通交流机制,企业在启动新型产品的研发前期,便可以与审评部门进行沟通交流,从而提高新型产品研发的成功率,以及缩短产品审评审批时间。杨焕也指出:“因为疫苗是一类特殊的药品,所以未来一些新的加速审评的渠道也会最先向疫苗开放。”
那么,业内最关心的创新型疫苗界定问题,药审是否已经出具了明确的规定?杨焕表示,从目前提交的注册申请来看,国内外疫苗的“研发热”主要集中在多联多价两方面。
多价疫苗是指同一个疾病的致病菌分为很多型别,疫苗针对不同型别有多价。例如上市的HPV疫苗有二价、四价、九价等,正在报批的还有十一价和十四价,审评的标准主要看这种型别的疫苗能不能形成规模。还有现在的“网红”十三价肺炎疫苗,已经有企业在申报十五价,还有一些国外企业在研发二十价,多价疫苗可以算作完全创新。
但针对多种疾病的联合疫苗,主要受制于每种疫苗的成熟度。这类疫苗虽然可以有效提高依从性减少注射针次,也要保证安全风险不能增加,有效性也不能降低。所以联合疫苗在开发的过程中一定要重视吻合程度,不仅要关注单苗的成熟度,还要看组合在一起是不是能够满足上述的标准。
杨焕指出:“针对联合疫苗的开发,国内外有很大的差别。微生物的流行在各个地区有所差异,国内的企业一定要慎重考虑国外单苗是否可以作为联合疫苗。但从药品审评的角度来看,由于联合疫苗仅仅是提高了患者的依从性,不能被看作是完全创新的产品。”这也意味着,联合疫苗的注册申报不能走“绿色”通道。
三支持、两鼓励、一优先
会上,国家药品监督管理局药品注册司副司长李芳也指出,关于疫苗注册管理工作可以用“三支持”“两鼓励”“一优先”来总括。
“三支持”:第一,国家支持疫苗基础研究和应用研究,促进疫苗研制和创新,将预防重大疾病的疫苗研制、生产和储备纳入国家战略;第二,国家制定疫苗行业发展规划和产业政策,支持疫苗产业发展和结构优化,鼓励疫苗生产规模化、集约化,不断提升疫苗的生产工艺和质量水平;第三,国家根据疾病流行情况、人群免疫状况等因素,制定相关研制规划,安排必要资金,支持多联多价等新型疫苗的研制。
“两鼓励”:国家鼓励疫苗上市许可持有人加大研制和创新资金投入,优化生产工艺,提升质量控制水平,推动疫苗技术进步;国家鼓励符合条件的医疗机构、疾病预防控制机构等依法开展疫苗临床试验。
“一优先”:对疾病预防、控制急需的疫苗和创新疫苗,国务院药品监督管理部门应当予以优先审评审批。
采访中,记者也了解到,国家在鼓励创新,开通各大优先审评审批渠道的同时,也进一步提升了疫苗的临床试验要求。
第十六条指出,开展疫苗临床试验,应当经国务院药品监督管理部门依法批准。疫苗临床试验应当由符合国务院药品监督管理部门和国务院卫生健康主管部门规定条件的三级医疗机构或者省级以上疾病预防控制机构实施或者组织实施。
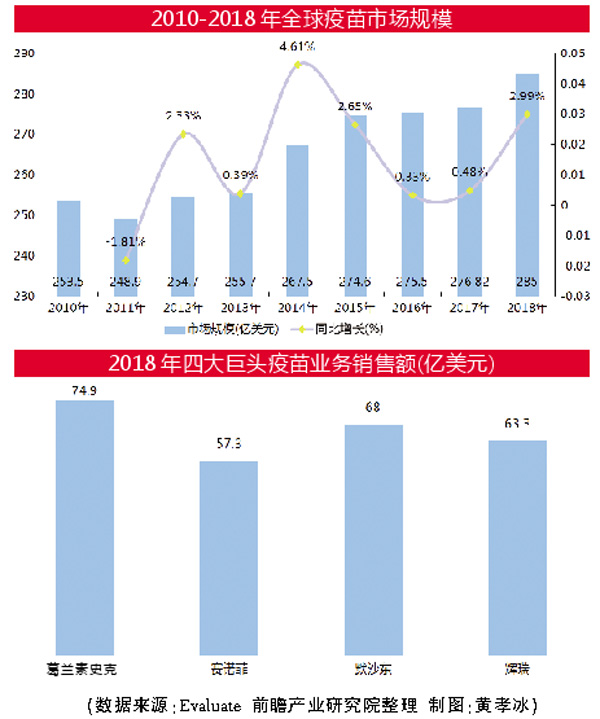
“疫苗行业是现代医药领域中一个较小的子行业,但又是生物医药领域中比较高端的细分领域。”数据显示,2020年疫苗市场规模预计在347亿美元,占药品市场的3.4%,年均复合增长率为5%。全球疫苗市场中四大疫苗生产巨头(葛兰素史克、默沙东、赛诺菲、辉瑞)占全球市场比重超过80%,中国疫苗市场规模仅为9%。
“国际市场最大的品类在中国均属于非免疫规划疫苗。2017年非免疫规划疫苗的批签发量呈现近20%的增长,如呼吸系统疫苗、人乳头瘤病毒、水痘和带状疱疹疫苗、轮状病毒疫苗等。”沈阳药科大学国际食品药品政策与法律研究中心主任杨悦认为,传染病防控需求的不断提升倒逼疫苗生产研发更新换代,未来多联苗会替代单苗,多价苗会替代低价苗。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






