严选药材供应商
发布时间:2019-09-30 16:23:13作者:殷鹏程 卢红委 张付轩来源:医药经济报
目前中药饮片生产违规行为常见于掺杂使假、违法加工、非法经营等。为避免供应商的违规操作对药品生产企业带来冲击,一方面需要依靠药品监管部门的监控,另一方面也需要药品生产企业的自行监管。本文从中药材供应商的管理角度,介绍药品生产企业如何把关中药材/中药饮片质量。
现状:种植加工缺乏规范约束
近年来中药材种植业发展迅速,各种问题也接踵而来。一方面,受地形限制的影响,西北、西南等地区难以机械化作业,种植效率低下。再加上药农的文化程度普遍偏低,田间管理较为粗放,使用化肥、农药无标准认定;另一方面,中药材种植栽培比农作物的栽培历史短,药材种源质量难保证,绝大部分中药使用历史不长,如地黄、丹参、板蓝根、人参栽培已有成熟的栽培品种,但分化、退化严重。
中药饮片质量优劣直接影响临床疗效,但在中药材加工方面,由于诚信缺失,使得中药饮片质量难以得到保障。现阶段饮片管理主要存在三方面的问题。
一是中药饮片企业缺乏标准化加工规范约束。我国中药材加工企业中,农村加工型企业居多,加工场所简陋,存在非法加工情况,问题的根源主要在:(1)生产质量人员短缺,专业素质不高,难以全程把关;关键管理人员短缺,变动频繁,质量管理体系运转艰难。(2)一些企业质量意识淡薄,即使通过GMP认证后,也难以按照要求生产。(3)中药材/中药饮片不检验就放行,质量把关流于形式。(4)贴牌包装,不按炮制工艺进行生产。中药饮片生产企业直接从市场或个体户手中购买饮片、半成品进行分包装或改换标签。(5)为应付检查,有的企业随意编造饮片生产记录、检验报告,以掩饰违法违规行为。
二是饮片生产企业规模小而散、集约度差,品种多批量小。相对于中成药产业,中药饮片产业起步晚、规模小,现有饮片生产工艺设备落后,不适应现代中药产业规模化、规范化生产需要。
三是饮片法制化管理有待完善。根据《药品管理法》第三十一条:“实施批准文号管理的中药材、中药饮片品种目录由国务院药品监督管理部门会同国务院中医药管理部门制定。”截止到2015年,已经实行文号管理的中药饮片有人工牛黄、青黛等70个品种。这些品种实际也未完全管理到位需要继续完善。
供应商审计:评价方式分步走
中药材质量直接影响中药产品制剂,其供应商的选择和管理就显得尤为重要。目前中药生产企业对中药材供应商评价方式主要是供应商审计。其流程主要如下。
1.审计前期准备
审计前,应先与供应商对接确定审计流程、所需材料等信息。对于首次审计需供应商提供:供应商基础信息评估结果、产品出厂质量标准、问题汇总等。对于周期性审计需提供的内容包括:前次现场检查提出的问题、建议及纠正报告、定期评估结果、问题汇总等。审计前可召开审计预备会议,确定供应商现场审计流程、时间安排、检查项目、文件清单、人员分工情况等。
2.现场审计
①确认供应商资质 先确认供应商资质,合格标准为确认供应商的公司基础信息资料、人员机构设置等各项真实性及有效性无误,且营业执照、生产许可证、经营许可证等均在有效期内。若供应商提供的检验报告有法定部门检验报告,应提供法定部门检验报告。企业供应商管理员应在国家或省药品监管部门网站上核对和确认供应商。
②现场检查 现场检查是最有效、最直接评估供应商质量体系的重要手段,主要是核实供应商的质量体系、机构组织、设备设施等是否能够保证持续生产出符合质量标准的产品;供应商是否真实地进行了相关的生产并如实进行记录等,现场发现供应商体系的缺陷漏洞。
现场检查要点主要为:企业组织机构和人员的管理情况,如审核供应商质量保证体系图,核对供应商人事情况。企业质量管理部门负责人资质确认及相关材料审核等;再有,仓储、设备和设施管理情况,包括仓储区是否有足够的空间确保分库存放待验、合格、不合格、退货或召回的中药材。仓库相应库区温、湿度设定是否符合要求等。生产管理情况,如是否制定中药材炮制加工的生产工艺的操作规程;还有更换品种、同品种更换批次是否对生产环境、设备等进行彻底清场,避免出现混淆和差错;另外,处理后的中药材是否直接接触地面,是否露天干燥。药材洗涤是否使用流动的工艺用水等。在对饮片供应商检查时,应看其是否建立符合国家标准的企业标准(包括原药材标准、饮片标准)。根据现行有效的产品质量标准及检验操作规程核查是否具备相应检测设备、仪器等。其它审计项目还包括前次审计缺陷是否整改完毕、物料质量反馈整改措施是否到位等。
③审计报告 资格审查结束后,形成审计报告,供应商进行缺陷项整改,同时可以进行试用,供应商在规定期限内完成整改,最后评价合格后,由质管部批准成为正式供应商。现场审计情况描述、需要整改的项目、审计结论,审计小组人员签名。对于审计报告中的关键缺陷和重要缺陷,应评估其对公司产品质量的影响。对于临时性审计报告,也应评估。
④判定标准 审计组长根据发现的缺陷,综合小组其他成员的意见,确定初步审计结论,合格或者不合格,整改后复审。同时供应商应对缺陷的整改提出相应的要求,并明确后续工作,如执行CAPA等。
具体来讲,如何判定为合格,主要在于无关键缺陷项目,重要缺陷≤2项,且在经药品生产企业认可的整改期限内整改完毕。重要缺陷必须在一个月内整改结束,特殊情况下由于客观原因不能在规定时限内完成,需在整改报告中明确说明并明确最终整改期限;一般缺陷≤30项。若违法下述其中一条,即判定为不合格:存在关键缺陷;重要缺陷≥3项;出现弄虚作假的情况。整改后复审判定标准(符合其中一条需进行整改后复审):一般缺陷>30项;重要缺陷≤2项,但有1项以上缺陷不能在药品生产认可的整改期限内整改完毕;供应商承诺对关键缺陷进行整改并明确期限。
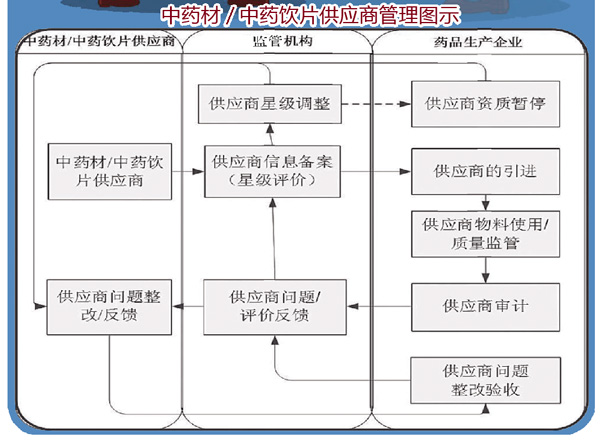
建议
中医治病求本,同理,中药材的质量应从源头抓起。加强道地药材的种植管理,形成产业联盟,优势互补。国家层面应加强中药材市场的监管,采取优胜劣汰,对违规供应商坚决予以取缔。而中药生产商作为中药材的使用方,应该加入监管队伍中,对公司采购的中药材和中药饮片的供应商进行分类。通过溯源分级的管理体系倒逼中药材供应商严格执行标准;建立企业内部诚信评价机制,对于周期审计问题较少,且按照GMP进行生产的,检查频率可相对降低;对于发现不符合要求且有作假、掺假的,取消供货资格。并且国家可建立中药材供应商信息化平台,梳理并公示国内所有工商注册的供应商企业目录。采用信用等级评价管理制度,进行信用等级区分。对于审计检查出的原则性问题,如批量生产记录作假、不具备检验条件等,直接降低该供应商信用等级,避免其他企业接触该供应商。总之,中药饮片的生产企业如想赢得市场,必须严把质量关。
(作者来自扬子江药业集团江苏龙凤堂中药有限公司)
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






