搅局者入场 冷门OAB机会来了
发布时间:2019-04-15 16:09:06作者:李勇来源:医药经济报
膀胱过度活动症(overactive bladder,OAB)是一种以尿急症状为特征的综合征。OAB给患者造成多方面影响,尤其是严重影响睡眠、出行和社交,不少患者还会出现抑郁、焦虑等心理问题。
流行病学调查数据显示:我国18岁以上人群OAB总体发病率为5.9%,而随着年龄的增长其发病率逐步增高,40岁以上的人群发病率可达11.3%。不过,我国OAB就诊率较低,仅有53%。口服药物是目前OAB最基本和常用的治疗手段,最常用的药物为抗胆碱能药物、β3肾上腺素受体激动剂(见表1)。
目前国内临床主要使用抗胆碱能药物。尽管疗效确切,但抗胆碱能药物个体选择性较大,且具有较大副作用和禁用人群。相比之下,作用机制不同的β3肾上腺素受体激动剂,在疗效和副作用方面具有自身优势,2017年米拉贝隆的进口上市,有望改变国内长期以来低迷的OAB用药市场格局。
中美日PK
表现悬殊,
但皆为爬行式增长
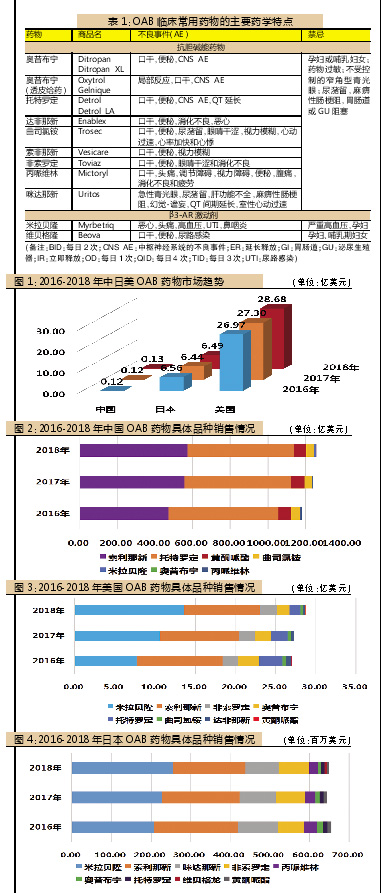
美国、中国、日本是全球前三大医药市场。根据IQVIA数据,过去3年(2016-2018年)这三个国家OAB用药整体市场分别为:美国为26.97亿、27.30亿、28.68亿美元;中国为0.12亿、0.12亿、0.13亿美元;日本为6.56亿、6.44亿、6.49亿美元(见图1)。由此可见,中国OAB用药市场远低于美国和日本。而从过去两年(2017-2018年)三个国家OAB用药整体市场增长率来看:美国为0.65%、4.23%,中国为4.84%、1.83%,日本仅为-1.71%、0.74%,都远低于其他类别药物增幅。
就具体品种而言,过去3年中国OAB用药市场中,索利那新和托特罗定两种药物占据OAB市场90%的份额,二者平分秋色。索利那新在国内样本医院销售金额分别为470万、558万、572万美元;托特罗定销售金额分别为583万、565万、566万美元;其他几种药物共享剩余10%份额(见图2)。
美国OAB用药市场则不同。在过去3年,米拉贝隆、索利那新、非索罗定、奥昔布宁、托特罗定这5种药物销售金额都达到了亿美元级别。其中,处于市场第一梯队的是米拉贝隆和索利那新。米拉贝隆销售金额分别为7.70亿、10.60亿、13.66亿美元,呈现快速增长趋势,该产品在2018年占据美国OAB用药市场近半壁江山(47%)。而索利那新销售金额开始出现下滑趋势,分别为10.69亿、9.88亿、9.39亿美元。处于市场第二梯队的是非索罗定、奥昔布宁和托特罗定。非索罗定销售金额分别为1.95亿、1.91亿、2.13亿美元;奥昔布宁销售金额分别为2.65亿、2.01亿、1.54亿美元;托特罗定销售金额分别为2.84亿、2.09亿、1.38亿美元。处于市场第三梯队的曲司氯铵、达非那新、黄酮哌酯,过去三年销售金额仅为千万或者百万美元级别。(见图3)。
与美国市场类似,过去3年日本OAB用药市场中,米拉贝隆、索利那新也是最畅销的药物:米拉贝隆销售金额分别为2.06亿、2.28亿、2.55亿美元;索利那新销售金额分别为2.14亿、1.94亿、1.82亿美元。两种药物增长趋势与美国市场类似:米拉贝隆在稳步增长,而索利那新在缓慢下降。此外,咪达那新、非索罗定、丙哌维林销售金额都达到了千万美元级别,而奥昔布宁、托特罗定、维贝格隆销售金额仅在百万美元级别(见图4)。
新药研发
有点冷,3个Ⅱ期项目打前锋
OAB用药的新药研发比较冷,目前最快的是3个达到Ⅱ期临床的项目。
美国Velicept Therapeutics公司正在开发的solabegron处于临床Ⅱ期试验中。solabegron是一种高选择性β3-肾上腺素受体激动剂。该项目由GSK发现并首先开发,随后被AltheRx收购,后者于2015年与Velicept合并。
日本大鹏制药(Taiho Pharmaceutical)正在开发的环己烯脂肪醇衍生物TAC-302,目前也处于Ⅱ期临床。
处于Ⅱ期临床的还有韩国Dong-A ST公司的DA-8010项目。
国内市场格局
抗胆碱能药物唱主角
OAB与膀胱充盈过程中膀胱逼尿肌不自主收缩有密切关系,而这种收缩主要通过激动逼尿肌上分布的M受体介导。M受体分为M1-M5共5个亚型,在膀胱逼尿肌主要分布M2(67%)和M3(33%)两种亚型,M2受体的密度虽远大于M3受体,但在功能上M3受体更为重要,它介导膀胱的直接收缩。通过抗胆碱作用,抗胆碱能药物可减少逼尿肌不自主收缩。
在美国销售额过亿级别的OAB用药中,除了米拉贝隆为β3肾上腺素受体激动剂,其余的索利那新、非索罗定、奥昔布宁、托特罗定这4个药物都属于抗胆碱能药物。
奥昔布宁:首个获批OAB药物
奥昔布宁是首个被批准用于治疗OAB的药物,目前有多种剂型获得批准上市销售。
国内已上市的口服剂型包括:盐酸奥昔布宁胶囊(由天津药物研究院药业、上海爱的发制药生产销售)、盐酸奥昔布宁缓释片(由南京亿华药业生产销售)、盐酸奥昔布宁口服溶液(由珠海联邦制药中山分公司生产销售)。奥昔布宁透皮贴剂由美国华生制药(Watson Laboratories)进口上市。在美国市场,奥昔布宁凝胶也获得批准上市销售。
奥昔布宁口服制剂目前国内企业暂无申报和进行生物等效性试验。奥昔布宁透皮贴剂国内暂无企业按新注册分类申报,江苏康倍得药业、北京康倍得医药2家企业正在进行生物等效性试验。
托特罗定:老牌一线用药
托特罗定是治疗OAB的一线药物,目前临床应用最广,是专门为治疗OAB而研发的药物。托特罗定是一种竞争性抗毒蕈碱药物,能同时阻断M2和M3受体与乙酰胆碱的结合。
国内市场上,托特罗定有多种口服剂型:酒石酸托特罗定缓释片,由南京美瑞制药生产销售;酒石酸托特罗定片由6家公司生产销售(成都迪康药业、南京美瑞制药、南京正科医药、瀚晖制药、鲁南贝特制药、深圳市海滨制药);酒石酸托特罗定分散片由鲁南贝特制药生产销售;酒石酸托特罗定胶囊由安徽环球药业生产销售。另外,托特罗定其他盐型富马酸托特罗定片由四川科伦药业生产销售。
托特罗定目前国内企业暂无按照新注册分类申报和进行生物等效性试验。
索利那新:新一代一线用药
索利那新为新一代选择性M受体拮抗剂,对平滑肌上的M3受体有高选择性,为OAB治疗的一线用药。
国内市场上,琥珀酸索利那新片国产有四川国为制药和齐鲁制药2家生产,安斯泰来为进口上市销售。
琥珀酸索利那新片目前国内3家企业按照新注册分类申报,分别为武汉人福利康药业、杭州华东医药集团浙江华义制药、浙江海正药业,无其他企业进行生物等效性试验。
[延伸]
国内上市的其他抗胆碱能药物还有曲司氯胺和丙哌唯林。
曲司氯胺国产有片剂1家(扬子江药业)和胶囊2家(舒泰神北京、寿光富康制药),进口药曲司氯铵片由MEDA Pharma上市销售。
丙哌唯林国产有片剂4家(贵州神奇药业、天津太平洋制药、康美药业、石家庄市华新药业),进口药盐酸丙哌维林缓释胶囊为APOGEPHA Arzneimittel的产品。
这两个药物目前在国内都暂无企业按照新注册分类申报和开展生物等效性试验。
非索罗定:
国外已上市、国内未上市
非索罗定是一种竞争性M受体拮抗剂。由于与托特罗定具有相同的活性代谢产物5-HMT,因而非索罗定被认为是托特罗定的新一代药物。
非索罗定缓释片由辉瑞开发,2007年在欧盟获得批准,2008年、2013年分别在美国和日本批准上市。目前尚未在国内上市,国内也尚无企业按照新注册分类申报和开展生物等效性试验。
[延伸]
除了非索罗定,目前国外已上市、国内尚未上市的抗胆碱能药物还有达非那新、咪达那新。
达非那新是诺华研发的选择性M3受体拮抗剂,2005年首次在美国上市。目前在国内尚无企业按照新注册分类申报和开展生物等效性试验。
咪达那新是一种高效抗胆碱能药物,对M3和M1受体具有高选择性。咪达那新片及口崩片,由日本小野药品工业株式会社与杏林制药联合开发,2007年在日本获得批准上市。目前在国内尚无企业按照新注册分类申报;生物等效性试验方面,昆明积大制药已完成,辅仁药业尚未开始招募。
搅局者能量
米拉贝隆
将改变国内市场格局
有别于抗胆碱能药物减少逼尿肌不自主收缩的作用,β3肾上腺素受体(β3-AR)激动剂使膀胱平滑肌松弛。米拉贝隆是第一个用于治疗OAB的β3-AR激动剂。
国内市场上,安斯泰来进口药贝坦利(米拉贝隆缓释片)于2017年批准上市。目前国内暂无企业按照新注册分类申报,杭州华东医药集团浙江华义制药的米拉贝隆缓释片人体生物等效性试验正在招募中。
维贝格隆是另一个β3-AR激动剂,在日本于2018年9月获得批准上市,最早由默沙东研发,目前在日本由杏林制药和Kissei上市销售,商品名为Beova(维贝格隆片)。维贝格隆目前在国内暂无企业申报和进行人体生物等效性试验。
由于OAB的复杂性,临床容易误诊,再加上患者认知度不高,就诊率较低。因此,虽然目前国内OAB药物整体市场不大、增速缓慢,但潜力巨大。
2017年米拉贝隆在中国批准上市,其进入市场可谓搅局者。从美国和日本OAB药物市场情况看,米拉贝隆占据了较大的市场份额,因此,米拉贝隆或将改变国内以传统抗胆碱能药物为主的市场格局。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



