血小板减少症用药 “上新”与“爆款”
发布时间:2019-03-21 15:09:39作者:灯芯来源:医药经济报
血小板减少症用药“上新”与“爆款”
2月6日,美国FDA批准赛诺菲子公司Ablynx的纳米抗体药物Cablivi用于获得性血栓性血小板减少性紫癜(aTTP)成人患者的治疗。Cablivi是FDA在2019年批准的首个血小板减少症新药,将给广大aTTP患者带来福音。
血小板是一类小的盘状无核细胞,存在于血液循环中,在止血、伤口愈合、炎症反应、血栓形成及器官移植排斥等生理和病理过程中有着重要作用。血小板减少是引起不正常出血最常见的原因。
【新药】
2019年FDA批准的第二款新药即为血小板减少症药物。回顾2018年FDA批准的新药,其中包含3个血小板减少症新药。这4个药物作用机制各不相同,都标志着血小板减少症新药研发迎来重大突破。
Cablivi:全球首个纳米抗体药物
获得性血栓性血小板减少性紫癜是一种危及生命的、基于自身免疫的凝血障碍,特征是遍布全身的小血管中形成大量的血凝块,导致严重的血小板减少症(血小板计数极低)、微血管病变性溶血性贫血(因溶血性破坏导致红细胞损失)、组织缺血(部分机体血液供应受限)和广泛的器官损害,尤其是大脑和心脏。
Cablivi的活性药物成分为Caplacizumab,是一种强效选择性双价抗血管性血友病因子(vWF)纳米抗体,早在2009年被美国和欧盟授予孤儿药地位。Caplacizumab能够阻断超大vWF多聚体(ULvWF)与血小板的相互作用,因此针对血小板聚集和随后发生的微小血凝块(microclot)的形成和积累具有立竿见影的效果。在aTTP患者中,这种微小血凝块能够导致严重的血小板减少症、组织缺血和器官功能障碍。Cablivi在2018年8月获得欧盟委员会批准上市,Cablivi在2018年的全球销售额为0.04亿欧元(约4.54百万美元)。
Mulpleta和Doptelet:血小板生成素(TPO)受体激动剂
2018年7月31日,FDA批准盐野义的Mulpleta(Lusutrombopag)上市,用于治疗计划接受手术的成人慢性肝病(CLD)患者的血小板减少症。
2018年5月21日,FDA批准AkaRx的新药Doptelet(Avatrombopag)片剂用于治疗计划接受医疗或牙科手术的慢性肝病(CLD)成人患者的血小板减少症。
Mulpleta与Doptelet都是每日口服给药的小分子血小板生成素(TPO)受体激动剂,在安全性、功效和给药方便性方面非常相似。
在CLD患者中经常可观察到血小板减少,研究表明它在肝硬化患者中发生比例高达78%。有血小板减少症的CLD患者每年医疗费用比无血小板减少的CLD患者高出3倍。当血小板计数低于5万/微升时,更会加剧手术或外伤出血,并且使常规诊断程序和患者护理明显复杂化。因此,这一领域迫切需要新的治疗选择。同时,有慢性肝病的成年患者由于各种原因需要进行手术,能够为患者提供这种新的口服治疗,就不必依靠血小板输注。
Tavalisse:慢性免疫血小板减少性紫癜(ITP)的新选择
2018年4月17日,FDA批准Rigel公司的Tavalisse(Fostamatinib disodium hexahydrate)治疗先前治疗无效的成人慢性免疫性血小板减少性紫癜(ITP)。
Tavalisse是一种口服的脾脏酪氨酸激酶(SYK)抑制剂,是目前唯一被批准上市的SYK抑制剂。这种SYK抑制剂可通过阻止血小板的破坏来应对疾病的潜在自身免疫原因,为成年慢性ITP患者提供了一个重要的新的治疗方案。
【畅销药】
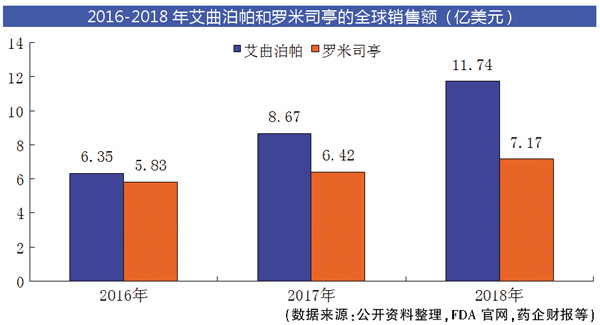
目前全球畅销的血小板减少症药物有诺华的艾曲泊帕(Promacta/Revolade)和安进的罗米司亭(Nplate),两者都是促血小板生成素受体激动剂(TPO-RA)类药物。
艾曲泊帕由英国葛兰素史克研发并于2008年11月获得美国FDA批准在美国上市,现已卖给诺华,并于2017年12月在中国获批上市。罗米司亭于2008年获得美国FDA批准在美国上市,2017年获得欧盟委员会批准上市。
艾曲泊帕和罗米司亭2018年的全球销售额分别为11.74亿美元和7.17亿美元,同比增长35%和12%。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



