全景大数据 FDA批准新药创纪录
发布时间:2019-01-31 18:30:58作者:李轩(中国医药工业研究总院来源:医药经济报
全景大数据FDA批准新药创纪录
2018年批准新药数量、孤儿药数量皆创近20年来新高
FDA的药物评价与研究中心(Center for Drug Evaluation and Research, CDER)每年都审批数以百计的药品。其中一小部分称之为“新药”(Novel Drugs),通常是指用于之前未能满足的医疗需求或者非常有助于促进医疗保健和公众健康的创新性药品。FDA对这些新药以新分子实体(New Molecular Entities,NMEs)的身份进行审评,这些药物含有以前没有被FDA批准的活性成分,以单一成分或组合药物的一部分给予患者新的治疗。
59个新药
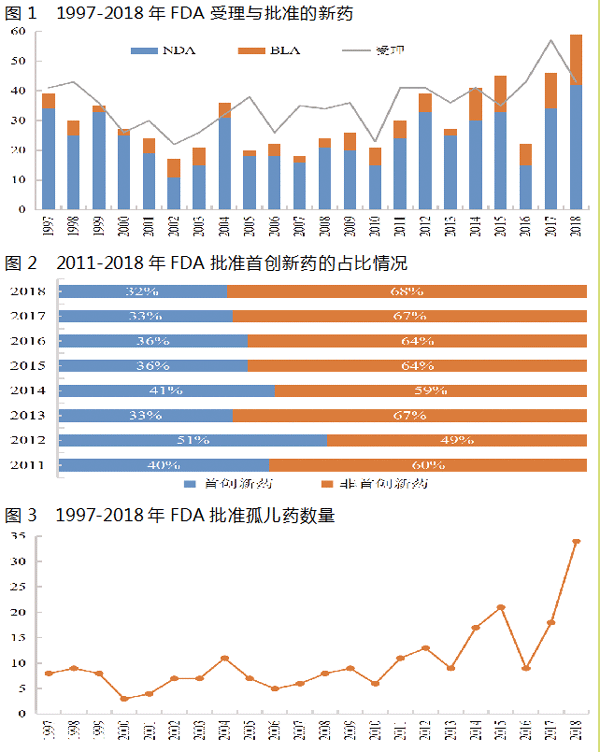
2018年,FDA共批准了59个新药(即NMEs),其中新药申请(New Drug Applications,NDAs)42个,约占年度批准新药的71%;生物制品许可申请(Biologics License Applications,BLAs)17个,约占年度批准新药的29%,不包括生物制品评价与研究中心(Center for Biologics Evaluation and Research, CBER)批准的疫苗、过敏性产品、血液和血液制品、细胞与基因治疗产品等。2018年批准新药数量创近20年来的新高(具体情况见图1)。
19个首创新药
2018年,FDA认定19个新药为首创新药(First in Class),约占年度批准新药的32%。首创新药通常具有不同于现有治疗药物的作用机理,是衡量药品创新性的一个重要指标(2011-2018年占比情况见图2)。
34个孤儿药
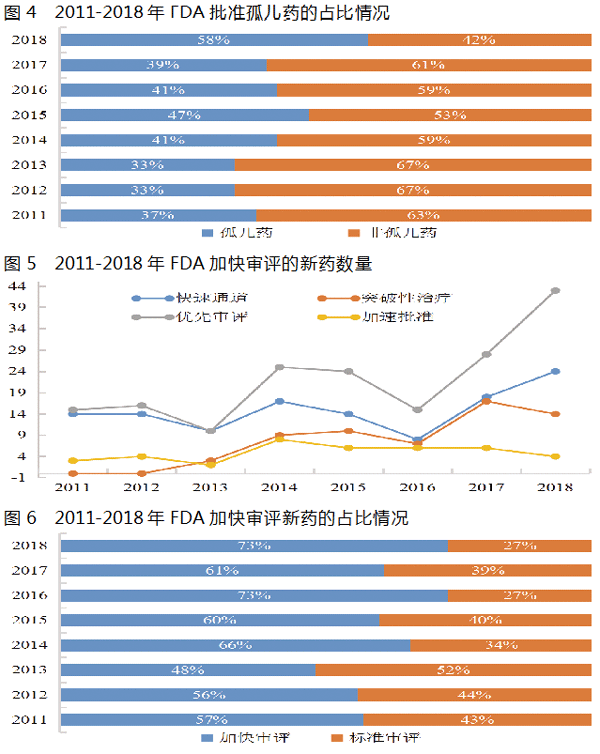
在美国,罕见病界定为影响人数少于20万的疾病,这些疾病的患者通常很少或没有可选择的治疗药物。2018年,FDA批准34个孤儿药,创近20年新高,约占所有批准新药的58%(2011-2018年占比情况见图4)。自1983年孤儿药法案实施以来,FDA共计批准300个孤儿药,年均约8个(1997-2018年批准情况见图3)。
73%加快审评获批
FDA通过多种监管途径提高新药审评效率,加快新药研发和批准速度。这些加快审评途径包括:快速通道(Fast Track)、突破性治疗认定(Breakthrough Therapy)、优先审评(Priority Review)和加速批准(Accelerated Approval)。这些途径使用中,FDA采取了一系列措施,如促进CDER人员和药物研发者之间更多交流、程序设计更大灵活性,以及缩短新药申请审批时间等。
2018年,FDA批准新药的方式中,16个为标准审评,约占所有批准新药的27%;获得优先审查、快速通道、突破性治疗、加速批准的新药分别为43个、24个、14个和4个,各约占所有批准新药的73%、41%、24%和7%;获得一种及以上加快审评资格的新药为43个,约占所有批准新药的73%(2011-2018年具体情况见图5、图6)。
TOP3领域占近7成
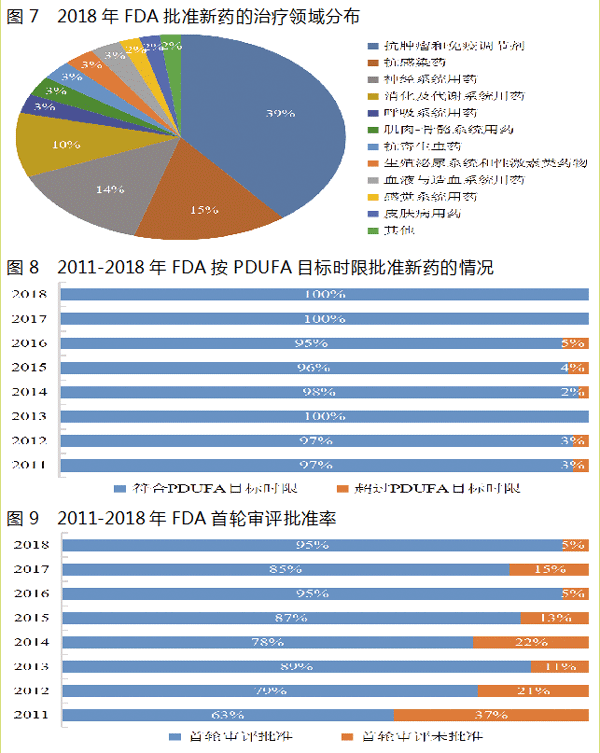
从治疗领域来看,2018年FDA批准的新药中,抗肿瘤药23个、抗感染药9个、神经系统用药8个,位居年度批准新药治疗领域的前三,分别约占年度批准新药的39%、15%和14%,共约占年度批准新药的68%(具体情况见图7)。
从剂型来看,2018年FDA批准的新药中,片剂24个、注射剂23个、胶囊剂7个,位居年度批准新药剂型的前三,分别约占年度批准新药的41%、39%、12%。可见,注射剂、片剂占绝大多数。
100%时限内获批
根据《处方药申请者付费法案》(Prescription Drug User Fee Act,PDUFA),FDA对申请药品、生物制品上市的制药企业收取相应的费用,以使其在预定目标时限前完成相关审评工作。纵观2018年FDA新药批准情况,CDER能够确保100%的新药是在目标时限的当天或之前获得批准(2011-2018年批准率情况见图8)。
首轮审评批准率95%
2018年,FDA新药审批程序平稳运行,首轮审评(First Cycle)批准率约为95%,这意味着对56个新药申请没有被要求提供额外信息,避免了这些新药的延期批准和新一轮的审评(2011-2018年批准率情况见图9)。
美国率先批准率71%
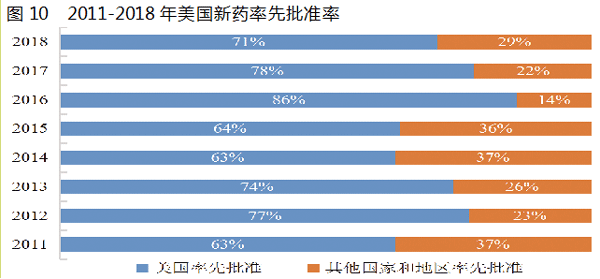
FDA与其他国家和地区同等监管机构的监管流程不尽相同,对新药首先在美国获批与首先在其他国家和地区获批的情况进行比较是衡量FDA审批效率的又一种指标。2018年,FDA批准新药中有42个(约71%)在美国获批早于在其它国家和地区获批(2011-2018年新药率先批准率见图10)。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



