2019全球医药四大看点
发布时间:2018-12-26 11:14:58作者:Amy Brown,Jonathan Gardner,Edwin Elmhirst 编译/廖联明 来源/Evaluate来源:医药经济报
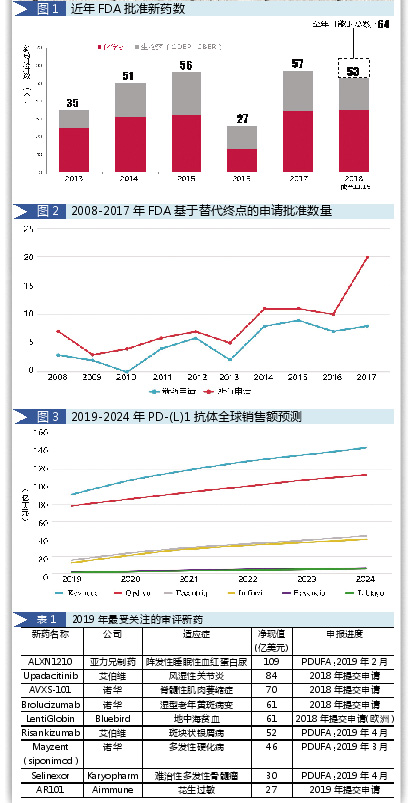
美国医药行业迎来了一个较为宽松的监管环境。过去5年中,FDA批准的药物数量有4年远远高于平均水平。2018年,FDA批准的新药数又有望创下新纪录。
FDA数据显示,新药申请的数量也有所增加,而获批药物的增幅更加明显。这种涨势在很大程度上反映了FDA为更快更高效地将新药推向市场所做的努力。不过,也有许多人认为,这一数字的跃升是新药审评标准降低的结果。
看点1
新药审评:宽松还是收紧?
这种宽松的环境在明年基本会得以延续。对新药安全性的高度担心可能会迫使监管机构开始更严格地进行药物审评,但严格到什么程度无法预测。一个更长远的问题是,这一趋势对进入市场的药品质量意味着什么?
“本轮牛市在很大程度上是由超级宽松的FDA推动的,这使得药企和投资公司甘于冒险投资于新药。”一位投资者指出。或许,印证新药获批门槛降低的另一个信号是保险公司对新药设定的支付条件越来越严格。FDA也许会说其基本职责是确保新药的安全性,而批评者认为,随着新药上市速度越来越快,药物安全性开始被忽视了。
不可否认的是,医药行业正在使用各种快速审评策略加快新药上市以增加收益流,FDA基于替代终点批准上市的药物一直在增加。
总的来说,明年制药行业的监管环境会是一大看点。但如果激增的新药申请反映的是这个行业被推进得过快——在某些情况下不仅会影响到药品使用的有效性和安全性,也会因为这些“拔苗助长”的新药商业前景不好而影响投资者的热情,宽松的监管环境反而可能会损害医药行业长期的发展。
明年,免疫检查点抑制剂会继续成为关注焦点。从这个被寄予巨大期望的领域的新药审评速度,也可以嗅出宽松的监管环境是否会发生转变。在过去几个月里,有几个抗PD-(L)1抗体的试验数据不及预期,未能将快速审评资格转化为最终的申请获批。
有5种免疫检查点抑制剂已获暂时性批准,用于治疗晚期尿道上皮癌。2018年进行的几个大型试验并未能确立其明确的治疗获益,但FDA对此仅发布了安全警告。此外,胃癌治疗的随访结果也同样令人失望,小细胞肺癌的研究结果也是如此,但免疫检查点抑制剂的相关适应症仍未被撤销。
如果FDA开始撤销这些批准,对制药行业和投资者而言将无异于一只震撼弹。事实上,欧洲药品管理局(EMA)的耐心已经开始逐渐消失,其要求百时美施贵宝(Bristol-Myers Squibb)与阿斯利康(Astrazeneca)就各自的肺癌药物Opdivo和Imfinzi提供进一步证据,以确定其确切疗效。EMA也拒绝批准BMS的Opdivo/Yervoy在肾细胞癌上的联合使用,因为其认为这两个药的独自疗效不能推导出来,而FDA对此并不是很严格。
FDA将临床需求大的药物加快推向市场,确实给许多疾病治疗领域带去了积极的影响。但是,患者可能需要承受药物毒性的风险,并对疗效并不好的新药抱有错误的希望。因此,也有声音抱怨美国监管机构变得过于宽松,那些通过快速审评通道上市的新药并没有按照法规要求进行上市后的验证性临床试验。
看点2
IO焦点:联合用药能否有所突破?
也许用不了多久风向就会改变,药物的审批可能变得更加严格。
一个备受关注的审评结果将在明年5月公布,是BMS将Opdivo和Yervoy联用于肿瘤基因突变负荷高的肺癌患者一线治疗的申请。由于肿瘤基因突变负荷作为生物标志物的临床意义还远未确定,因此这一决定很可能会考验FDA对于审批的宽松程度。
上个月初,FDA批准了罗氏(Roche)的Tecentriq、Avastin联合化疗的三药联合方案用于多个适应症。
不过,这两家公司的产品都不太可能对默沙东(Merck)的领头羊地位造成太大影响。默沙东及其竞争对手明年如何扩大患者群也将受到密切关注。
一些重要的试验数据将于明年公布,包括Keynote-426,验证Keytruda与化疗联合用于肾细胞癌患者的一线治疗的效果,相关数据将于近几个月公布。BMS也将公布两项肺癌一线治疗的试验结果:第二阶段Checkmate-227试验的数据和Checkmate-9LA试验的数据将分别于明年上半年和下半年公布。
BMS还将在明年1月发布Opdivo的长期随访数据,这也将影响该药的市场预期。当前有预测指出,Opdivo的销售增长将在明年晚些时候停滞,到2020年其销售额可能会下降。
目前市场上已有6种抗PD-(L)1抗体,未来几年出现价格竞争的可能性也不容忽视。
第一波免疫检查点抑制剂的巨大成功促使业内对后续肿瘤免疫靶点的期望达到顶峰。然而,2018年公布的一系列令人沮丧的数据显示,现有药物要继续发扬光大远非易事。
“对于抗肿瘤领域来说,这是非常令人失望的一年。业界在联合用药研究上的投资是巨大的,但epacadostat的失败让我们对整个IDO抑制剂的研究都感到失望。美国临床肿瘤学会年会(ASCO)和欧洲临床肿瘤学会年会(ESMO)上发表的数据也同样非常令人失望。”生物技术领域投资者Brad Lonca表示,“不过,有很多引人注目的研究正在进行中,所以我相信明年的情况一定会有所好转。”
要找到合适的肿瘤免疫药物联合治疗方法仍然很困难,但是各方仍然对此抱有极大的期望。针对Sting agonism、Tim-3、Tigit和Lag-3等靶点的药物在等待更多数据,而细胞因子领域也还保有众多追随者。
Nektar和BMS的新型IL-2细胞因子免疫激动剂NKTR-214的疗效并不理想,已经打击了市场信心。如果礼来(Eli Lilly)的聚乙二醇化人白细胞介素-10 (pegilodecakin)能给出漂亮的中期数据,投资者的兴趣可能会重新燃起。两个肺癌试验将在明年下半年公布结果:Cypress 1正在研究pegilodecakin联合Keytruda用于PD-L1(>50%)高表达的非小细胞肺癌患者的一线治疗;Cypress 2正在研究PD-(L)1-野生型或PD-L1低表达患者(1-49%)的二线治疗。
溶瘤病毒是明年肿瘤免疫领域另一个值得关注的联合用药选项,此前围绕该技术达成了一系列交易。安进(Amgen)的Imlygic联合Keytruda治疗黑色素瘤的Ⅲ期大型试验将于明年12月得出结果,可能有助于评估这些治疗方案的有效性。
看点3
细胞疗法:漂亮翻身还是神话破灭?
血液肿瘤治疗领域明年也有望得到进一步发展。在美国血液学会年会(ASH)上,从来自Immunogen、ADC Therapeutics和再生元(Regeneron)等公司的最新数据看,明年抗体偶联药物和双特异性抗体治疗白血病和淋巴瘤的结果值得关注。
“血液系统肿瘤的研究数据非常惊人,有很多令人振奋的结果。我认为,明年将是细胞疗法非常激动人心的一年。”Loncar表示。
在ASH上,几个针对BCMA靶点的 CAR-T项目进展顺利;多发性骨髓相关抗原被认为是CD19之后的下一个重要靶点。
尽管如此,CAR-T的商业前景仍需付出很大努力才能令投资者重新燃起希望。今年,由于吉利德(Gilead)的Yescarta和诺华(Novartis)的Kymriah市场表现低于预期,CAR-T相关的研究已大幅缩减规模。2019年,CAR-T产品的季度销售数据将继续受到密切关注。
让人惊讶的是,2018年CAR-T药物平淡无奇的表现并没有影响资本市场对实验阶段细胞疗法的热度——例如,虽然产品仍处于非常早期的研发阶段,Allogene和Autolus等公司还是以相当高的估值上市。
相关研究进展也将在2019年受到密切关注,尤其是异体细胞疗法。生物技术领域投资者Wilson Cheung指出,Atara有一个Ⅲ期试验tabl -cel,将在明年上半年公布数据,这将是第一个通用型T细胞免疫疗法的关键结果。
许多人也希望看到自体细胞治疗领域的研究进展。一大关注点就是新基医药(Celgene),投资者非常希望看到该公司并购Juno的90亿美元没有被浪费。还有很多事情需要证明,尤其是该公司声称其CAR-T产品与其他同类产品相比在安全方面有更明显的优势。
新基医药最受重视的CAR-T项目JCAR017(liso-cel)将在明年从Transcend-NHL研究中获得注册数据,进而寻求在2020年年中获得FDA的上市批准。这个进度已经远远晚于2018年Juno的乐观预估。
从ASH来看,新基医药似乎将重心转移到CLL上,这一适应症并非CAR-T项目的研究热点。但JCAR017被认为是新基医药未来最重要的增长点之一,因此,如果这个新药的上市步伐被进一步延迟,将给这家陷入困境的大型生物科技公司带来更大的压力。
CAR-T疗法并不是目前唯一令人失望的新技术。基因疗法的旗舰产品——Spark公司的Luxturna上市慢于预期,且Alnylam公司的RNAi淀粉样变疗法Onpattro的早期研究数据也并不理想。
明年还将有两种基因疗法上市,分别是Bluebird的Lentiglobin和诺华的AVXS-101。投资者很快就会知道,此前上市产品未能大获成功是归于异常表现,还是表明要对此类新技术应用持有更保守的预期。
看点4
生物类似药:原研药企能否继续捍卫市场?
小分子药物也有望在明年引起关注。今年,Loxo Oncology与拜耳(Bayer)的larotrectinib (商品名Vitrakvi)获得批准,这可能掀起针对广泛基因突变的高度选择性肿瘤疗法的新浪潮。投资者和竞争对手也将关注患者对于Vitrakvi令人瞠目结舌的高价会如何反应。
“无成药性的靶点将会有所突破。”Nextech投资公司合伙人Thilo Schroeder表示,“KRAS、PI3K、p53等致癌基因,将在未来5年得到解决。现在技术已经成熟了,我们有一些非常不同的化合物即将投入临床,这些已经得到了验证。”
无论是肿瘤免疫、细胞疗法,还是小分子药物,有一件事是肯定的——明年抗肿瘤领域仍将是制药行业最热门的板块之一。
生物类似药也将被重点关注,尤其是在美国。在这个非常有利可图的市场里,还没有多少企业试水。
Neulasta的原研保卫战可能是2019年值得关注的市场焦点,迈兰(Mylan)已经推出了生物类似药Fulphila,Coherus公司也计划在明年初推出生物类似药Udenyca。原研药企有能力与保险公司谈判并阻止生物类似药列入医保名单,这是其在美国药品市场保持影响力的原因,同时也被指责是美国生物类似药发展缓慢的“罪魁祸首”。
但美国降低药品价格的政治意愿正在增强,因此这些成本较低的生物类似药所处的环境应该不会变得更糟。如果立法者在推动美国医疗体系的结构性改革上取得任何进展,苦苦挣扎的生物类似药行业可能会成为首批受益者之一。
编译/廖联明 来源/Evaluate
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



