高值药品准入医保, 如何三方共赢
发布时间:2018-11-28 16:50:41来源:医药经济报
今年8月,用于严重哮喘患者的Nucala(Mepolizumab,美泊利单抗)与全球首个免疫哨卡抑制剂、用于转移性黑色素瘤的Yervoy(Ipilimumab,伊匹单抗)先后通过新药审查,纳入中国台湾地区的高值创新药品健保目录。
其中,Nucala通过降低血嗜酸性粒细胞水平以降低严重哮喘发作,该药仅供皮下注射使用,每4周一次于上臂、大腿或腹部皮下注射100mg。Nucala每瓶100mg,定价34,245元新台币,患者一年药费为410,940元新台币。该药在台湾地区每年用药人数约为100~200人。Yervoy(5mg/ml,10ml)为单一疗程用药,每隔3周治疗一次(以静脉注射的方式给药3mg/kg),总共治疗4次。该药单价为102,823元新台币,每人总疗程药费为1,645,168元新台币,台湾地区每年用药人数约为80人。
可见,创新药品,尤其是生物制剂单价高昂、适用人群极少,同样增加了台湾地区健保单位的财务负担。然而,毋庸置疑的是,创新药品入市有利于满足病患未满足的医疗需求,但如何创造药企、医保、病患三方共赢的局面,是一个值得深究的问题。
从上市到临床,跨过三道关
一个新药要在中国台湾地区上市使用,必须闯过三道关。第一关:准许上市。首先要接受“CDE(财团法人医药品检验中心)”的新药申请(NDA)技术审查,再接受“药品咨议小组”的审议,最后要获得“TFDA(台湾食品药物管理署)”的批准。第二关:医疗保险给付。通过“医药科技评估(HTA)组/CDE”的评估后,再由“药物共同拟订会议”进行审议,审议通过并向“健保署”提出建议,由“健保署”决定给付。第三关:进入医疗院所、基层诊所使用。原则上,只要医师开处方,不论医院门诊药局或社区药局都可调剂,但若“健保署”设定了“药品给付规则”,则应按该规定条件使用。支付价与采购价有价差时,医院多自我调剂以保留利润。
2011年1月台湾地区通过了第二代“全民健康保险法”,并于2013年正式执行。第四十二条对医疗服务及药物给付项目和支付标准进行了规定,其中提到:医疗服务给付项目及支付标准的制定,保险人需先办理医疗科技评估(HTA),并应考虑该项目是否为医疗所必需(其相对疗效如何),同时应考虑医疗伦理、医疗成本效益、保险财务负担等问题。药物给付项目及支付标准的制定同样应该经过上述流程与考量。
严格的新药给付审查流程
新药要进入“台湾健保给付目录”,要通过申请制。新药只要获得“食药署”的审批,厂商便可立刻向“健保署”提出申请,请求纳入健保给付。该案件将交由CDE内的医药科技评估组进行评估,在42天内出具新药评估报告先交由“专家咨询小组会议”进行审议,在专家提出建议后,再由“药物给付共同拟订会议”进行审议,并对是否能报销、报销的条件、药品报销单价等做出最后的决定。在这一过程中,患者团体主要将其意见通过网络对新药申请案提出看法。
台湾地区对于医疗资源的分配,多以科学性证据作判断,包括临床相对疗效、成本效益、预算冲击等多方因素。例如,新科技与参照品比较是否更安全、有效?新科技的疗效价值是否值得多花费来使用?医保财务是否能承担?是否符合临床医疗需求?是否符合健保政策等。然而,对新科技的价值判断不仅仅需要科学性判断,更需要利害相关人的参与审议讨论。
新药分类与核价原则
在中国台湾地区,新药被分为两类:第一类为突破创新之新药,第二类为临床价值中等优于最佳常用药品(2A)和临床价值相近于已收载核价参考品(2B)。其中,突破创新新药需符合以下任一个条件,才能提交新药申请:1.新药理机转作用者(new mechanism of action);2.为有效治疗特定疾病的第一个申请收载的新药;3.显著优于现行最佳常用药品,且有药品对药品直接比较或间接比较结果显示具有正面效果者;4.符合经济效益者。此外,还必须提供能证明突破创新新药疗效显著性与国外成本效益的数据及其对应的文献资料。
在核价原则方面,与现行最佳常用药品的head-to-head比较或临床试验文献间接比较,显示临床疗效有明显改善的突破创新新药,即第1类新药以十国(英国、德国、日本、瑞士、美国、比利时、澳洲、法国、瑞典、加拿大)中位数核价。致力于国人族群特异性疗效及安全性的研发,在中国大陆实施临床试验达一定规模,以十国药价中位数的1.1倍核定。国际药价≤五国,自新药生效次年起,于每年第四季检讨国际药价来做药价调整,直至有药价的国家多于五国的次年或国际药价已检讨五次为止。
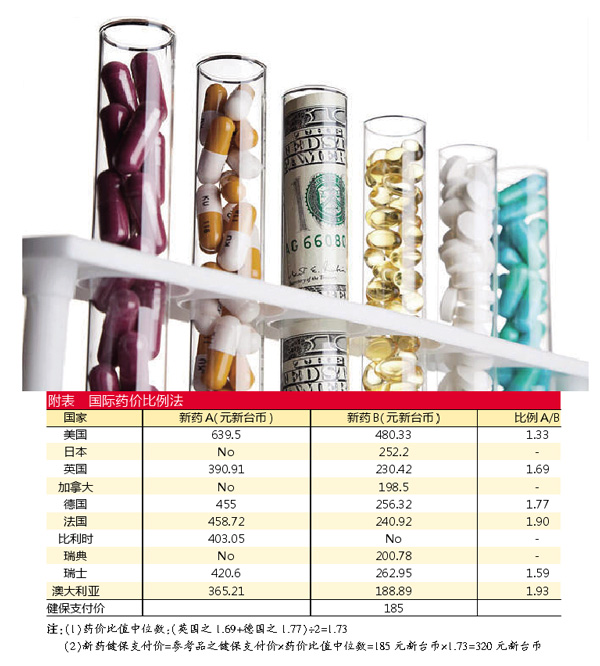
第2类新药的核价原则以十国药价中位数为上限,核价方式多样,如十国药价最低价、原产国药价、国际药价比例法(如附表)、疗程剂量比例法等,而复方制剂应采用各单方健保支付价合计×70%或单一主成分价格核算药价。致力于国人族群特异性疗效及安全性的研发,在中国大陆实施临床试验达一定规模,核算后加算10%。在大陆进行药物经济学的临床研究者,最高加算10%。
核价参考品(比较药)选取原则,以ATC分类(Anatomical Therapeutic Chemical,即解剖学、治疗学及化学分类系统)为筛选基础,原则上以同药理作用或同治疗类别的药品,看谁的使用量最大为选取对象。若有执行临床对照试验的药品,则列为重要参考对象。
[结语]
今年4月,“药物给付共同拟定会议”通过了中国台湾地区“高费用癌症药品纳入健保给付的送审原则”,使得曾经因财务冲击过大等因素无法入选“健保”的第一个癌症免疫疗法新药Yervoy迎来了纳入台湾地区给付项目的曙光。
依据台湾地区新的“修正法”,针对高价药品,在疗效或使用量有较大不确定性时,为达到厂商较快获得给付且保持表面高单价、“健保署”有能力负担、病人尽早获得治疗的三赢目标,将执行价量协议或药品给付协议等方案。具体而言,在健保资源有限的情况下,厂商愿意共同分担风险,以加速新药的给付审议,并执行依疗效结果或财务结果为基础的其他协议。协议由厂商提出,并提交“药物共同拟定会议”同意后适用。协议原则上以5个观察年为上限,必要时重新签约。此外,根据个案情况,厂商可提出以疗效结果为基础的协议方案、以财务结果为基础的协议方案和协议共同分摊方案。由于篇幅有限,此部分内容本文暂不展开,请关注近期本版报道。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



