罕见病用药逆袭秘技
发布时间:2018-11-28 12:39:27作者:马乐伟(本报特约科睿唯安)来源:医药经济报
Alexion如何在“不毛之地”挖出了“金矿”?对中国药企有何启示?
中国罕见病用药布局时机已然来临!
5月22日,国家卫生健康委员会、科学技术部、工业和信息化部、国家药品监督管理局、国家中医药管理局等五部门联合发布了《关于公布第一批罕见病目录的通知》。6月5日,国家卫生健康委员会公布了《关于印发罕见病目录制订工作程序的通知》,为罕见病用药目录的申请提供了具体途径。一时间,罕见病用药万众瞩目!
如何才能抓住这个机遇呢?先行成功者的经验无疑是值得借鉴的。
自1983年美国颁布全球第一部《罕见病用药法案》以来,罕见病用药飞速发展,Sanofi Genzyme、Biomarin、Shire、Aleixon等专注于罕见病用药的公司耳熟能详。其中,Alexion为全球最大的非肿瘤罕见病用药公司。
笔者有幸到访Alexion位于爱尔兰的运营总部,其高效的运营模式、独特的发展理念令人印象深刻。笔者解析其发展路径,结合自身对行业的理解,撰成此文,以期给大家带来一些启发。
Alexion成立于1992年,是一家专注于罕见病用药研发、生产及销售的生物药公司。Alexion从完全需要政府、投资者、合作伙伴财政支持的初创型公司,发展为市值270亿美元、全球排名第41位的跨国制药企业,仅用了26年。
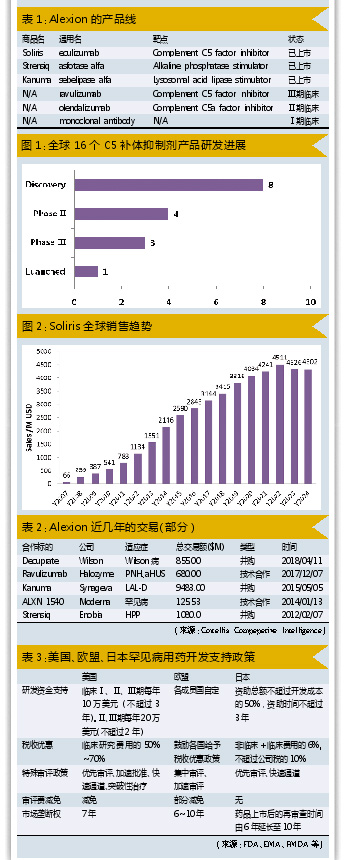
其研发管线只有6个产品,上市的有3个(Soliris、Strensiq和Kanuma)。看惯跨国巨头们动辄数十甚至上百的产品线,Alexion的产品线显得单薄得多。但是,正是这3个产品,成就了Alexion全球罕见病用药“领头羊”的地位。
让我们来看看Alexion的独门秘技!
第一招
“小众药”做成“重磅炸弹”
[关键点] 给医保买单的理由
Soliris(eculizumab)为全球第一个也是唯一一个上市的C5补体抑制剂。围绕该靶点,全球范围内处于活跃状态的药物共16个。或许是因为该靶点开发难度巨大,该领域的竞争显得并不那么激烈。
该药2007年登陆美国及欧盟市场,也是Alexion成立15年后上市的第一个药物。截至目前,Soliris共获批3个适应症:阵发性睡眠性血红蛋白尿症(PNH)、非典型溶血性尿毒综合征(aHUS)、乙酰胆碱抗体阳性重症肌无力(AChR antibody-positive generalized MG)。其中,Soliris是全球范围内PNH、aHUS两个适应症唯一的用药选择。
从适应症来看,3个适应症均获孤儿药资格。Soliris上市后,全球销售额一路飙升,2012年以11.24亿美元的销售额步入重磅炸弹梯队,2017年全球销售额31.44亿美元,占公司营业收入的89%。Clarivate分析师预测,2022年将突破45亿美元。Soliris在扮演Alexion吸金利器的同时,也成为全球孤儿药妥妥的大佬。
全球范围内,使用Soliris的患者不过几千人,其市场却“芝麻开花节节高”,在笔者看来,主要得益于两方面:
1.天文数字般的药价:每位病人每年需花费44万美元。而且,因为该药疗效确切及不可替代性,私营保险公司和国家性医保机构都愿意为此买单。
2.高难度的研发:C5补体抑制剂开发难度高,竞品在短时间内很难被开发出来。
从作用机制上看,C5补体抑制剂理论上在类风湿性关节炎、银屑病、心脏病炎症并发症等风湿免疫性疾病领域均有较大潜力。Alexion早期的确在这些领域做了大量研究。然而事与愿违,在一系列临床试验中,eculizumab对类风湿性关节炎和膜性肾病的疗效均未达预期,这也意味着eculizumab从风湿免疫性领域中市场潜力最大的疾病获利的可能性微乎其微。
不过值得庆幸的是,2006年初,基于TRIUMPH和SHEPHERD的Ⅲ期临床研究结果显示,eculizumab在治疗PNH方面表现出显著的疗效和良好的安全性。
然而,PNH为罕见病,开发此类疾病与Alexion最初的发展战略出现了很大偏差。面对如此处境,Alexion的领导层经过深思熟虑后,重新规划了企业的发展策略——与其在正面战场与各路诸侯厮杀,不如在罕见病用药领域一骑绝尘。
剑走偏锋,在看似不毛之地中挖出了金矿。令人意想不到的是,这个金矿还非常耐挖:与那些患者群达几万、几十万的非罕见病用药面临的价格压力相比,Alexion开发的药品多年来几乎不受影响。
Soliris上市之后,Alexion深度挖掘了在研产品治疗罕见病潜力,并成功转型为一家专注于罕见病用药的制药公司。
第二招
“买买买”摆脱单一品种风险
[关键点] 买什么?申报策略?
得益于Soliris超强的盈利能力,Alexion在资本界大受追捧,2015年市盈率一度高达105倍。
但是,要配得上如此高的市盈率,Alexion必须维持非常高的增长速度。由于自身产品线短时间内很难出现新的增长点,因此Alexion一方面大力拓展已有产品的适应症,另一方面发起了一系列并购及合作,最近5年交易额高达122.2亿美元。
Alexion的并购策略非常清晰——完全围绕罕见病用药进行。值得关注的是,目前Alexion上市的3个产品中,2个来自并购(Strensiq和Kanuma),而且这两个药物均是各自领域中唯一的不可替代产品。
2012年2月7日,Alexion以10.8亿美元的代价完成了对Enobia公司的收购。看重的品种就是其在研产品asfotase alfa(Strensiq)。
Strensiq的上市结束了Alexion八年来完全依靠单一品种Soliris的历史。Strensiq于2015年登陆美国、欧洲及日本市场,是全球第一款也是目前唯一一款用于围产期、婴儿期、青少年期发作的低磷酸酯酶症(HPP)的治疗性药物。其临床优势显著,可使5岁及以下HPP患者的5年总生存率从27%提高到89%。Strensiq上市后第二年,全球市场就突破3.3亿美元。Clarivate分析师预测,该产品在2024年将成为“重磅炸弹”(10.2亿美元)。
从Strensiq在美国的获批路径来看,除加速批准之外,几乎把FDA所有的特殊审评政策都用上了。
其实,特殊审评政策只是美国政府鼓励企业开发罕见病用药的政策之一。除此之外,美国政府还从“研发资金支持”“税收抵免”“市场垄断权”等药品的全生命周期进行政策倾斜,这些政策极大提高了企业开发罕见病用药的积极性。QuintilesIMS的一项研究表明:单就“税收抵免”一项而言,若无该项政策,三分之一的孤儿药将无法被成功开发出来。
除美国外,欧盟、日本等发达国家和地区也有类似的政策。
另一个并购重要产品是Kanuma(sebelipase alfa),其原研公司为Synageva。正是看好这个品种在罕见病溶酶体酸性脂酶缺乏症(LAL-D)的潜力,2015年5月,Alexion发起了其历史上规模最大的并购,通过股票及现金的形式,以84亿美元的代价收购了Synageva。
Kanuma是一种基因重组酶,于2015年12月登陆美国市场,它是全球第一个也是唯一一款用于LAL-D的药物。
临床价值方面,在Kanuma之前,患有LAL-D婴儿1年内的生存率几乎为零。从2017年11月公布的最新临床数据看,Kanuma可将患婴1年的生存率从0提高到了80%。
考虑到LAL-D极其罕见(发病率低于0.002%)以及Kanuma“独一无二”的地位,分析师预计该药2024年将突破3亿美元。
无独有偶,从申报策略来看,Kanuma采用了与Strensiq几乎完全相同的思路,而且获批速度更快(从获得孤儿药资格到上市,仅用了5年)。
第三招
“二代重磅药”应对仿制冲击
[关键点] 拓展适应症、剂型升级
虽然Alexion通过并购获得了Strensiq和Kanuma,但目前Soliris仍是一品独大。而安进已将Soliris的生物类似药推进到了Ⅲ期临床。为了守住Soliris的阵地,Alexion提早布局了Soliris的下一代产品——ALXN1210(ravulizumab)。
ALXN1210的推进主要从两方面进行:一个是对Soliris适应症的延续和拓展,另一个是皮下给药途径的探索及释药周期的延长。
在适应症延续方面,PNH及aHUS已经进入Ⅲ期临床。从公布的临床结果看,ALXN1210非劣效于Soliris,半衰期却是Soliris的4倍,所以ALXN1210的给药周期可以达到8周一次(Soliris为2周一次)。因此,与Soliris相比,ALXN1210占绝对优势。2018年6月,Alexion向FDA提交了ALXN1210的上市申请,有望于2019年获批。
在皮下给药途径探索及释药周期的延长方面,2017年10月,在ALXN1210皮下注射给药Ⅰ期PK临床试验完成的基础上,Alexion计划开展给药周期1周/次的Ⅲ期临床。2017年12月,又与Halozyme公司合作,利用ENHANZE递药技术平台开发“2周/次”“4周/次”的皮下注射剂(ALXN1210 SC)。静脉滴注改进为皮下注射,可避免给药前复杂的稀释工作并缩短给药时间,治疗顺应性会大为提高。
基于此,分析师预测ALXN1210有望在上市第二年就突破10亿美元。即便Soliris的生物类似药上市,Alesion公司依然可以延续Soliris的神话。
在Soliris的“阵地守护战”中,因为有了ALXN1210,已然成功了一大半。
【中国启示】
中国企业布局罕见病用药
时机已到
对于制药企业来说,在抗肿瘤、心血管、CNS等“正面战场”竞争日益白热化的当下,布局罕见病用药不失为一种明智的选择。
从临床需求看,中国罕见病患者至少有1600万人,每30万至50万人中就有一名患者。在美国、欧盟和日本批准的罕见病用药中,只有37.8%、24.6%和52.4%在中国市场销售。在24所三级公立医院中,31种罕见病用药的平均使用率仅为20.8%。
从政策支持看,罕见病用药因市场调节失灵,其发展高度依赖政策,中国第一批罕见病用药目录的发布,为罕见病用药的发展奠定了政策基础。相信后续会有一系列配套政策落地,如研发财政支持政策、审评审批政策、税收优惠政策、医保支付政策等。
从盈利能力看,据Quintiles IMS(现IQVIA)统计,2016年,罕见病用药仅占美国药品使用量的0.3%,但销售额却占到药品总销售额的7.9%,其盈利能力之高可见一斑。
企业发展要长远,
关键是“聚焦”
纵观Alexion的发展历程,无论研发还是并购,都紧紧围绕其最擅长的罕见病用药进行,并逐渐形成了与众多制药巨头完全不同的发展思路——“以罕见病适应症为核心”而并非“以产品为中心”的研发思路和商业模式。
事实证明,并非只有产品多元化才能取胜,在一个领域做到极致也可以称霸世界。对于“什么都想做”的中国医药企业来说,“聚焦”显得弥足珍贵。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



