药价调控思路
发布时间:2018-11-22 15:28:53作者:杨峋来源:医药经济报
对标国际药品先进政策,提高药品审评速率;选择正确的成本分析方法,谋求合理范围内的药品最大利润;建立公开透明、多方参与的药品价格谈判机制
药品关乎着民生健康,我国一直把药价调控视为新医改的重中之重。近日,国家下调14种前期国家谈判抗癌药的支付标准和采购价格,要求9月底前各省级药品集中采购平台按照调整后的新价格公开挂网采购。
药品的最终价格,大体来说要经过研发、上市、流通三大步骤才能确定。想要降低药价,必须从这三个方面入手,对症下药,以达到立竿见影的效果。
审批提速和控费
缓解研发负担
药品的研发成本主要受药品研发难度和审评时限的影响。近年来国家为了降低药品的研发难度,加快药品的审评速率,对标国际药品先进政策,推出了一系列政策文件和指导原则,包括:要求药品审评必须严格按照规定时限进行操作;对具有明显临床价值和优势的药品优先审评审批;发布了国家鼓励研发的药品目录;针对特定剂型、用途的药品甚至是某一特定药品的研发制定专门的指导原则;加强药企与药监部门的沟通交流,为药品开发及时提供指导,减少药企无效重复的工作。
自这些政策文件和指导原则实施以后,药品从开发到获批的时长大幅下降。目前仿制药一致性评价的审评平均时长为70个工作日,新药一期临床的审评平均时长为120个工作日,新药的上市批准可在4~5年内完成,审评速率已经达到了国际先进水平。随着药品审评积压问题逐步解决,药品排队等待时间将进一步下降,未来这一时长还会进一步缩减。
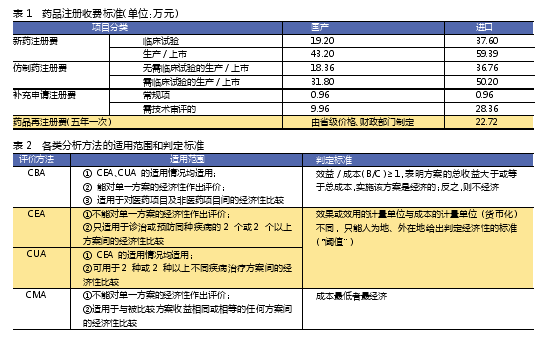
另外,在全球范围来说,中国药品的注册收费标准还是较为合理的,基本不到国际收费标准的十分之一,目前实施的现行药品注册费标准见表1。
除了优惠的药品注册收费标准外,对于中小微药品生产企业还有一定的费用减免政策。另外,为了激发药企的研发热情,国家还制定了专门的研发项目加计扣除退税政策,这些政策进一步降低了药企的研发支出,变相降低了药品的研发成本。
用适合的成本分析法合理定价
药品正常获批,生产场地通过GMP认证后,就正式进入投产阶段。药企会通过改进生产方式、提高生产效率的方式来降低企业的生产成本,同时根据市场上同类药品的竞争激烈程度和自身的优势制定出厂价格,尽快收回研发和生产投入,谋求合理范围内的最大利润。
目前药物经济学中确定成本的分析方法主要有四种,包括成本-效益分析(cost-benefit analysis,CBA)、成本-效果分析(cost-effectiveness analysis,CEA)、成本-效用分析(cost-utility analysis,CUA)以及最小成本分析(cost-minimization analysis,CMA)。
现今CEA在药品成本分析中最为常用,因为两个药品治疗同一疾病,CEA是一种更为快速和直接的评价,而CBA 和CUA 主要用于不同治疗类别的项目的比较,测算时间周期也相对较长,CEA收益以临床效果指标表示,这些指标在药品临床研发的过程中即可获得,并且可以更加直观地进行定性和定量分析,指导制定出更加科学合理的治疗方案。
除了成本分析外,在制定药品出厂价时还应该考虑病例人数、患者分布、治疗效果、市场竞争、政策扶持等多方面的因素,其中最主要的一点就是市场竞争力的影响。在市场独占期内的药物可能会适当提高出厂定价来尽快收回研发和生产支出,因为在市场独占期过后,大批仿制药上市后,药品的出厂价格将出现大幅度跳水,这无疑会打击药企创新的动力;但若矫枉过正,大批仿制药被专利和市场独占权挡在门外,则会造成一家独大。如何保持药品创新和仿制竞争之间的平衡,是相关部门应该认真考虑的。
参照目前FDA的做法,针对药品创新和仿制竞争平衡,有Hatch-Waxman(药品价格竞争与专利补偿)法案、GDUFA(仿制药用户付费法案)、PDUFA(处方药用户付费法案)和BPCI Act(生物药价格竞争和创新法案)支持,按分类对药品设立了不同长度的市场独占期、审评资料要求和收费标准,同时鼓励药企对原研药进行专利挑战,对首批通过专利挑战的仿制药给予180天市场独占期的奖励;建议药师在开具处方时选择仿制药,控制成本;采取措施阻止原研药企妨碍仿制药上市进程的各种操作,包括提交无意义的公民请愿申请、滥用REMS等,在保障低价仿制药可及性的同时,激励药物创新,使药品的出厂价格保持在一个合理的范围内。
介入药品流通 打碎利润泡沫
新医改以来,在构建公立医疗机构药品集中采购新机制过程中,各地普遍反映专利药品和独家生产药品缺乏市场竞争,价格偏高,建议在推进公立医院药品集中采购过程中,采取统一谈判的方式,把价格降至合理区间,这也是国际通行做法。因此,《关于完善公立医院药品集中采购工作的指导意见》提出分类采购的新思路,要求对部分专利药品、独家生产药品,建立公开透明、多方参与的药品价格谈判机制。
2017年国家医保药品目录调整时,针对部分专利、独家药品临床价值高且价格相对较贵的实际情况,建立了医保经办机构与药品企业的谈判协商机制,将36种高价药(其中15种是抗癌药)通过谈判降价、确定全国统一的医保支付标准后纳入目录范围,这些药品的平均降价幅度达到44%,最高降幅达70%。近日,国家医疗保障局印发《关于做好前期国家谈判抗癌药品医保支付标准和采购价格调整的通知》,再次下调14种前期国家谈判抗癌药的支付标准和采购价格,要求9月底前各省级药品集中采购平台按照调整后的新价格公开挂网采购。这14种抗癌药均为国家医保药品目录中的品种,其中12种是2017年谈判降价后纳入目录的,其余2种是2015年国家药品价格谈判的药品。
除了药品价格谈判外,国家还在大力推行“两票制”和“零加成”政策,规定从生产企业到医疗机构中间最多只能经过一个经销商,全程只能最多只能开两次税票,并且医疗机构在销售药品必须平进平出,大大缩减了药品的流通环节,降低了药品的市场价格。不过在政策推广实施的过程中,有关部门也要加强监管,建立黑名单制度,防止虚开发票变相抬高药价的现象出现。
国家针对药品流通领域的种种政策实施,着实降低了药品的市场价格,危重急需药品也纳入了医保,增加了医保报销比例,降低了人民群众的治病负担。现在的当务之急是推动政策在各地尽快实施,让更多的人享受到该政策的福利。
结语<<<
在多管齐下综合施策下,我国药品市场价格近年得到了有效控制,尤其是对急危重症患者的治疗费用都有了大幅削减,再加上医保高比例的报销制度和社会慈善机构的支持,像电影《我不是药神》中普通家庭一病返贫的现象有望不再轻易发生。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



