“药品质量更新”谋略
发布时间:2018-10-31 17:00:18作者:李壮琪/编译来源:医药经济报
“药品质量更新”谋略
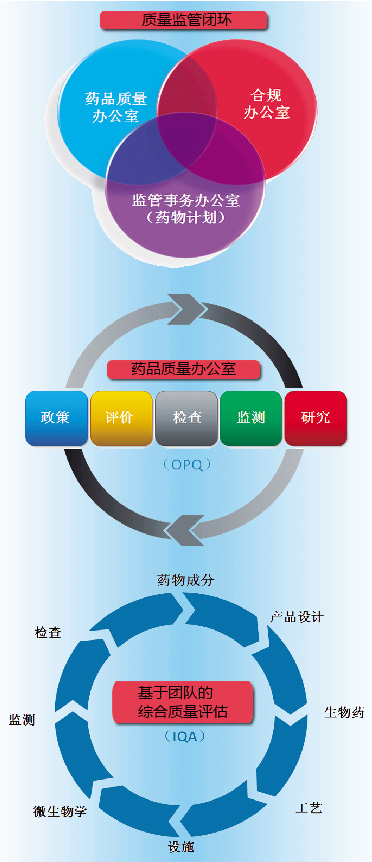
药品质量(Pharmaceutical Quality)是确保患者和消费者持续获得安全有效的药物的基础。药品质量办公室(OPQ)作为美国FDA药品评价与研究中心(CDER)下设办公室,旨在确保美国公众对高质量药品的可及性。OPQ坚持与CDER合规办公室、监管事务办公室保持“质量监管一个声音”,其质量监管形成闭环,包括制定政策、评价政策的可行性、对药品质量进行检查、持续监测、过程研究,最终再指导政策,实现药品质量监管的动态循环。
OPQ未来战略重点
2018年初,OPQ发布了2018-2022年战略计划。该计划包括战略重点、使用者付费计划中的优先事项和绩效目标,笔者梳理总结为四个方面。
加强组织合作
OPQ通过综合质量审评(IQA)整合其审评和检查职能。所谓IQA,是指其学科专家团队对申请人向CDER提交的申请进行全面质量审评,并最终形成质量建议书。同时进行质量审评的改进,开发贯穿整个药品生命周期的现代审评和知识管理工具:围绕药品关键质量属性的质量风险和相应的控制策略,以及围绕药品成分(APA)和控制策略设置管理面板,为生命周期知识管理和ANDA质量评估标准化设计计算机辅助界面;制定风险-获益评估框架,平衡临床实践中潜在的产品质量问题。
据悉,2017年CDER共发布7个政策和程序手册(MAPP),对220个外部咨询和527个书面咨询做出回复,并在GDUFA的目标日期内发布了10个指南,分别是《ANDA:与仿制药申请优先审评相关的设施信息的预提交》、《推进新兴技术用于医药创新和现代化》、《年度报告中的特定生物制品的CMC批准后生产变更》、《固体口服制剂单位剂量再包装产品的有效期》、《药品标签中儿童安全包装声明》、《医用气体质量管理规范》、《延长战略性库存中强力霉素片剂和胶囊的有效期》、《基于生物药剂学分类系统的速释固体口服制剂的体内生物利用度和生物等效性研究豁免》、《含有纳米材料的药品(含生物制品)》以及《药品中的麸质和相关标签建议》。
提升高质量药物可及性
为实现提高高质量药物可及性目标,OPQ建立了新兴技术计划,支持研发中药物设计和生产的创新方法,确定并解决与新方法相关的潜在科学和政策问题,包括首个批准上市药品从批生产转向连续生产。2017年,FDA开发了关于新兴技术计划的网站,并发布一份行业指南,以保证该计划要点顺利实施。
此外,OPQ正在对免疫学、肿瘤生物学、生产科学与创新、药物分析与表征、感染性疾病与炎症的科学研究,以在不同方面提高药品质量,扩大可及性范围。
提高对药品质量重要性的认知和承诺
申请人和监管机构在质量沟通方面存在偏差,往往导致监管机构审评时间的严重无效付出。基于此,FDA要求申请人在提交NDA、ANDA、BLA时,更好地利用通用技术文件(CTD)的质量综述(Quality Overall Summary,QOS),旨在为审评人员提供药品质量的关键信息,减少审评人员工作量。
2018年1月,FDA发布的白皮书中描述了创建QOS需要考虑的关键因素:(1)在以患者为中心的背景下解释产品和工艺开发;(2)有效总结总体质量控制策略;(3)通过提交申请充分总结整体质量控制策略,以指导监管机构。
当前,在基于问题审评(QbR)的模式下,许多仿制药申请人已经可以有效使用QOS,并且未来仍有可能继续使用这种方法。
2017年,OPQ年度报告还重点介绍了审评、检查、监测、政策及研究方面的主要成就,报告强调本年度共有1027个仿制药申请获得批准或暂时批准,这一数据突破了历史记录。
加强利益相关方的参与合作
OPQ与美国药典委员会(USP)、美国药物研究与生产商协会(PhRMA)等多个组织定期合作。2017年,FDA有上百位联络人与USP专家委员会和专家小组的专家保持联络。同时与澳大利亚、日本、欧盟等国家和地区的监管机构也有广泛合作。与PIC/S合作检查并及时共享质量信息,如产品质量缺陷、召回。
此外,OPQ还与ICH基于Q12“药品生命周期管理的技术和监管方面的考虑因素”和M9“基于生物药剂学分类系统的生物豁免”内容进行了质量沟通。并与签署协议的12个欧盟成员国就检查药品质量内容进行交流,提高检查效率。
利益相关方参与
质量量度计划
FDA认为,“只有被量化的工作,才能有效完成。”故FDA相关负责人在改进生产和提高产品质量的愿景下于2013年首次提出质量量度概念。FDA于2015年7月发布《质量量度要求指南草案》,要求行业报告批次接收率、产品质量投诉率、无效的超标(OOS)率、年度产品回顾(APR)或产品质量回顾(PQR)按时完成率,就如何使用数据进行讨论。
基于行业反馈,2016年底,FDA发布了《质量量度指南草案修正案》,报告将不再包括年度产品质量按时完成率,但不包括不等于不重要,监管机构希望行业以更有效的质量量度进行质量监管。
为评估潜在的质量问题并在整个制药行业监测质量效用,FDA还于今年6月宣布了两项最新的质量量度计划——质量量度反馈计划和质量量度现场考察计划,这是对利益相关方就质量量度继续加强沟通请求的回应,并告知监管部门质量量度实施绩效的方法。
为什么质量量度对监管机构如此重要?
有文献提出,21世纪的药品质量监管愿景是“最大程度地提高制药行业效率、敏捷度和灵活性,无需过多监管,就能生产出高质量药品”。FDA的药品cGMP要求生产商有持续的计划,以维护和评估产品及与产品质量相关的工艺数据,促进持续改进并满足ICH Q10要求的质量测量指标。质量量度是现代化生产的要求,作为质量文化的重要步骤,监管部门鼓励企业改进现有质量计划或启用新的质量计划。
当前,很多生产场地使用质量量度,质量量度不仅可以监测质量控制体系和工艺,确保其符合标准,确定改进生产的方法,对制药行业来说,质量量度的应用还能为患者、生产商及FDA带来潜在效益,比如更好地应对药品短缺问题等。
小结<<<
OPQ加强组织合作,使用工具使申请和知识管理的质量评估现代化;提高高质量药物可及性,支持药品设计和生产过程中创新方法的开发和实施;提高对药品质量重要性的认知和承诺,在以患者为中心的背景下,强调产品和工艺开发的重要性;还将加强合作关系并使利益相关方参与进来,持续讨论质量量度。
(本文由沈阳药科大学杨悦教授指导)
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



