中药新药开发审慎前行
发布时间:2018-10-31 11:45:21作者:安金蒙来源:医药经济报
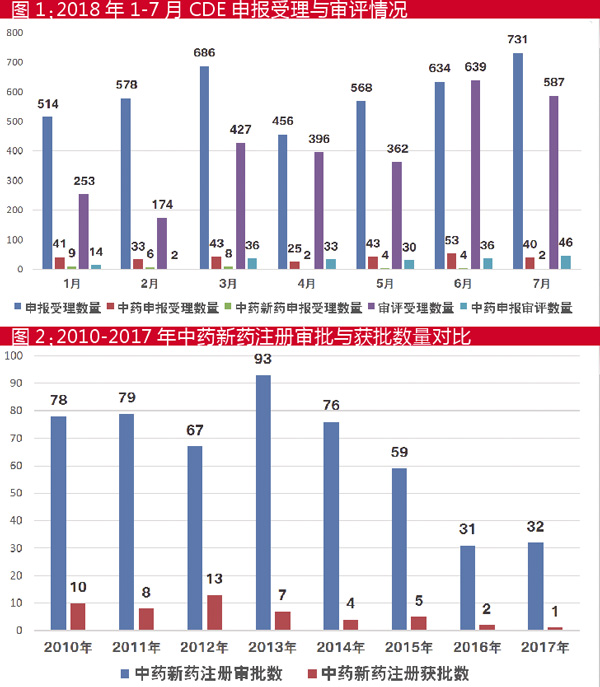
截止2018年7月31日,今年CDE共受理药品注册申请4167件,其中中药申请278件,中药新药申请35件;审评受理申请2838件,其中中药申请197件(见图1)。从审评审批进展来看,根据中国新药研发监测数据库CPM的统计,2018年上半年,有127个全新品种完成首个临床研究申请的审批,其中创新药100个,改良型新药26个,首仿药1个,未有中药产品;从批准上市来看,国产创新药共计5个产品拿到上市许可,未有中药产品。
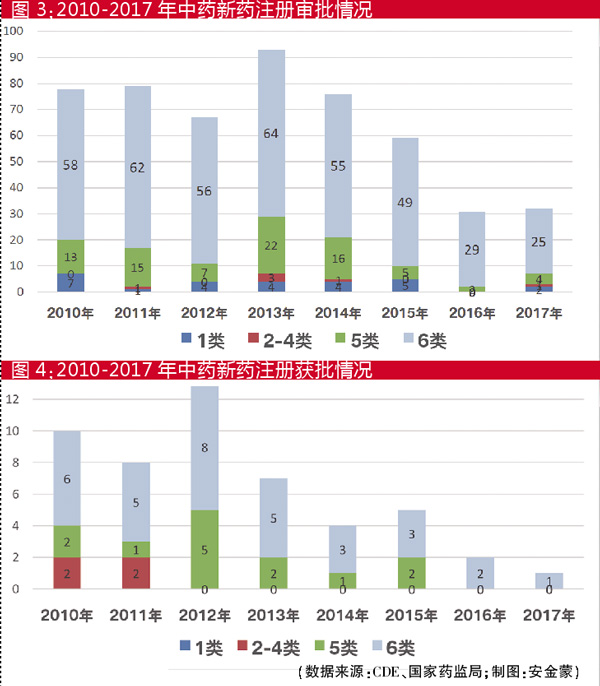
近年来,中药的注册审批始终低迷,注册数与通过数屡创新低(见图2)。究其原因:一方面国家监管日趋严格,上一轮中药现代化大潮催生的诸多独家大品种注射剂安全性存疑,顶层审批态度回归谨慎,转而鼓励传统用法;另一方面,因缺少确切临床证据,中药产品的销售首要取决于推广能力而非产品疗效,导致研发回报率低迷。研发型企业的研发对利润的贡献较低,多数企业选择等待新规,且多通过收并购等方式进行新品种开发。因此,为切实推动中药新药开发,除企业的积极行动外,政府的支持也至关重要。
上半年6项临床试验获批
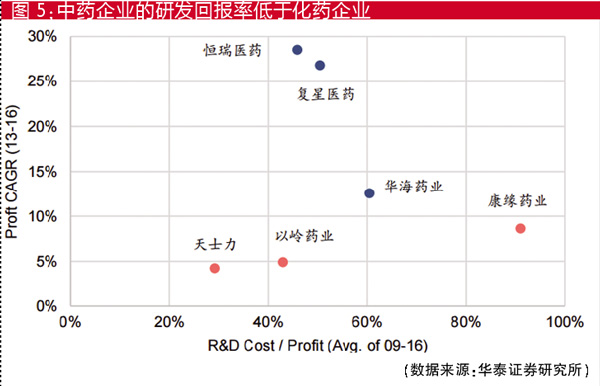
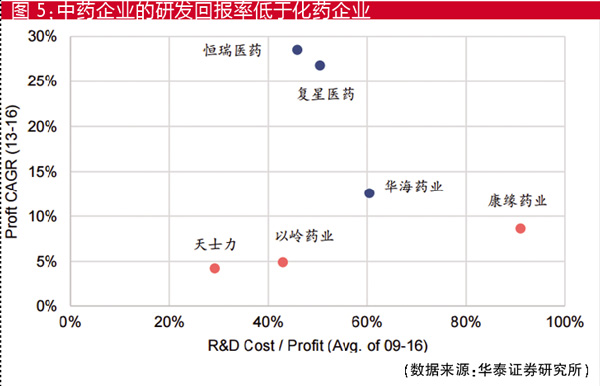
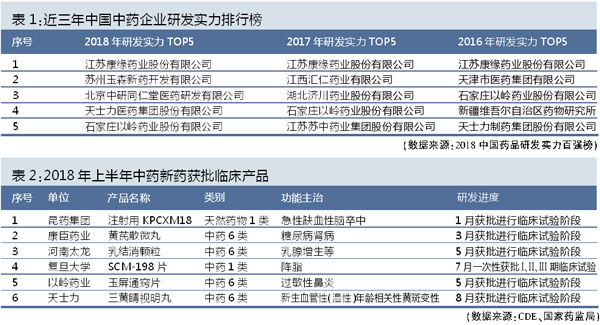
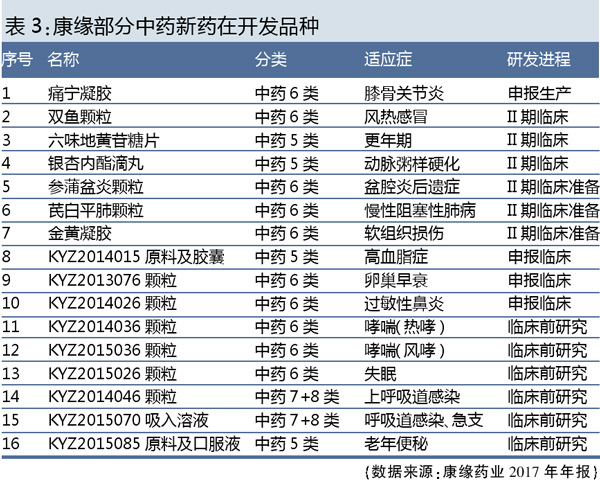
近年来,我国中药新药上市数量持续低迷,2017年批准上市的394个药品中,中药仅有2个,中药新药仅有1个。2012-2016年,批准上市的中药新药分别为21个、15个、11个、7个和2个,呈递减趋势。2017年,中药新药申报分布较多的地区为江苏、上海、北京等中医药产业较为发达的地区,申报企业排名靠前的企业为江苏康缘药业、和记黄埔医药、济川药业集团、北京中研同仁堂。
为鼓励企业进行中药新药研发工作,6月,国家药品监督管理局发布《中药药源性肝损伤临床评价技术指导原则》,同时发布《中药药源性肝损伤临床评价技术指导原则》起草说明,旨在控制中药用药的安全风险,推动中药新药研发,从而促进中药产业健康发展。
8月,安徽省政府印发《支持现代医疗和医药产业发展若干政策》,提出鼓励创新药械产品研发、支持中药材规范化种植和原料药保障能力建设等十项政策措施。对在该省生产的中药新药(1~4类)及中药经典名方二次开发等,单个项目最多补助可达1000万元。
得益于各级政策的支持,未来中药新药研发及上市或有望迎来春暖。2018年上半年,获国家药品监督管理局批准进行的中药新药临床试验就有6项(见表2),其中4项为中药6类,另外,多个中药企业已着手布局经典名方和中药新药的开发。
寻找开发新思路
中药新药的开发需要注意以下几点:
开发能充分发挥中药优势与特色,市场短缺的中药。中药新药的开发应顺应人类医疗服务模式转向自助预防保健的大趋势,解决人类疾病谱改变所产生的新课题,发挥其自身特色和优势,吸收当代科技的最新成果,开发出有中药特色的新药品。如中医的外用药、皮肤科用药、儿科、妇科用药,有很多疗效独特,亟待挖掘开发的品种。
重视经典名方开发,推进中药复方的开发。经典名方目录现已发布,其政策节奏、调控思路与一致性评价有异曲同工之妙,或将引发中成药市场洗牌。提前做好战略布局,尽早启动产品开发,或可先声夺人。
重视疗效与循证研究。中药开发,疗效应放在首位,如何正确处理好疗效与各方面的辨证关系,找到其平衡点是首要考虑的问题;再者,要重视产品上市后的循证研究,不断为疗效提供关键思路与确证。
结合企业实际,制定战略布局与规划。中药新药开发是一项高投入,以期有高收入的行为,要对研究工作进行全方位的把控,结合企业实际,开发确有药源保障、技术支持、营销渠道的产品。尤其应重视专利布局,保证开发者对所开发产品市场销售的独占权。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



