数据解密一致性评价四大焦点
发布时间:2018-10-31 11:16:09作者:本报特约撰稿 边界来源:医药经济报
[焦点1] BE豁免
目前获得豁免BE的品种有哪些情况?若豁免申请不能通过会怎样?豁免BE品种未来竞争状况会是怎样的?
根据2017年《总局关于仿制药质量和疗效一致性评价工作有关事项的公告》(2017年第100号),可以豁免BE研究的情况有两种:
一是对符合《人体生物等效性试验豁免指导原则》的品种,以及不适合开展人体内研究的品种,将区别情况,分批公布具体品种目录;另外,企业也可向国家药监部门提出豁免申请并说明理由,国家药监部门经论证后,决定是否同意豁免。
目前已豁免并通过一致性评价的产品只有蒙脱石散,其通过一致性评价的厂家有四川维奥、先声药业和扬子江药业。
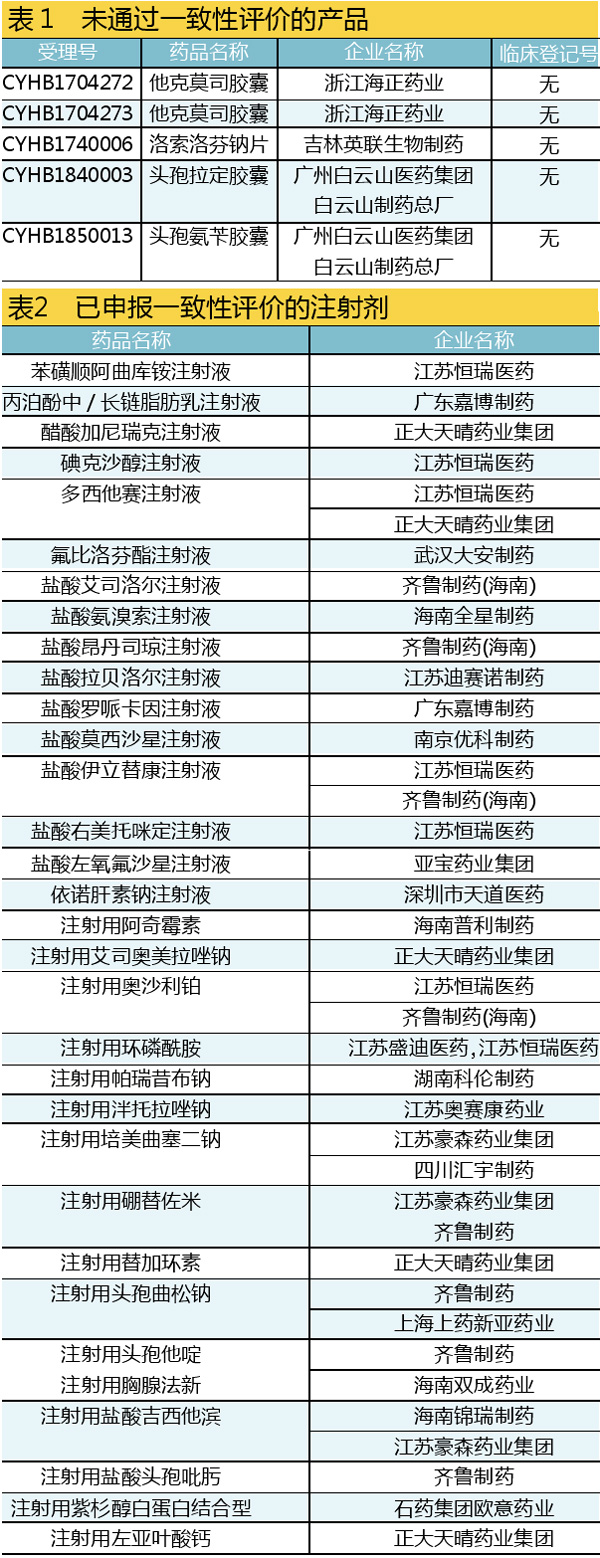
然而,豁免申请并不一定都能获得通过,一旦不通过,就有可能不予批准通过一致性评价。如表1所示,目前未通过一致性评价的产品有4个,它们的共性是都没有启动BE研究。
在欧盟、美国或日本批准上市的仿制药已在中国上市并采用同一生产线同一处方工艺生产的,申请人需提交境外上市申报的生物等效性研究、药学研究数据等技术资料,由国家药品监管部门审评通过后,视同通过一致性评价。例如浙江华海的厄贝沙坦片、厄贝沙坦氢氯噻嗪片、福辛普利钠片、赖诺普利片、利培酮片、氯沙坦钾片、奈韦拉平片和盐酸帕罗西汀片,石药集团欧意的阿奇霉素片和盐酸曲马多片,都是2015年以后并没有启动BE研究但也视同通过一致性评价了。
市场潜力大、不需要启动BE研究的产品无疑受到青睐。但笔者认为,这类产品技术门槛相对较低,竞争加大后将会面临价格战。
[焦点2] 289目录品种
2018年底期限在即,目前通过率多少?未通过一致性评价的289品种未来何去何从?
2016年发布的《国务院办公厅关于开展仿制药质量和疗效一致性评价的意见》 (国办发〔2016〕8号)中提到,2007年10月1日前批准上市的化学药品仿制药口服固体制剂,应在2018年底前完成一致性评价,其中需开展临床有效性试验和存在特殊情形的品种,应在2021年底前完成一致性评价;逾期未完成的,不予再注册。化学药品新注册分类实施前批准上市的其他仿制药,自首家品种通过一致性评价后,其他药品生产企业的相同品种原则上应在3年内完成一致性评价;逾期未完成的,不予再注册。但是,在2017年第100号文中,并没有提及相关产品逾期未完成不予再注册的限制。
此项政策影响最大的是2007年10月1日前批准上市的化学药品仿制药口服固体制剂(即289目录产品),目前通过一致性评价的生产批文仅23个,此前(截至2018年8月8日)公布的289个仿制药质量和疗效一致性评价品种批准文号共17740个,通过率仅0.13%。
自2017年12月29日首批一致性评价通过品种公布以来,共有17个产品属于化学药品新注册分类实施前批准上市的其他仿制药。截至2018年8月8日,共有139个产品申报一致性评价。若已上市产品设定一个通过一致性评价的时间表,大量的生产文号有可能因此而被淘汰。
[焦点3] 注射剂
目前注射剂启动一致性评价的积极性如何?申报产品数量较多的是哪些企业?
2018年国家开始启动针对注射剂的一致性评价,目前已有32个产品申报。
如表2所示,齐鲁制药(含海南)是申报产品数最多的生产厂家,共申报了8个产品。其次是恒瑞,申报了7个产品。正大天晴申报5个注射剂排名第三。
同品种药品通过一致性评价的生产企业达到3家以上的,在药品集中采购等方面不再选用未通过一致性评价的品种,医院采购影响最大的是注射剂。由此可见,为了一致性评价的红利,注射剂企业也在积极竞争最早通过一致性评价的资质。
[焦点4] 通过一致性评价需要多少时间
第一家获批一致性评价后,同类产品其他企业在3年内完成一致性评价是否可能?
咸达药海遨游数据库发现,289个申报一致性评价的受理号中,仅162个在2015年7月22日以后登记了BE研究,其中2个为2015年启动BE研究,2016年启动了14个BE研究,2017年公开BE研究111个,2018年至今则有35个。从CDE临床登记号公示到一致性评价申报,平均要花7.4月,这个时间可能受到企业公告临床登记号较晚的影响。从申报一致性评价到有结论是否通过一致性评价(不含发补通知),平均要花5.6个月。如果考虑药学研究和中试放大的时间,一致性评价预计用24个月就可获得审批结果。
因此,第一家获批一致性评价后,同类产品生产企业在3年内完成一致性评价是非常有可能的。289目录的产品企业之所以不启动一致性评价研究,归根到底还是市场潜力不足以支持一致性评价研究的费用。
【小结】
随着越来越多产品获批通过一致性评价,国内企业也在不停地争取一致性评价的福利。上海、江苏、山西、陕西、内蒙古、宁夏、吉林、广西、辽宁、湖北、浙江等多个省份对通过一致性评价品种明确出台了特殊采购政策。然而,国内的一致性评价产品偏向于市场潜力大、不需要启动BE研究的产品。但这类产品技术门槛相对较低,竞争加大后将会面临价格战。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



