药品管理风险简史
发布时间:2018-10-29 14:40:48作者:编译 陈昕朦来源:医药经济报
药品管理风险简史
本文讨论质量风险管理(QRM)的主要原则,以及QRM在产品生命周期中的作用、实施过程中常见的困难等。
早期药物风险管理
自相关监管机构成立以来,风险管理一直是药品监管的基本内容。事实上,人们可能会争辩说,监管机构存在的主要原因是为了保护公众免受与药品使用相关的健康安全风险。
药典,是最早期的参考文献来源,可追溯到公元1世纪。最早始于西西里的弗雷德里克二世于1240年颁布的《萨勒诺医疗法令》,要求药剂师们采用同样的方式配备药物。这些法令在中世纪的整个欧洲大陆越来越普遍,人们认识到药物制剂之间的一致性对于确保产品的预期效果十分必要,并且能够最大限度降低患者服用药物的风险。
至19世纪晚期,有更多的关于药物的法规生效。在美国,第一个与药物管理相关的法规于19世纪中叶颁布。在此期间,美国士兵接受各种药物治疗各种疾病(包括疟疾、黄热病和霍乱)。其中许多药物是进口的,有些药物由于管理失误被证实缺乏预期的安全性和有效性。这一时期发生的大量死亡,不仅仅来源于战争因素,还包括使用这些不安全的药物。因此,1848年美国进口药物方案出台,以确保进口药物在进口之前已进行纯度和质量检测。“进口药物法”确定了全球药物监管的主题——药物监管的进展由药物监管结果所促使。
FDA相关法规的颁布也是由几个被广为传播的恶性事件所促使的,在此不赘述。这种模式的反应性,即医疗灾难先与医疗监管的模式,一直延续至今。例如2008年的肝素丑闻,随后对药物活性成分(APIs)的管理和日益负责的供应链受到了越来越多的关注。虽然这种模式能够防止未来的伤害,但人们日渐发现,通过使用正确的工具和理念可以预见和避免类似悲剧发生。
遵循预防原则
预防原则是主动的风险管理。该原则最初是在环境法的背景下进行讨论,认为当面临给定风险的不确定性时,特别是当风险的后果可能产生严重和持久影响时,必须谨慎使用。该原则作为监管机构的决策指南,在缺乏关于某种风险的科学证据下被援用。
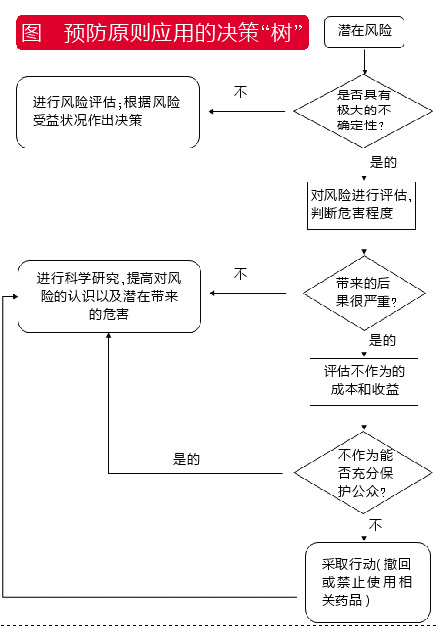
作为决策的辅助手段,预防措施被看作是一个基本的风险管理过程(如图所示)。预防原则的主动性源于对不确定性的早期识别,加上各方面的努力避免相关风险,直到不确定性减少或消除。这样一来,风险的概念就与科学知识紧密联系在一起,因此,只有足够的了解才能得出合理的结论,进而有效进行合理合适的风险管理。
在药品监督中的作用
药品和生物制品风险管理的现代探索源于1999年风险管理专职小组向FDA提交的报告。当时设立的这个工作组主要负责确定FDA内部正在进行的风险管理活动的技术合理性、一致性和有效性,并制定相关指导原则以改进这些活动的有效性,提高其效率。该工作组的最后报告“管理医疗产品使用风险”包括:创建风险管理框架、重点关注支持药品新药申请(NDAs)、生物制药和生物制剂生产许可证申请(BLA)以及上市前审批(PMA)和上市后监督活动。该报告没有明确指出与产品质量有关的风险管理,并解释说:“由于产品质量控制和制造过程中的质量保证受到高度的重视,产品本身带来的风险在美国并不常见。”尽管有这一项申明,但该报告还是继续引用了一些造成伤害和死亡的案例来说明QRM的重要性。
尽管1999年的报告是对监管机构风险管理和风险管理有效性的一次现代化尝试,但是质量风险管理这个主题还没有得到圆满解决。2002年8月,出现了一个完整的主动风险管理概念,包括内在和外在风险管理。FDA因此还提出了一项倡议《21世纪药品的cGMPs——一种基于风险的管理方法》。倡议目标如下:
* 鼓励制药行业尽早采用新技术以谋求进步。
* 促进现代质量管理技术的行业应用(包括质量体系方法在药品生产和质量保证等各个方面的实施)。
* 鼓励实施基于风险的管理方法。
* 保证基于合规性的监管审查正常进行。
* 加强FDA药品质量监管计划的一致性和协调性。
至2004年9月,关于上述举措的最终报告发布,阐述了FDA旨在达到这些目标完成的实施框架。尽管这些目标明确将风险管理列为重点领域,但仔细阅读最终报告,可以发现风险原则是该计划的基础。该报告表示,将采用质量管理和监管的体系模式,以供制药生产行业以及FDA等采用。尽管质量体系的概念已经在医疗器械监管范围内实施了一段时间(如ISO13485,医疗设备-质量管理体系-监管目的的要求,以及21CFR 820,质量体系法规),但是在生物制药行业应用这一模式是新颖的做法。
上述倡议依据最先进的科学技术,把相关风险作为基石,提出以下框架——
* 基于风险设立检查监督模型。
* 发布21CFR第11部分新指南,采用电子记录、电子签名时也需要考虑相关风险。
* 发布无菌加工新指南。虽然无菌生产加工的药品已有良好的生产规范,但仍需强调在生产过程中主动防止污染,并进一步估计采用风险管理原则,确保药品无菌。
“21世纪倡议”标志着药品监管的模式转变:过去的监管模式是按照制定的原则来操作,而现在的监管是从风险质量管理和合规性出发。该倡议还重点强调了高效的风险管理,如果风险管理不正确,管理效率将十分低下。风险管理应以高效率和有效的方式进行,以便为患者提供高效而有效的服务。
预告:下一篇将讨论该领域的主要管理文件ICH Q9质量风险管理。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



