神经精神新药竞争格局
发布时间:2018-09-27 14:35:40作者:吴健(科睿唯安)来源:医药经济报
神经精神新药竞争格局
揭密三类临床需求型市场
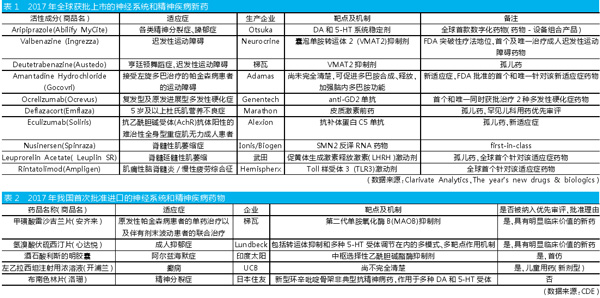
科睿唯安最新发布的新药报告The year’s new drugs & biologics 2017显示,在2017年全球首次批准的113个新化学药和生物药中,有9个中枢神经系统药物,以及1个精神疾病用药。
而根据我国《2017年度药品审评报告》,CDE在2017年首次批准了5个进口神经系统和精神疾病新药,其中有4个品种通过优先审评程序得以加快批准上市。
进一步对比2017年全球和我国获批上市的神经系统和精神疾病新药可以发现,国外获批的新药多是突破性的针对该领域罕见疾病的孤儿药,且大部分药物是针对某适应症的首个及唯一用药。
而2017年我国获批的神经系统和精神疾病新药主要集中在一些国外已上市而国内未上市的基础用药品种,将为我国患者提供更多治疗选择,满足临床用药需求。通过以下3个值得关注的获批品种市场情况的分析,可以获知我国神经系统和精神疾病用药市场有别于全球的特点和竞争情况。
帕金森病
2017年获准新药:甲磺酸雷沙吉兰
由Teva和Lundbeck共同开发的甲磺酸雷沙吉兰片(Azilect,安齐来)是第二代选择性不可逆单胺氧化酶B(MAOB)抑制剂,通过抑制MAOB进而增强脑内多巴胺的信号传递,也可增强左旋多巴的作用,具有神经保护和疾病修饰作用。
安齐来最早于2005年在以色列和欧洲上市,2006年在美国上市,用于帕金森病早期的一线单药治疗或与左旋多巴联用治疗中、重度帕金森病。2017年安齐来经批准在我国上市,用于原发性帕金森病患者的单药治疗以及伴有剂末波动患者的联合治疗。
【市场格局】
帕金森病(Parkinson’s disease,PD)是全球仅次于阿尔兹海默症的第二大神经退行性疾病,患者生活质量严重下降,并常出现多种并发症,给患者家庭和社会带来沉重负担。受庞大的人口基数和快速人口老龄化等因素的影响,我国PD患病人数保持增长并长期维持在高水平状态,预计到2030年我国PD病例数将达到500万例,占全球PD患病人数的一半。
PD的治疗包括药物治疗、手术治疗、运动疗法、心理疏导及照料护理等,其中药物治疗是首选和主要的治疗手段。目前我国临床用于PD治疗的药物主要包括普拉克索、多巴丝肼、恩他卡朋、恩他卡朋双多巴片、溴隐亭、吡贝地尔、司来吉兰、卡比多巴左旋多巴复方、苯海索、金刚烷胺等,其中普拉克索在PD药物整体市场中的份额接近40%,远超过其他品种。另外,除苯海索和金刚烷胺,大部分品种均是进口产品占据主导地位。
最新的雷沙吉兰、普拉克索、恩他卡朋、恩他卡朋双多巴片、溴隐亭、吡贝地尔6个品种目前在我国只有进口产品,但多家国内企业已对这6个品种进行相应仿制药的上市申报,且进程较快,2018年国产品种就有望上市。
此外,国内还有研发实力较强的企业进行PD新药研发。山东绿叶制药的注射用罗替戈汀缓释微球在中美同步进行临床试验,2018年3月获FDA批准无需开展Ⅱ期剂量探索临床试验,并在证明与对照药——目前唯一上市的罗替戈汀制剂(Neupro,透皮贴剂)生物等效的前提下豁免Ⅲ期临床试验;2018年4月获批准在我国进行Ⅲ期临床试验。中科院药物所自主开发的1.1类新药芬乐胺片目前处于临床Ⅰ期。第三代选择性MAOB抑制剂沙芬酰胺片已在国外上市多年,我国已有包括正大天晴、石药中奇、贵州恒顺药物研发等多家企业获得该药临床批件。
虽然甲磺酸雷沙吉兰片(安齐来)因属于“具有明显临床价值的新药”并获得优先审评在我国快速上市,但未来第三代MAOB抑制剂和国外其他新型PD药物会加速在我国的上市进程,国内已上市品种更会牢牢把握已有地位并开拓新的市场,PD药物市场容量扩增的同时,也会存在巨大的挑战和激烈的竞争,安齐来在我国的市场优势则有待考量。
抑郁症
2017年获准新药:氢溴酸伏硫西汀
Lundbeck研发的氢溴酸伏硫西汀片(Brintellix/Trintellix,心达悦)是一种多模式、多靶点的新型抗抑郁药物,通过抑制5-HT转运体的再摄取和调节5-HT受体两种作用模式,作用于6个药理学靶点(5-HT3、5-HT7、5-HT1D、5-HT1B、5-HT1A、5-HT转运体)而发挥综合性的抗抑郁疗效,并可改善抑郁症患者的认知功能。
心达悦在2013年率先在美国上市,2017年11月经批准在我国上市,用于治疗成人抑郁症,目前已在全球近80个国家上市。2018年5月,FDA更是通过了Trintellix的一项补充临床应用,即改善抑郁症急性期患者的信息加工速度。
【市场格局】
WHO数据还显示,西方发达国家的抑郁症患病率普遍比我国高。然而,受文化传统、健康意识、诊疗水平等因素影响,我国抑郁症识别率不足20%,治疗率不足10%,很多患者并没有得到及时的诊断和治疗,因此我国抑郁症实际患病率和患病基数可能远超预估。
目前我国抗抑郁药市场规模在药品整体市场中的占比还比较小,但每年以超过10%的增速在增长。临床主要使用的品种包括艾司西酞普兰、舍曲林、文拉法辛、帕罗西汀、度洛西汀等。其中艾司西酞普兰由于具有较好的安全性和有效性,临床使用较为广泛;而GSK的盐酸帕罗西汀肠溶缓释片是2017年国家药品谈判成功的36个品种中仅有的1个抗抑郁药,并被纳入国家医保目录,预计未来市场将进一步放量。另外,虽然5个临床抗抑郁常用品种目前都有国产品种上市,但在每个品种的细分市场中,进口产品的市场表现均优于国产品种。
研发方面,由于预计今后相关市场规模将进一步扩大,加之与其他治疗领域相比,我国已上市抗抑郁药物的生产企业和批文较少,目前国内有较多企业进行抗抑郁药物品种的仿制和申报,尤其以度洛西汀、文拉法辛和舍曲林为多。
值得注意的1类新药主要有:浙江华海药业的1.1类抗抑郁新药盐酸羟哌吡酮片被列入重大专项而获得优先审评,目前已进行到临床Ⅱ期;山东绿叶制药的1.1类抗抑郁新药盐酸安舒法辛缓释片已完成中国Ⅱ期,取得积极疗效并成功达到了主要及次要临床终点,美国Ⅱ期正在进行中;军科院毒研所和石药中奇的1.1类抗抑郁新药盐酸阿姆西汀肠溶片目前正处于国内临床Ⅰ期。
Lundbeck是专注于精神和神经系统疾病领域的制药企业,先前已在我国成功上市了草酸艾司西酞普兰片(来士普)、氢溴酸西酞普兰片(喜普妙)、氟哌噻吨美利曲辛片(黛力新)等抗抑郁药物。最新上市的氢溴酸伏硫西汀片(心达悦)可使Lundbeck在中国的产品组合更加多元和完善,并且Lundbeck可借助已经建立起来的成熟的销售渠道和营销模式,迅速打开心达悦的市场。
但是,随着国内抗抑郁药物市场参与者的不断增多,市场竞争程度和格局都将发生改变。尤其是科伦药业和复星医药的草酸艾司西酞普兰片,目前都已经通过一致性评价,将对Lundbeck的来士普产生冲击。Lundbeck的多个产品能否对其他企业的抗抑郁竞品形成“包围圈”,国产药物能否快速替代进口产品,都让人拭目以待。
儿童药
2017年获准新药:左乙拉西坦
左乙拉西坦作为癫痫治疗领域的一线用药,最早于1999年以片剂形式在美国上市,现已被广泛认为是癫痫治疗的“金标准”药物。目前我国已有包括片剂及口服溶液在内的多个进口和国产左乙拉西坦制剂上市,其中以UCB的产品占据较大市场份额。
此次UCB的左乙拉西坦注射用浓溶液(Keppra,开浦兰)能在2017年通过优先审评程序得到上市批准,是因为该品种是适用于儿童癫痫患者的新剂型,也是目前我国唯一上市的左乙拉西坦注射剂型。
【市场格局】
考虑到儿童用药研发的特殊性、市场的相对狭小性和临床用药的匮乏性,各国对儿童药均给予不同程度的倾斜政策,我国在儿童用药的研发创制、申报审评等方面也给予了鼓励和扶持。
但是,目前我国制药企业对儿童用药的研发并不十分积极。究其原因一是儿童药研发难度和风险较大,除了处方设计、剂型、辅料等临床前研究存在特殊要求和困难外,最重要的是临床和伦理问题。另一个重要原因是,我国在儿童药的研发保护、生产供应、医保定价、使用监管等方面的具体激励政策细则还未能明朗、完善和落实,企业缺乏实际的利益保障,进而对儿童药的投入不足。
儿童药短缺是实际存在的疑难,研发难度和伦理遵守也是必须考虑的问题,如何在两者间寻找到均衡的解决途径值得深思。短期内可加快引进国外已上市儿童药,加强国内外交流;长期则需要我国政府、企业、医疗机构和患者之间相互沟通和配合,突破认识瓶颈,提升儿童药研发能力,以最小的代价促进更多的儿童药上市。
小结<<<
目前,神经系统疾病和精神疾病在我国的知晓率、识别率和就诊率还比较低。这除了与我国现有的诊疗水平有关,也受到国民对该领域疾病的认识和观念影响,很多人往往没有意识到自己患病,即使意识到患病也会因“病耻感”而影响就医和治疗。
因此,对于神经系统和精神疾病治疗领域,新药的上市仅仅是产品市场周期的第一步,更重要的是提高公众对疾病的认识,加强对神经系统疾病和精神疾病患者和家庭的支持,创建患者、社区、医院、社会团体、政府机构等多方参与的协作化诊疗和关怀体系,并完善医疗保障系统,让更多、更好的药物能及时为神经系统疾病和精神疾病患者所用,满足治疗所需,最大程度地减轻患者的痛苦和社会负担。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



