飞检常态下经营企业勤练内功
发布时间:2018-08-29 18:18:33作者:黄健航来源:医药经济报
飞检常态下经营企业勤练内功
2017年,医药行业政策频出、热点不断。据了解,去年广州市食品药品监督管理局检查完成数147家,派出检查员302次,撤证18家,约谈企业10家,发布限期整改通报138家。可见,药品监管要求不断升级,监管更加严格。
2017年,广东省食品药品监督管理局发布了两个重要文件:1.《关于印发<2017年药品经营企业跟踪检查方案>的通知》(粤食药监办药通)[2017]21号;2.《关于印发<广东省食品药品监督管理局食品药品监督检查管理办法>的通知》(粤食药监办法[2017])11号。以上两个文件出台的目的均是打击药品流通领域违法违规行为。
在如今药品监管要求不断升级的大环境下,企业应该更加重视质量管理工作,才能立于不败之地。下面笔者对2017年广州市食品药品监督管理局通告的检查缺陷进行汇总分析。
主要缺陷比重最高
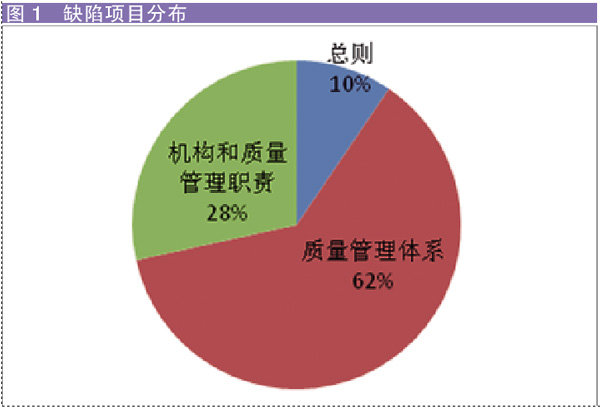
全年跟踪检查共判定缺陷项目共892项次,其中严重缺陷项31项,主要缺陷项511项,一般缺陷项350项。如图1所示。
从图表可知,主要缺陷项比重占比最高,占57%;紧接着是一般缺陷项,占39%;严重缺陷项则占4%。根据笔者的经验,检查员检查企业的重点是先判断企业有无违反严重缺陷项,然后看主要缺陷项,最后才看一般缺陷项。因此企业应坚决不触碰10项严重缺陷项,同时做好主要缺陷项,力争把一般缺陷项减到最少。
质量管理和储运缺陷最多
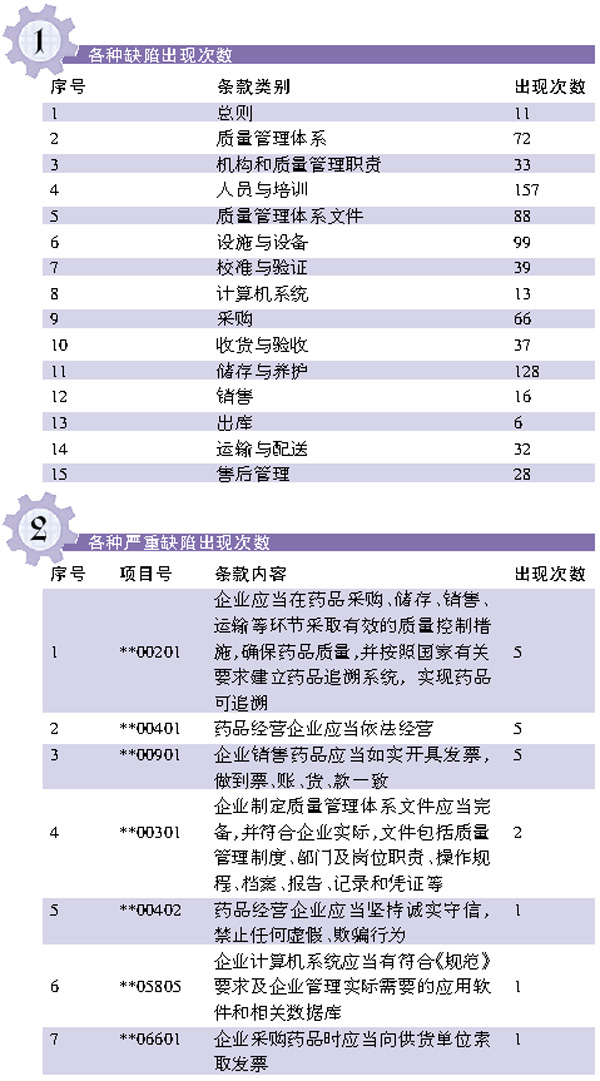
为更清楚缺陷的具体分布,笔者把所有缺陷进一步拆分,整理成表1。
从表1可知,人员与培训占比最高,达到19%;紧接着是储存与养护,达到15.5%;第三是设施与设备,达到12%。以上数据说明在质量管理部和储运部这两个部门所产生的缺陷项目是最多的。
撤证原因有哪些
那么,这些严重缺陷、主要缺陷项目具体的内容是什么?先来看看严重缺陷出现的次数(见表2)。
由表2可以看出,企业被撤证的原因主要集中在:
第一,未建立追溯系统。现行《药品经营质量管理规范现场检查指导原则》强调,企业应当在药品经营各环节采取质量控制措施,实现药品可追溯。但是,个别企业仍存在侥幸心理,未严格执行法规要求,建立可靠有效的追溯体系,无法保障药品经营各环节的可追溯性。
第二,未能依法经营。这反映出个别企业法律法规意识仍然淡薄,对飞行检查的常态和最严格监管仍抱有侥幸心理,企业负责人对质量负责人的建议不采纳,质量负责人的裁决权没有真正落实。
第三,未开具发票。检查企业购销的票、账、货、款是否相符,是药品经营企业日常监管和飞行检查工作的重中之重。个别企业为了降低财务成本,在药品销售过程中仍然不开发票或不及时开具发票。企业若想在监管要求越来越严的形势下不被淘汰,应加强投入硬件,诚信经营。
主要缺陷TOP10
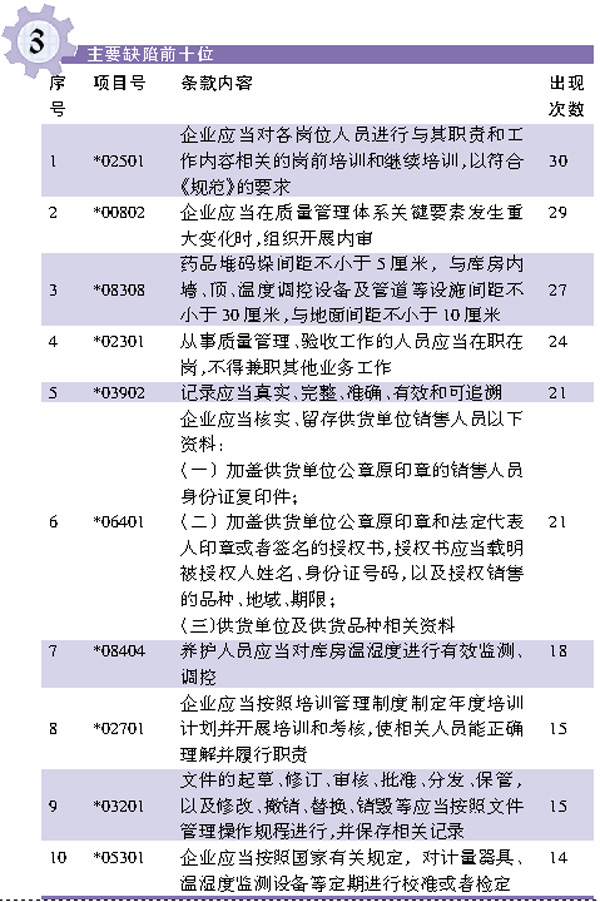
根据表3,笔者将从人员培训、仓库储存与养护、数据上传等方面进行分析。
第一,质量管理部门未按要求履行职责,人员培训不足(缺陷条款出现157次,在所有缺陷条款中出现最多)。根据笔者的经验,部分企业的培训计划流于形式,没有真正落实到位。另外,部分企业对新法规要求不够重视,学习积极性不高,部分未能及时组织学习。笔者认为,培训不认真落实容易造成岗位人员无法正确行使职能,不能严格履行质量管理职责,这也是造成企业质量管理混乱、出现严重违反GSP规定行为的重要原因。
第二,仓库储存与养护不到位 (缺陷条款出现128次,排名第二)。企业普遍存在药品与非药品混放、药品堆码垛间距不符合要求、不合格药品未及时处理并摆放于专区、库房温湿度超标、仓管人员未能及时有效采取措施进行调控等问题,个别企业仓库因库存太多占用了一些必要的功能库(如中药材库、中药饮片库)。
第三,部分企业未按照省、市要求上传企业经营品种的购销存数据到电子监管平台 (该缺陷在主要缺陷出现次数最多的条款中排名第五)。个别企业不上传购销存数据,或上传不完整,部分企业只将数据上传省局平台,不上传市局平台。
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用, 包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。



