泽璟制药的“钱”景
发布时间:2020-01-08 17:54:07来源:医药经济报
2019年12月31日,中国证监会同意苏州泽璟生物制药股份有限公司(简称“泽璟制药”)科创板首次公开发行股票注册。2020年1月6日,泽璟制药发布发行安排及初步询价公告,正式启动发行,初步询价日为1月9日。这两则消息标志着,自科创板落地以来,资本市场终于迎来第五套标准的首家企业,这一具有里程碑意义的事件标志着中国A股市场对未盈利医药创新型企业所体现的极大的重视、支持和包容。

未实现盈利就登陆资本市场的创新型生物制药公司不乏先例,包括信达生物、君实生物、百济神州、和记黄埔等从事创新药研发的制药公司都在实际盈利之前于香港或纳斯达克等资本市场上市。随着这些公司的产品研发、新药审批、商业销售的逐步进展,已经为投资者带来回报。信达生物-B在2018年10月在港交所上市时市值175亿港币,2019年3月(商业化之前)市值达到389亿港币左右,5个月投资收益率达222%。君实生物-B在2018年12月在港交所上市时市值155亿港币,2019年4月(商业化2个月左右)市值达到258亿港币左右,4个月投资收益率达166%。百济神州2016年在美国纳斯达克上市时市值为7.5亿美元,目前市值已经涨至100亿美元左右,三年累计投资收益率达1600%。
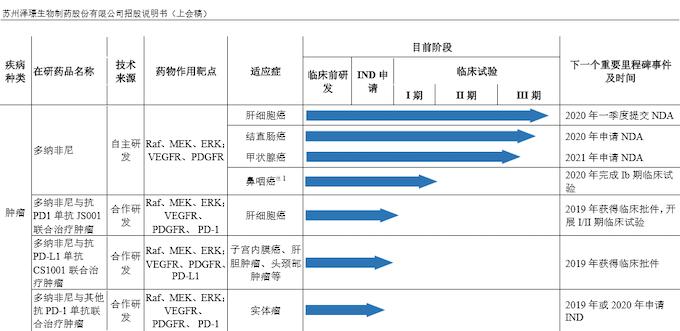
根据招股意向书的披露可看出,泽璟制药作为创新驱动型新药研发企业拥有多样化的产品管线,截至2019年12月9日,正在开展11个创新药物的29项临床研究。核心在研药品多纳非尼先后获得四项国家重大新药创制专项支持,计划在2020年第一季度向NMPA提交NDA申请,有望成为中国首个上市的一线治疗晚期肝细胞癌的国产靶向新药。外用重组人凝血酶处于Ⅲ期临床试验阶段,有望成为全球第二家、国内唯一采用基因重组方法生产的产品。杰克替尼也是“十三五”国家重大专项支持项目的另一个化学新药,是中国唯一处于Ⅱ期临床阶段的治疗中高危骨髓纤维化的靶向药物,有望进入有条件批准审批通道。
泽璟制药自2020年开始,将以每年至少一个新产品/新适应症的上市申请的速度,推出其研发成果,加快产品管线的商业化进程。
近期,泽璟制药公布了一条重磅信息,多纳非尼一线治疗晚期肝细胞癌的Ⅲ期注册临床研究获得成功,达到预设的主要终点以及安全性结果。在未接受过系统治疗的不可手术或转移性晚期肝细胞癌患者中,多纳非尼治疗组的中位总生存期(mOS)显著优于对照药物索拉非尼治疗组,达到统计学上差异显著性且具有临床意义的延长。多纳非尼组在3级及以上不良事件发生率、与药物相关的导致停药或减量的不良事件发生率等方面显示出更优的安全性。试验中未出现新的或超出预期的重大安全性问题。有关该项研究的详细数据,将于2020年适时在国际国内临床肿瘤学术大会上公布。
肝细胞癌市场潜力巨大, 多纳非尼将是泽璟制药第一块“试金石”
原发性肝癌是我国第四位的常见恶性肿瘤,死亡率仅次于肺癌。中国每年新发病人约有 46.2万人,每年死亡人数达到42.2万人。原发性肝癌治疗手段非常缺乏,肝癌治疗药物的研发历程也让全球制药公司充满挫折感。自2007年索拉非尼获批之后,直至2018年才有第二个靶向药物仑伐替尼获批,仑伐替尼以非劣于索拉非尼作为临床评价标准。中国的肝癌靶向药物市场在2019年快速放量,从2017年的3.4亿人民币迅速增至2019年的近40亿人民币的销售额。据Frost & Sullivan的预测,2030年肝细胞癌一线靶向药市场的临床可惠及的人口渗透率将提升至43.2%,整体市场规模将达到160.7亿元人民币。
在公司的网站上了解到,该试验主要研究者秦叔逵教授和毕锋教授这样评述:“多纳非尼是晚期肝细胞癌治疗领域十二年来第一个在头对头比较的大型III期临床试验中OS优于索拉非尼的小分子靶向药物。多纳非尼应是我国重大新药创制的成果之一,可喜可贺!” 多纳非尼将是泽璟制药第一块“试金石”。
创新药布局多适应症研究, 探索 “多点开花”
近年来, PD-1/PD-L1免疫检查点抑制剂在肿瘤免疫治疗领域的临床应用,正在改变业界及资本市场对于一个创新药物成功的定义。一个创新药“多点开花”,获取多个不同的适应症,是基于对创新药作用机理和治疗多种不同疾病的认识和临床开发的不断深入和拓展。
多适应症+联合研究:泽璟制药的招股意向书显示,多纳非尼单药治疗在结直肠癌、甲状腺癌、鼻咽癌的临床研究都已在开展中,而且与多个抗PD-1/PD-L1单抗联合治疗肝细胞癌、子宫内膜癌、肝胆肿瘤、头颈部肿瘤的研究也在进行中。
在多纳非尼治疗难治型甲状腺癌的研究,也获得了多纳非尼治疗RAIR-DTC的国内多中心Ⅲ期临床研究的主要负责人、北京协和医院核医学科林岩松教授的高度评价:“多纳非尼的Ⅱ期临床试验结果展现了多纳非尼同类最佳的治疗潜力”。
此外,泽璟制药的杰克替尼具有抑制JAK激酶的作用,也是1类新药。据浙江大学血液肿瘤重点实验室主任、浙江大学医学院附属第一医院血液科主任金洁教授介绍,杰克替尼治疗骨髓纤维化的安全性和有效性初步数据令研究者印象深刻,患者在治疗后缩脾效果显著,且对MF患者伴有的贫血也有很好的改善。杰克替尼还具备在免疫炎症性疾病中的更广泛的临床应用潜力。据招股意向书,泽璟制药已经启动或申请了盐酸杰克替尼片治疗重症斑秃、特发性肺纤维化、移植物抗宿主病、类风湿性关节炎、强直性脊柱炎等适应症Ⅱ期临床试验。“多点开花”在杰克替尼这个药物上也体现充分。杰克替尼正在开发众多适应症,也使得杰克替尼“钱途”值得期待。
涉猎领域广泛, 小分子药物和大分子药物齐头并进
泽璟制药也加大了在肝胆疾病领域的新药研发,3个小分子新药ZG5266、 ZG0588和ZG170607主要针对原发性胆汁性肝纤维化和非酒精性脂肪肝炎(NASH)等疾病。上述疾病本身异质性高、发病机理复杂,属于目前中国尚无任何批准药物的常见病,全球范围内也仅有奥贝胆酸可用于原发性胆汁性肝纤维化。可以看出,泽璟制药正积极布局“掘金”后肿瘤时代。
在大分子药物方面,目前处于Ⅲ期临床试验阶段的外用重组人凝血酶是中国唯一进入外科手术止血临床试验的重组蛋白质止血新药,并计划于2021年申请NDA;据资料显示,2018年中国有外科手术约6,000万台,凝血市场容量高达百亿市场规模。
泽璟制药显然也考虑了未来的战略发展,通过整体收购拥有世界先进水平的多靶点抗体技术平台和产品管线丰富的美国GENSUN BIOPHARMA INC.,直接布局到第二代肿瘤免疫治疗的新领域,专注于双特异抗体药物的开发。GENSUN拥有自主知识产权的TriGen、CheckGen和TGen技术平台,已开发出10多种抗体候选新药。泽璟制药的双靶点抗体药物ZG005和ZG006预计于2020-2021年在申请IND,公司在大分子药物研发领域从传统的复杂蛋白质药物迅速跨入到First-in-Class及Best-in-Class抗体新药行列。泽璟在创新抗体领域的“钱景”值得期待。
创始人与领导者的使命初心 驱动企业砥砺前行
泽璟制药董事长盛泽林博士毕业于美国迈阿密大学药理学专业,是最早一批回国布局生物和化学新药的创业企业的代表人物之一。盛博士在生物创新药企创业的经历,以及担任外资新药研发公司首席营运官的经历,使他具备了全面的新药公司管理和系统研发经验,是不可多得的兼具科学和研发经验、以及商业运营和管理经验的医药创业家和领导者。盛泽林博士及其管理团队风格低调务实,在他看来,一个新药的研发,8年以上的研发进程非常正常,沉下心来,避开浮躁的外界影响,踏踏实实开展新药研发非常重要。
曾为血液科医生的盛泽林博士对临床医学和国内患者的需求有深刻理解。企业成立之初,即开始研发治疗国内患者常见疾病的创新小分子靶向药物以及高难度重组蛋白质药物,以满足中国患者的临床急迫需求。
泽璟制药即将迈上新台阶、踏上新征程、并面临更加广阔的历史机遇。可以预见,凭借泽璟创始人的使命感和初心,公司扎实的研究管线布局,借力资本市场,加上国家药监部门审评审批制度改革的加速,有理由相信,泽璟制药未来多个创新药进入商业化阶段必将产生良好商业回报。随着科创板IPO上市,祝福泽璟制药成为中国创新药的一股新锐力量!
此内容为《医药经济报》融媒体平台原创。未经《医药经济报》授权,不得以任何方式加以使用,包括转载、摘编、复制或建立镜像。如需获得授权请事前主动联系:020-37886610或020-37886753;yyjjb@21cn.com。






